18/09/2021
El cerebro, a diferencia de otros órganos expuestos al entorno como la piel o las mucosas, se encuentra resguardado dentro del cuerpo, protegido por una estructura vital conocida como la Barrera Hematoencefálica (BHE). Esta barrera es un sistema de defensa extraordinariamente eficaz que impide que la mayoría de los compuestos extraños y potencialmente dañinos penetren en el delicado tejido cerebral. Su existencia es fundamental para mantener la homeostasis cerebral y asegurar el correcto funcionamiento de nuestro órgano más complejo. Comprender su composición y funcionamiento no solo es fascinante, sino crucial para el desarrollo de futuras terapias.
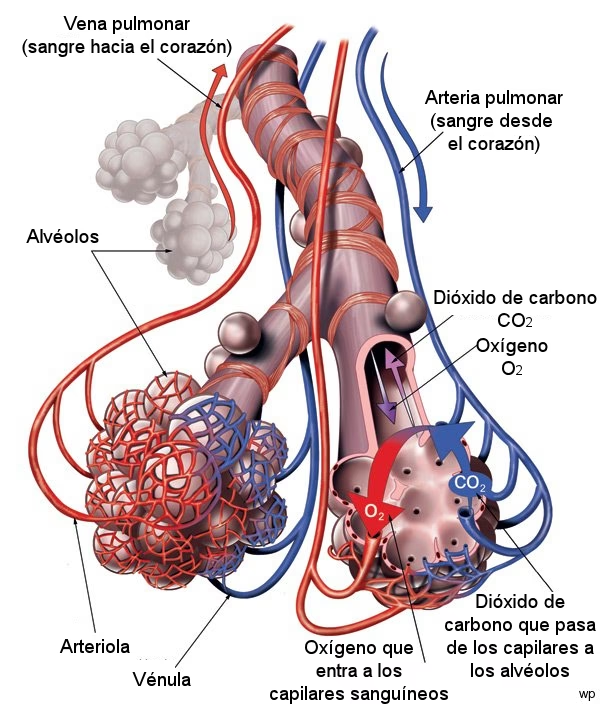
La BHE está formada por una red intrincada de microcapilares, que son parte integral del sistema vascular que transporta sangre por todo el cuerpo. Sin embargo, los capilares que componen la BHE no son como cualquier otro capilar; poseen características únicas que los distinguen y les otorgan su formidable capacidad protectora.
- Composición y Características Únicas de la Barrera Hematoencefálica
- Investigación y Modelos In Vitro de la BHE
- Preguntas Frecuentes sobre la Barrera Hematoencefálica
- ¿Qué es la Barrera Hematoencefálica (BHE)?
- ¿Por qué es tan importante la BHE para la salud cerebral?
- ¿Cómo se diferencian los capilares de la BHE de otros capilares del cuerpo?
- ¿Qué son las uniones estrechas y cuál es su papel en la BHE?
- ¿Cómo afecta la BHE el desarrollo de fármacos para el cerebro?
Composición y Características Únicas de la Barrera Hematoencefálica
Los microcapilares de la BHE están constituidos por células endoteliales capilares específicas del cerebro. Estas células exhiben particularidades morfológicas distintivas que son la clave de su función de barrera. Entre ellas se incluyen la presencia de uniones estrechas (tight junctions o TJs) entre células endoteliales individuales, la ausencia de fenestraciones (poros) y una actividad pinocitótica (proceso de ingestión celular) casi nula. Estas características son el resultado de la interacción y el contacto directo de las células endoteliales microvasculares con otras células cerebrales como los pericitos, los astrocitos y las células de la microglía.
Mientras que en otras partes del cuerpo el intercambio de nutrientes y oxígeno entre la sangre y los tejidos ocurre fácilmente a través de las paredes capilares, en el cerebro, muchas sustancias esenciales no pasan directamente, sino que son transportadas por sistemas específicos ubicados en las células endoteliales. Estos sistemas especializados mueven las sustancias que el cerebro necesita a través de la BHE de manera selectiva. La presencia de las uniones estrechas es un factor limitante crucial, ya que restringe o excluye el paso de muchos compuestos terapéuticos útiles, como antibióticos, quimioterápicos, péptidos y proteínas, desde la sangre hacia el cerebro.
Mecanismos de Transporte a Través de la BHE
Para superar la selectividad de la BHE, el cerebro ha desarrollado diversos y únicos mecanismos de transporte. Estos sistemas permiten el paso de nutrientes esenciales y la eliminación de productos de desecho, al tiempo que mantienen la integridad de la barrera frente a sustancias nocivas. A continuación, se detallan los principales mecanismos identificados:
| Mecanismo de Transporte | Características | Ejemplos de Sustancias Transportadas |
|---|---|---|
| Transportadores ABC (ATP-binding cassette) | Transportan compuestos liposolubles y no polares; requieren energía ATP. | Fármacos lipofílicos, metabolitos. |
| Transportadores de Solutos (Solute Carriers) | Facilitan el paso de moléculas hidrofílicas específicas. | Glucosa, aminoácidos, nucleósidos, péptidos pequeños. |
| Transcitosis Mediada por Receptor | Involucra la unión de sustancias a receptores específicos en la superficie celular, seguida de internalización y tránsito. | Transferrina, lipoproteínas, inmunoglobulinas, citocinas. |
| Transcitosis Mediada por Adsorción | Basada en la interacción electrostática entre la sustancia y la membrana celular, seguida de internalización. | Histonas, péptidos penetrantes en células. |
Estos mecanismos demuestran la complejidad y la especificidad con la que la BHE regula el paso de sustancias, asegurando que solo lo necesario y seguro llegue al cerebro.
El Rol Crítico de las Uniones Estrechas
La característica principal que diferencia la microvasculatura de la BHE de la de otras partes del cuerpo es la presencia de uniones de adhesión (AJs) y, fundamentalmente, las uniones estrechas (TJs). Estas estructuras limitan la permeación de solutos en la sangre por difusión entre las células endoteliales hacia los espacios extracelulares del cerebro. Las TJs son formadas por las células endoteliales en la interfaz entre la sangre y el cerebro, y están asociadas con los astrocitos del cerebro.
Las TJs están compuestas principalmente por proteínas transmembrana de adhesión como las claudinas, las ocludinas y las moléculas de adhesión de unión (JAMs). Estas, a su vez, están ancladas a las células endoteliales por proteínas de andamiaje citoplasmáticas y proteínas reguladoras como ZO-1, ZO-2, ZO-3 y cingulina. Cualquier alteración de estas proteínas disminuye la resistencia de las TJs y provoca una BHE más permeable o 'con fugas'. La forma en que estas proteínas se organizan e interactúan juega un papel crucial en el grado de integridad de la barrera. La integridad de la BHE y la presencia de TJs se demuestran por una inhibición del movimiento iónico a través de la difusión paracelular entre las células endoteliales, y puede medirse por una alta resistencia transelectrical in vivo de la BHE.
Interacciones Celulares que Fortalecen la BHE
La asociación de la microglía, los astrocitos, las terminaciones nerviosas y los pericitos es esencial para la formación de las TJs por parte de las células endoteliales cerebrales. Estas células liberan agentes vasoactivos y citocinas que pueden modificar el ensamblaje de las TJs y la permeabilidad de la barrera, e influir en la expresión polarizada de transportadores específicos dentro de las células endoteliales cerebrales en las membranas luminal y abluminal. La importancia de estas interacciones célula-célula en la formación, estabilización y aumento de las TJs ha sido demostrada en numerosos estudios in vitro mediante aumentos de la resistencia transelectrical (TER) a través de monocapas de células endoteliales en comparación con cocultivos.
Marcadores de Células Endoteliales Especializadas
La capa interna de todos los vasos microcapilares en la BHE está formada por células endoteliales. Aunque estas células pueden diferir en sus propiedades de barrera, comparten algunas características con las células endoteliales de todas las partes del cuerpo. Estos marcadores celulares endoteliales especiales permiten distinguir entre células endoteliales y no endoteliales. Uno de los principales marcadores de células endoteliales es el factor von Willebrand (vWF, también llamado factor VIII). Esta glicoproteína sanguínea es expresada por las células endoteliales y, tras su liberación en la sangre, es importante para la coagulación sanguínea (hemostasia). El segundo marcador de células endoteliales es PECAM-1 (molécula de adhesión célula-endotelial plaquetaria), también llamada CD31 (clúster de diferenciación), que se expresa en la superficie celular de las células endoteliales. Está involucrada en la adhesión célula-célula e interactúa con otras moléculas CD-31 o proteínas de la familia de las integrinas. También la VE-cadherina (cadherina-5), una proteína de adhesión celular, se expresa específicamente en las células endoteliales. El dominio citoplasmático de esta proteína interendotelial está conectado al citoesqueleto de actina a través de α-, β- y γ-cateninas. La VE-cadherina es importante para la organización de nuevos vasos sanguíneos y está involucrada en varios procesos reguladores de las células endoteliales. Estos marcadores pueden ser teñidos por anticuerpos específicos y visualizados mediante microscopía de fluorescencia, siendo cruciales para la investigación.
Investigación y Modelos In Vitro de la BHE
El estudio de la BHE es complejo debido a su intrincada naturaleza in vivo. Para ello, se han desarrollado diversos modelos in vitro que buscan replicar sus estructuras y funciones, permitiendo una investigación más controlada y ética. Estos modelos son fundamentales para entender las interacciones entre nuevos materiales y células vivas, así como para validar la posibilidad de transporte de compuestos a través de la barrera.
Modelos de Cultivo Celular
Los modelos de cocultivo, utilizando células primarias recién aisladas, tienen la ventaja de que estas células suelen expresar la mayoría de las propiedades y funciones celulares importantes y, bajo las condiciones adecuadas, pueden generar las características de una barrera hermética. Sin embargo, existen desventajas significativas, como la dificultad para obtener tejido cerebral humano fresco, la pureza de las células después del aislamiento y la variabilidad del éxito y la función del aislamiento celular, que dependen del donante.
Afortunadamente, existen líneas celulares endoteliales cerebrales disponibles que exhiben la mayoría de las características y propiedades, aunque las propiedades de barrera de las células primarias, como la TER, suelen ser más altas y se acercan más a la situación in vivo. Por lo tanto, la mayoría de los modelos in vitro utilizan células primarias de diferentes animales. Modelos bien establecidos basados en células primarias de rata, porcino y especialmente bovino son de uso rutinario. Las células endoteliales cerebrales aisladas a menudo se cocultivan con astrocitos o pericitos, ya que se ha demostrado que esto aumenta la TER y las propiedades de las TJs, e induce y estabiliza la expresión de proteínas específicas de la barrera.
Aislamiento y Caracterización de Células
Un método desarrollado para aislar células endoteliales microcapilares cerebrales humanas ha sido adaptado para el aislamiento de células endoteliales de tejido cerebral porcino. Este proceso implica la digestión del tejido cerebral con enzimas como la colagenasa tipo IV, seguida de la separación de los pequeños capilares de los restos de mielina mediante un gradiente de Percoll. Una segunda digestión con una mezcla de colagenasa/dispasa y un gradiente de Percoll adicional asegura una alta purificación de los microvasos con pocas células contaminantes adicionales.
Para el aislamiento de pericitos cerebrales, los microvasos se resuspenden en un medio con puromicina, un antibiótico nucleósido que es tóxico para fibroblastos y otras células contaminantes, pero que puede ser transportado por transportadores de eflujo fuera de las células endoteliales cerebrales sin exhibir un efecto tóxico. Esta metodología mejora significativamente la pureza de las células capilares cerebrales aisladas.

La caracterización precisa de los pericitos es un desafío. Un criterio es su estructura morfológica: larga, delgada y estirada. Estas células también son positivas para la actina de músculo liso, desmina, NG-2, receptor del factor de crecimiento derivado de plaquetas (PDGFR)-β, y aminopeptidasa A y N. Sin embargo, ninguno de estos marcadores es absolutamente específico para los pericitos, y ninguno de ellos reconoce a todos los pericitos, ya que su expresión es dinámica, difiere según la ubicación de la fuente celular y depende de la etapa de desarrollo celular. La identificación de pericitos generalmente se basa en una combinación de métodos de tinción, morfología estructural e imágenes confocales de alta resolución.
Evaluación de Nuevos Biomateriales para el Cerebro
La investigación de nuevos biomateriales para la administración de fármacos al cerebro se centra principalmente en métodos para dirigir la BHE o para actuar como transportadores a través de la barrera. La mayoría de las estrategias de investigación se enfocan en el uso de péptidos o nanopartículas específicamente diseñadas para características únicas de la BHE, con el fin de ser transportadas a través de ella. Por lo tanto, los estudios in vitro de estos compuestos con modelos de la BHE son necesarios para comprender las interacciones entre los nuevos materiales y las células vivas, y para validar la posibilidad de transporte. Realizar estudios con cada nuevo compuesto in vivo no sería factible; de ahí la importancia de los modelos in vitro.
Pruebas de Biocompatibilidad y Toxicología
Para determinar si un nuevo compuesto o nanopartícula es biocompatible y no exhibe efectos tóxicos, se utilizan varias pruebas. El test MTT o MTS es el más utilizado para examinar los efectos de los compuestos en la viabilidad celular. En esta prueba, las células se incuban en presencia o ausencia del nuevo compuesto y luego se añade MTS/MTT. El nivel de reducción del sustrato MTS/MTT por las deshidrogenasas ubicadas en las membranas mitocondriales de las células, que forman formazán, se correlaciona directamente con la viabilidad de las células. Cuanto más MTT se convierte enzimáticamente en formazán, mayor es la viabilidad celular.
Además de la viabilidad celular, también se debe evaluar la citotoxicidad. La prueba LDH (lactato deshidrogenasa) es la más común para examinar la toxicidad celular de un compuesto. La LDH es una enzima citoplasmática, y si un biomaterial/nanopartícula causa toxicidad celular, la membrana celular de la célula afectada se vuelve permeable. Después de la exposición de las células a un compuesto de prueba, se recoge el sobrenadante y se determina el contenido de LDH, comparándolo con los controles. Cuanto más tóxico es un compuesto, más LDH está presente en el sobrenadante y más sustrato se convierte. Es importante utilizar más de una prueba para excluir una alteración del sistema de prueba por parte de nuevos biomateriales/nanopartículas.
Estudios de Interacción y Captación de Nanopartículas
Los estudios iniciales de la interacción de nuevos compuestos con la BHE se realizan con sistemas de una sola célula. Además de los estudios de toxicidad, el siguiente paso es examinar cómo los compuestos interactúan con las células. Las nanopartículas a menudo son internalizadas, y esta internalización puede causar una disminución de la viabilidad celular y/o un aumento de la toxicidad celular. El nivel de daño de las células por las nanopartículas puede asociarse con diferentes propiedades, como la concentración, la forma, el tamaño y la composición química de los nanomateriales o combinaciones de los mismos. Si un compuesto es captado, la pregunta que generalmente debe responderse es su destino después de la internalización dentro de la célula, especialmente si las nanopartículas se van a utilizar para transportar compuestos a través de la barrera.
Para investigar mecanismos de captación como la pinocitosis o la endocitosis mediada por receptores, se pueden utilizar inhibidores específicos de estos sistemas. Además, se dispone de anticuerpos específicos para teñir estructuras y orgánulos intracelulares individuales, que pueden utilizarse para rastrear o localizar nanopartículas dentro de las células. Un criterio para estudiar nanopartículas u otros péptidos/proteínas es que contengan un método de detección adecuado, siendo el óptimo una etiqueta fluorescente o la visibilidad por microscopía óptica.
Uno de los inconvenientes en el estudio de nanopartículas en células es que la detección de la nanopartícula está limitada por la apertura numérica y la longitud de onda de la luz visible alcanzable por microscopía. Debido al pequeño tamaño de las nanopartículas individuales, estas se encuentran por debajo de la resolución máxima obtenible por microscopía. Generalmente, solo es posible detectar aglomeraciones de nanopartículas dentro de las células. Para detectar nanopartículas individuales en la superficie celular o incluso dentro de las células, es necesario utilizar microscopios electrónicos con una resolución máxima más alta. Aunque la resolución de los microscopios electrónicos de transmisión o de barrido es mayor en comparación con los microscopios ópticos, no todas las nanopartículas o compuestos pueden detectarse. Solo las nanopartículas con un número atómico o densidad alta, como el oro o la plata, pueden detectarse mediante estas técnicas. Otros nanomateriales o compuestos con un número atómico más bajo pueden recubrirse con una fina capa de oro para hacerlos adecuados para la microscopía electrónica.
Preguntas Frecuentes sobre la Barrera Hematoencefálica
¿Qué es la Barrera Hematoencefálica (BHE)?
La Barrera Hematoencefálica es un sistema de protección altamente selectivo compuesto por células endoteliales especializadas que recubren los capilares sanguíneos del cerebro. Su función principal es controlar el paso de sustancias desde la sangre hacia el tejido cerebral, protegiéndolo de toxinas y patógenos, mientras permite el acceso de nutrientes esenciales.
¿Por qué es tan importante la BHE para la salud cerebral?
La BHE es crucial porque mantiene un ambiente interno estable para el cerebro, esencial para su funcionamiento óptimo. Protege al cerebro de fluctuaciones en la composición sanguínea, de sustancias tóxicas que podrían circular por la sangre y de infecciones, asegurando que solo los compuestos necesarios lleguen a las neuronas.
¿Cómo se diferencian los capilares de la BHE de otros capilares del cuerpo?
Los capilares de la BHE se distinguen por sus uniones estrechas intercelulares que limitan el paso de sustancias, la ausencia de fenestraciones (poros) y una baja actividad pinocitótica. Además, interactúan estrechamente con pericitos y astrocitos, lo que refuerza su función de barrera, a diferencia de otros capilares que suelen ser más permeables.
¿Qué son las uniones estrechas y cuál es su papel en la BHE?
Las uniones estrechas (TJs) son complejos de proteínas que sellan el espacio entre las células endoteliales de la BHE, impidiendo el paso paracelular (entre células) de la mayoría de las sustancias. Son esenciales para mantener la integridad y la baja permeabilidad de la barrera, y su disrupción puede comprometer la protección cerebral.
¿Cómo afecta la BHE el desarrollo de fármacos para el cerebro?
La BHE representa un desafío significativo en el desarrollo de fármacos, ya que su selectividad impide que muchos compuestos terapéuticos, incluyendo antibióticos y quimioterápicos, lleguen al cerebro en concentraciones efectivas. La investigación se centra en encontrar estrategias para que los fármacos puedan atravesar esta barrera de manera segura y eficaz.
En resumen, la Barrera Hematoencefálica es un guardián sofisticado y vital para la salud de nuestro cerebro. Su compleja estructura y sus mecanismos de transporte selectivo la convierten en un escudo indispensable, y su estudio sigue siendo un campo activo y prometedor en la neurociencia y la medicina.
Si quieres conocer otros artículos parecidos a La Barrera Hematoencefálica: Guardián del Cerebro puedes visitar la categoría Cabello.