20/06/2024
La electroforesis capilar (EC) es una técnica analítica poderosa y versátil que ha transformado la forma en que los científicos separan y analizan una amplia gama de compuestos. Desde su concepción, ha ofrecido una alternativa eficiente y de alta resolución a los métodos de separación tradicionales, destacándose por su rapidez, mínima necesidad de muestra y capacidad para manejar mezclas complejas. A diferencia de las técnicas clásicas, la EC se realiza dentro de tubos capilares extremadamente estrechos, lo que le confiere ventajas únicas en términos de disipación de calor y eficiencia de separación.
- El Modo Normal de Funcionamiento de la Electroforesis Capilar
- Instrumentación Básica de la Electroforesis Capilar
- Métodos de Detección en Electroforesis Capilar
- Modos de Separación en Electroforesis Capilar
- Eficiencia y Resolución en Electroforesis Capilar
- Aplicaciones de la Electroforesis Capilar
- Preguntas Frecuentes (FAQ)
- ¿Qué es el flujo electroosmótico (EOF) en electroforesis capilar?
- ¿Cómo se separan los analitos en el modo normal de EC si todos se mueven en la misma dirección?
- ¿Cuáles son las dimensiones típicas de un capilar utilizado en electroforesis capilar?
- ¿Se pueden separar moléculas neutras con electroforesis capilar?
- ¿Qué ventajas ofrece la electroforesis capilar frente a otras técnicas de separación como la HPLC?
El Modo Normal de Funcionamiento de la Electroforesis Capilar
En el corazón de la electroforesis capilar reside un principio fundamental: la separación de iones basada en su movilidad electroforética bajo la influencia de un campo eléctrico aplicado. Sin embargo, lo que distingue el modo más común de EC es la combinación de este movimiento electroforético con un fenómeno conocido como flujo electroosmótico (EOF).
El EOF es el movimiento global del tampón o solución electrolítica a través del capilar. Se genera cuando se aplica un campo eléctrico a una solución dentro de un capilar que tiene cargas fijas en su pared interior. En un capilar de sílice fundida, que es el tipo más común, los grupos silanol (Si-OH) en la pared interna se ionizan a grupos silanoato (Si-O-) con carga negativa a valores de pH superiores a tres. Estos grupos negativos atraen a los cationes positivos de la solución tampón, formando dos capas internas de cationes en la pared del capilar: una capa fija (adherida a los silanoatos) y una capa móvil (más alejada). Cuando se aplica un campo eléctrico, la capa catiónica móvil es arrastrada hacia el cátodo (electrodo negativo), y como estos cationes están solvatados, arrastran consigo la mayor parte de la solución tampón, creando el EOF.
En el modo normal de EC, el EOF es típicamente dirigido hacia el cátodo. Esto significa que, en la mayoría de los sistemas, la solución tampón fluye a través del capilar desde el vial de origen hacia el vial de destino. Lo crucial es que, en este modo, todos los iones, ya sean positivos o negativos, son arrastrados a través del capilar en la misma dirección por el EOF. La separación de los analitos ocurre a medida que migran debido a sus diferencias en movilidad electroforética.
La movilidad electroforética es la velocidad a la que una partícula cargada se mueve en respuesta a un campo eléctrico. Las partículas cargadas positivamente son atraídas hacia el cátodo, mientras que las cargadas negativamente son atraídas hacia el ánodo. Sin embargo, dado que el EOF es generalmente más potente que la movilidad electroforética individual de los analitos, incluso los aniones pequeños y triplemente cargados son arrastrados hacia el cátodo por el flujo del tampón. Los analitos cargados negativamente son retenidos más tiempo en el capilar debido a que su movilidad electroforética los impulsa en dirección opuesta al EOF. Por lo tanto, el orden de migración observado por el detector es el siguiente: los cationes pequeños y con múltiples cargas migran rápidamente, seguidos por otros cationes, luego las especies neutras (que migran con la velocidad del EOF), y finalmente los aniones, siendo los aniones pequeños y con múltiples cargas los que son retenidos más fuertemente.
La velocidad del EOF depende de la fuerza del campo y de la densidad de carga de la pared del capilar, que a su vez es proporcional al pH de la solución tampón. El EOF aumentará con el pH hasta que todos los silanoles disponibles en la pared del capilar estén completamente ionizados.
Instrumentación Básica de la Electroforesis Capilar
La instrumentación necesaria para realizar la electroforesis capilar es relativamente sencilla. Un sistema básico de EC se compone de varios elementos clave:
- Vial de muestra y viales de origen/destino: Contienen la muestra a analizar y las soluciones tampón donde se sumergen los extremos del capilar.
- Capilar: Es el corazón del sistema, un tubo estrecho donde ocurre la separación. Están hechos principalmente de sílice fundida y suelen estar recubiertos con polímeros como poliimida o teflón para aumentar su flexibilidad. Las dimensiones típicas de un capilar son de 25 a 75 cm de longitud, con un diámetro exterior de 300 a 400 µm y un diámetro interior de 25 a 75 µm. El diámetro interno pequeño es crucial para una disipación de calor eficiente.
- Electrodos: Sumergidos en los viales de origen y destino, aplican el campo eléctrico.
- Fuente de alimentación de alto voltaje: Suministra el campo eléctrico necesario para la migración de los analitos y el EOF, generalmente entre 5 y 30 kV.
- Detector: Ubicado cerca del extremo de salida del capilar, registra la llegada de los analitos separados.
- Dispositivo de salida y manejo de datos: Recibe la señal del detector y la convierte en un electroferograma, que muestra la respuesta del detector en función del tiempo, con los compuestos químicos separados apareciendo como picos.
La muestra se introduce en el capilar mediante métodos como la acción capilar, presión, sifonado o electrocinéticamente. La migración de los analitos se inicia al aplicar el campo eléctrico entre los viales de origen y destino.
Métodos de Detección en Electroforesis Capilar
La capacidad de detectar los analitos una vez separados es fundamental en EC. Existen varios métodos de detección, cada uno con sus propias ventajas:
Detección por Absorbancia UV/UV-Vis
Es el modo de detección más común en sistemas comerciales. Una sección del propio capilar se utiliza como celda de detección. Para capilares recubiertos de poliimida, se quema o raspa un segmento del recubrimiento para crear una ventana ópticamente transparente. La longitud de paso de la celda de detección en EC es muy pequeña (aproximadamente 50 micrómetros), lo que afecta la sensibilidad según la ley de Beer-Lambert. Para mejorar la sensibilidad, se puede aumentar la longitud de paso, aunque esto podría reducir la resolución. Se han desarrollado técnicas como las celdas de burbuja o las celdas en 'Z' (tubos adicionales) para lograr esto, triplicando la longitud de paso y mejorando significativamente la sensibilidad.
Detección por Fluorescencia
Se utiliza para muestras que fluorescen naturalmente o que han sido modificadas químicamente con etiquetas fluorescentes. Este método ofrece alta sensibilidad y selectividad. La fluorescencia inducida por láser (LIF) es particularmente sensible, alcanzando límites de detección extremadamente bajos. Los sistemas de detección LIF multicolor son rutinariamente utilizados en secuenciación de ADN y aplicaciones de genotipado.

Acoplamiento con Espectrometría de Masas (MS) y Espectroscopia Raman Realzada en Superficie (SERS)
Para obtener la identidad de los componentes de la muestra, la EC puede acoplarse directamente con un espectrómetro de masas o con SERS. En la mayoría de los sistemas, la salida del capilar se introduce en una fuente de iones que utiliza ionización por electrospray (ESI), y los iones resultantes son analizados por el espectrómetro de masas. Para CE-SERS, los eluyentes de la electroforesis capilar pueden depositarse sobre un sustrato activo SERS, permitiendo la identificación de analitos con alta sensibilidad.
Modos de Separación en Electroforesis Capilar
La separación de compuestos por electroforesis capilar depende de la migración diferencial de los analitos en un campo eléctrico aplicado. Existen seis tipos principales de métodos de electroseparación capilar, que pueden clasificarse en sistemas continuos y discontinuos:
1. Electroforesis Capilar de Zona (CZE)
Es la técnica más utilizada y la más sencilla. La separación se basa en las diferencias en la relación carga-masa de los analitos. Los iones migran en zonas discretas a diferentes velocidades. CZE es útil para separar aniones y cationes, mientras que las especies neutras coeluyen con el EOF. Es ideal para compuestos con carga permanente, como alcaloides cuaternarios y antocianinas.
2. Electroforesis Capilar en Gel (CGE)
Utiliza un gel dentro del capilar, y la separación se basa principalmente en el tamaño del soluto a medida que las partículas migran a través de la matriz del gel. Los geles minimizan la difusión del soluto, previenen la absorción de la pared del capilar y limitan la transferencia de calor. Es ampliamente utilizada para la separación de proteínas (como en SDS-PAGE capilar) y fragmentos de ADN, ofreciendo alta sensibilidad con pequeñas cantidades de muestra.
3. Cromatografía Electrocinética Micelar (MEKC)
Es una técnica híbrida entre electroforesis y cromatografía. Incorpora micelas (agregados de moléculas de tensioactivo) en la solución tampón por encima de la concentración micelar crítica. Las micelas actúan como una fase pseudoestacionaria. Los solutos se separan en función de su coeficiente de reparto entre la fase acuosa y las micelas. Esta técnica es especialmente útil para separar moléculas neutras, que no se separarían por CZE, ya que pueden interactuar con las micelas y, por lo tanto, mostrar diferentes tiempos de migración.
4. Electrofocalización Isoeléctrica Capilar (CIEF)
Es una técnica comúnmente utilizada para separar péptidos y proteínas, que son compuestos zwitteriónicos (con cargas positivas y negativas que dependen del pH). La separación se basa en el punto isoeléctrico (pI) de cada molécula, que es el pH en el que la molécula no tiene carga neta. Durante la CIEF, se establece un gradiente de pH a lo largo del capilar. Cuando se aplica el voltaje, las moléculas migran hasta alcanzar la región donde el pH es igual a su pI, momento en el que se detienen y se "enfocan" en una zona estrecha, permitiendo su detección distintiva.
5. Cromatografía Electroforética Capilar (CEC)
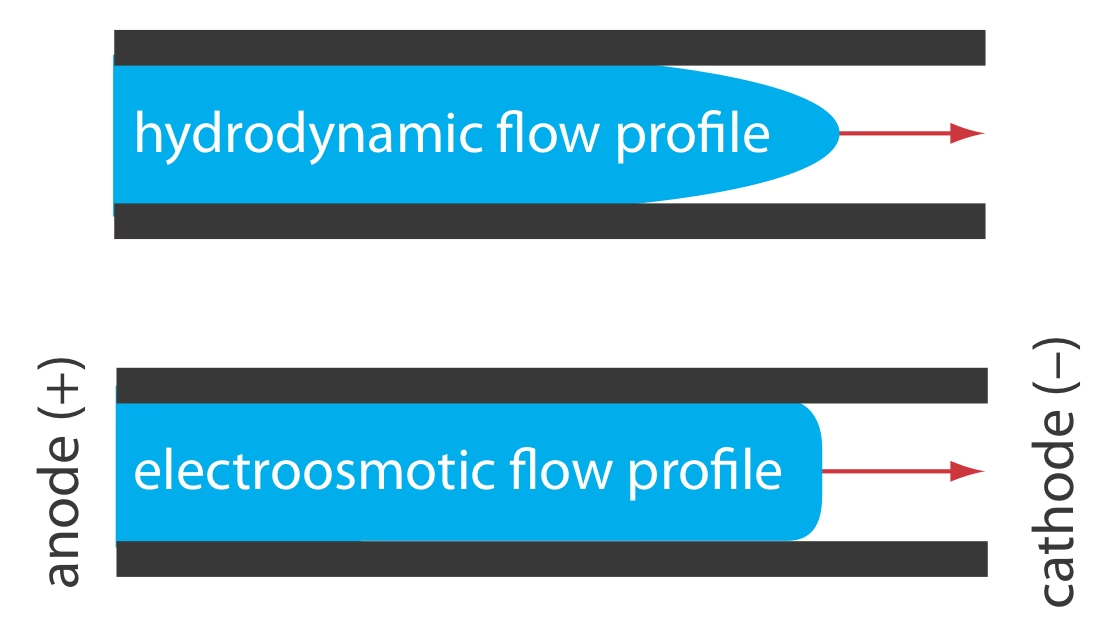
Combina los principios de la cromatografía líquida de alto rendimiento (HPLC) y la electroforesis capilar. En CEC, el capilar está empaquetado con una fase estacionaria similar a la de las columnas cromatográficas. La fase móvil es impulsada por el EOF, lo que proporciona un perfil de flujo tipo "tapón" (plug-flow) que reduce el ensanchamiento de banda, a diferencia del flujo parabólico en HPLC. Esto permite una separación de alta eficiencia basada tanto en interacciones cromatográficas como electroforéticas.
6. Isotacoforesis Capilar (CITP)
Es una técnica de preconcentración y separación en la que los analitos se separan en zonas contiguas, sin espacios entre ellas. Utiliza dos electrolitos diferentes: uno de arrastre (leading electrolyte) y otro de terminación (terminating electrolyte), con diferentes movilidades. Los analitos se mueven entre estos dos electrolitos y se enfocan en zonas estrechas, ordenándose según sus movilidades efectivas. Es muy útil para concentrar analitos diluidos antes de la separación final.
Otros modos avanzados
- Electroforesis Capilar No Acuosa (NACE): Una variante de CZE que utiliza sistemas de tampón no acuosos. Favorece una mayor solubilidad de analitos hidrofóbicos y mejora la selectividad.
- Cromatografía Electrocinética de Microemulsión (MEEKC): Similar a MEKC, pero emplea microemulsiones (gotitas de aceite nanométricas suspendidas en un tampón acuoso) como fase pseudoestacionaria.
Eficiencia y Resolución en Electroforesis Capilar
La eficiencia de separación en EC es excepcionalmente alta, a menudo superando a otras técnicas como la HPLC. Se mide en términos de "platos teóricos". La eficiencia solo está limitada por la difusión y es proporcional a la fuerza del campo eléctrico. Sin embargo, la aplicación de campos eléctricos muy altos puede conducir al calentamiento resistivo (calentamiento Joule) del tampón dentro del capilar. Este calentamiento puede crear gradientes de temperatura radiales, lo que a su vez afecta la movilidad electroforética y disminuye la resolución. La mejor resolución se obtiene generalmente a la máxima fuerza de campo para la cual el calentamiento Joule es insignificante.

A diferencia de la HPLC, en la electroforesis capilar no hay transferencia de masa entre fases en la mayoría de los modos, y el perfil de flujo impulsado por el EOF es plano, no parabólico como el flujo impulsado por presión en las columnas cromatográficas. Como resultado, el EOF no contribuye significativamente al ensanchamiento de banda, lo que permite que las separaciones por EC alcancen varios cientos de miles de platos teóricos, resultando en una resolución excepcional.
Aplicaciones de la Electroforesis Capilar
La versatilidad de la electroforesis capilar la ha convertido en una herramienta indispensable en numerosos campos:
- Análisis Bioquímico y Clínico: Se utiliza para la determinación simultánea de iones (como NH4+, Na+, K+, Mg2+, Ca2+) en fluidos biológicos como la saliva.
- Ciencias Forenses: Es una de las principales aplicaciones, especialmente en el análisis de ADN. Permite la amplificación y detección de fragmentos de ADN mediante PCR, lo que ha revolucionado el tipado de STR (Short Tandem Repeats) para generar perfiles genéticos únicos. También se emplea para la detección de fragmentos de ARNm para identificar el origen de fluidos o tejidos biológicos y en el análisis de tintas de impresión para casos de falsificación de documentos, utilizando MECC.
- Industria Farmacéutica: La electroforesis capilar de afinidad (ACE) es ampliamente utilizada para estudiar interacciones de unión intermoleculares, como las de proteínas-ligandos o fármacos-sistemas vehiculares (micelas). Permite determinar constantes de asociación/unión, ofreciendo resultados rápidos con mínima cantidad de analito. Las variantes basadas en aptámeros son cruciales para el análisis y modificación de reactivos de afinidad específicos.
- Secuenciación de ADN: La EC se ha establecido como un enfoque rentable y de alta precisión para la secuenciación de ADN, permitiendo un alto rendimiento y gran exactitud en la determinación de secuencias de nucleótidos (A, T, C, G).
- Análisis de Fitocompuestos: Es una alternativa valiosa a la cromatografía líquida en la investigación de productos naturales. Ha resuelto con éxito la separación de metabolitos secundarios derivados de plantas como alcaloides (ej., berberina, nuciferina), cumarinas (ej., imperatorina), flavonoides (ej., quercetina), ácidos fenólicos (ej., ácido cafeico, ácido ferúlico) y terpenos.
Preguntas Frecuentes (FAQ)
¿Qué es el flujo electroosmótico (EOF) en electroforesis capilar?
El flujo electroosmótico es el movimiento global del tampón dentro del capilar, impulsado por un campo eléctrico. Se debe a la interacción de los iones de la solución tampón con las cargas fijas en la pared interna del capilar (generalmente grupos silanol ionizados). En el modo normal de EC, el EOF arrastra todos los componentes de la muestra hacia el cátodo, independientemente de su carga.
¿Cómo se separan los analitos en el modo normal de EC si todos se mueven en la misma dirección?
Aunque el EOF arrastra a todos los analitos en la misma dirección, la separación ocurre debido a las diferencias en la movilidad electroforética de cada analito. Los analitos cargados positivamente se mueven más rápido en la dirección del cátodo (sumándose al EOF), mientras que los cargados negativamente se mueven más lento (su movilidad electroforética se opone al EOF). Las especies neutras migran únicamente con la velocidad del EOF.
¿Cuáles son las dimensiones típicas de un capilar utilizado en electroforesis capilar?
Un capilar típico en electroforesis capilar mide entre 25 y 75 cm de longitud, con un diámetro exterior de 300 a 400 micrómetros y un diámetro interior mucho más pequeño, de 25 a 75 micrómetros. Estas dimensiones reducidas son clave para la eficiencia de la técnica al permitir una disipación de calor superior.
¿Se pueden separar moléculas neutras con electroforesis capilar?
Sí, aunque las moléculas neutras no tienen movilidad electroforética y, por lo tanto, no se separan por CZE (migran con el EOF como una sola banda), se pueden separar utilizando modos como la Cromatografía Electrocinética Micelar (MEKC). En MEKC, las moléculas neutras interactúan de manera diferencial con las micelas presentes en la solución tampón, lo que permite su separación.
¿Qué ventajas ofrece la electroforesis capilar frente a otras técnicas de separación como la HPLC?
La EC ofrece varias ventajas significativas, incluyendo una eficiencia de separación mucho mayor (mayor número de platos teóricos), tiempos de análisis más rápidos, un consumo de muestra significativamente menor (nanolitros), y la capacidad de acoplarse fácilmente con detectores de alta sensibilidad como la espectrometría de masas. Además, el perfil de flujo tipo "tapón" del EOF reduce el ensanchamiento de banda, contribuyendo a una resolución superior.
En resumen, la electroforesis capilar es una técnica analítica de vanguardia que, gracias a su modo normal de funcionamiento basado en el flujo electroosmótico y la movilidad electroforética, su instrumentación optimizada, sus diversos métodos de detección y sus múltiples modos de separación, ha consolidado su posición como una herramienta indispensable en el análisis químico y biológico moderno. Su alta eficiencia y versatilidad continúan impulsando avances significativos en la investigación y el desarrollo en una multitud de disciplinas científicas.
Si quieres conocer otros artículos parecidos a Electroforesis Capilar: Principios y Aplicaciones puedes visitar la categoría Cabello.

