01/01/2020
¿Alguna vez te has preguntado cómo algunos insectos logran deslizarse sobre el agua sin hundirse, o por qué las gotas de rocío adoptan una forma casi perfectamente esférica? Estos son solo dos ejemplos cotidianos de fenómenos gobernados por la tensión superficial y la capilaridad, dos propiedades fundamentales de los líquidos que, aunque invisibles a simple vista, tienen un impacto profundo en nuestro mundo. Desde la forma en que el agua se comporta en la naturaleza hasta procesos industriales y biológicos, comprender estas fuerzas nos permite desentrañar muchos de los misterios que nos rodean.

En este artículo, exploraremos en detalle qué son la tensión superficial y la capilaridad, cómo se originan a nivel molecular y cuáles son sus múltiples manifestaciones. Abordaremos sus causas, las propiedades que las definen, los diversos efectos que producen y los métodos utilizados para medirlas, incluso considerando cómo factores como la temperatura y la concentración de solutos pueden modificarlas. Prepárate para sumergirte en el fascinante comportamiento de los líquidos.
- ¿Qué es la Tensión Superficial?
- Efectos Comunes de la Tensión Superficial
- La Capilaridad: Un Vínculo con la Tensión Superficial
- Métodos de Medición de la Tensión Superficial
- Consideraciones Termodinámicas
- Tensión Superficial del Agua y del Agua de Mar
- Preguntas Frecuentes sobre Tensión Superficial y Capilaridad
- 1. ¿Por qué el agua tiene una tensión superficial tan alta comparada con otros líquidos?
- 2. ¿Cómo permite la tensión superficial que los insectos caminen sobre el agua?
- 3. ¿Qué es el menisco y por qué es cóncavo o convexo?
- 4. ¿Cuál es la importancia de la capilaridad en la naturaleza y la tecnología?
- 5. ¿Qué papel juegan los surfactantes en la tensión superficial?
- Conclusión
¿Qué es la Tensión Superficial?
La tensión superficial de un líquido puede entenderse de dos maneras principales, ambas interconectadas. La primera la define como la cantidad de energía necesaria para aumentar su superficie por unidad de área. Esta definición implica que el líquido se resiste a expandir su superficie, lo que explica por qué objetos ligeros, como una aguja de acero cuidadosamente colocada, pueden "flotar" sobre el agua sin hundirse, o por qué algunos insectos pueden desplazarse sobre ella. Es una manifestación directa de las fuerzas intermoleculares dentro del líquido.
La segunda definición, igualmente válida, describe la tensión superficial como la fuerza que actúa tangencialmente por unidad de longitud en el borde de una superficie libre de un líquido en equilibrio, tendiendo a contraer dicha superficie. En las interfases líquido-aire, esta tensión es el resultado de una mayor atracción entre las moléculas del líquido (cohesión) que entre las moléculas del líquido y las del aire (adhesión). Es como si la superficie del líquido estuviera cubierta por una membrana elástica estirada, aunque esta analogía tiene sus límites, ya que la tensión superficial es una propiedad inherente de la interfaz, no dependiente de la deformación como una membrana elástica.
Causas de la Tensión Superficial
La razón fundamental de la tensión superficial reside en la diferencia de fuerzas que experimentan las moléculas en el interior de un líquido y las que se encuentran en su superficie. En el seno del líquido, cada molécula está rodeada por otras moléculas en todas direcciones, lo que resulta en fuerzas de atracción que, en promedio, se anulan. Esto permite que la molécula tenga una energía relativamente baja.
Sin embargo, en la superficie, las moléculas tienen menos "vecinas" con las que interactuar hacia el exterior (hacia el gas o el aire), lo que genera una fuerza neta hacia el interior del líquido. Energéticamente, las moléculas de la superficie tienen una energía promedio más alta que las del interior. Para que el sistema líquido disminuya su energía total, busca minimizar el número de moléculas en su superficie, lo que se traduce en una reducción del área superficial hasta el mínimo posible. Por esta razón, una gota de líquido libre adopta una forma esférica, ya que una esfera es la forma geométrica que minimiza la relación entre área superficial y volumen.
Propiedades y Factores Influyentes
La tensión superficial (representada comúnmente por γ) posee varias propiedades clave:
- Representa el trabajo necesario para llevar una molécula del interior a la superficie.
- Es la responsable de fenómenos como el menisco y la capilaridad, debido al equilibrio entre fuerzas cohesivas (dentro del líquido) y adhesivas (líquido-superficie).
- Su valor varía significativamente entre diferentes líquidos. Por ejemplo, el agua tiene una tensión superficial relativamente alta (72,8 mN/m a 20 °C) debido a sus fuertes enlaces de hidrógeno, mientras que líquidos como el hexano o el éter tienen valores mucho menores. El mercurio, con su enlace metálico, presenta una tensión superficial excepcionalmente alta.
- Disminuye con el aumento de la temperatura. A medida que la temperatura sube, la agitación térmica de las moléculas aumenta, debilitando la intensidad efectiva de las fuerzas intermoleculares. La tensión superficial llega a cero en la temperatura crítica (Tc) del compuesto, donde el líquido y el vapor se vuelven indistinguibles.
Existen ecuaciones empíricas que describen la relación entre la tensión superficial y la temperatura, como la ecuación de Eötvös y la de Guggenheim-Katayama, que reflejan esta dependencia y la convergencia a cero en la temperatura crítica.
Influencia de la Concentración de Soluto
Los solutos pueden afectar la tensión superficial de diversas maneras, dependiendo de su naturaleza y la del solvente:
- Poco o ningún efecto: Como el azúcar en agua.
- Incremento: Muchas sales inorgánicas en agua.
- Decremento progresivo: Sustancias anfífilas, como los alcoholes en agua, que tienden a acumularse en la superficie.
- Decremento hasta una concentración crítica: Los surfactantes, que reducen drásticamente la tensión superficial y son cruciales para la formación de burbujas estables y emulsiones.
La isoterma de Gibbs describe cómo la concentración de un soluto en la superficie puede diferir de su concentración en el volumen del líquido, lo que influye directamente en la tensión superficial.
Efectos Comunes de la Tensión Superficial
La tensión superficial se manifiesta en una miríada de fenómenos, algunos de los cuales son sorprendentemente cotidianos:
Formación de Gotas
Las gotas de lluvia sobre una superficie cerosa (como las hojas) adoptan una forma casi esférica. Esto se debe a que el agua se adhiere débilmente a la cera pero fuertemente a sí misma, y la tensión superficial minimiza el área, haciendo que se agrupe en esferas, la forma con la menor relación área superficial a volumen. De manera similar, un chorro de agua que cae de un grifo se rompe en gotas esféricas debido a que la gravedad alarga el chorro y la tensión superficial lo pellizca para reducir su área.
Flotación de Objetos
Objetos más densos que el agua, como una aguja de acero o pequeños insectos como los zapateros de agua (Gerridae), pueden flotar sobre la superficie. Esto ocurre cuando el objeto no es mojable (es decir, el líquido no se adhiere a él) y su peso es lo suficientemente pequeño como para ser soportado por las fuerzas de tensión superficial. La superficie del agua se deforma ligeramente, aumentando su área y generando una fuerza hacia arriba que contrarresta el peso del objeto.
La fuerza que soporta un objeto flotante puede expresarse matemáticamente:
Fuerza de Peso (Fw) = 2 * Fuerza por Superficie (Fs) * sen(θ) Donde Fw = m * g (masa x gravedad) Fs = γ * L (tensión superficial x longitud de contacto)
Así, la masa que puede ser soportada es: mg = 2γL sen(θ). Esto demuestra que la superficie del agua actúa como una membrana elástica que se resiste a ser penetrada.
Separación de Líquidos
La separación de aceite y agua, o la formación de las "lágrimas de vino", son ejemplos de tensión interfacial, un tipo de tensión superficial que ocurre en la interfaz entre dos líquidos diferentes. En el caso del vino, es una compleja interacción entre las diferentes tensiones superficiales del agua y el etanol, exacerbada por la evaporación diferencial.
El Papel de los Surfactantes
Los surfactantes (agentes tensoactivos) son sustancias que reducen drásticamente la tensión superficial de un líquido. Son esenciales para la estabilidad de las burbujas de jabón, que tienen una enorme área superficial con muy poca masa. En agua pura, las burbujas son inestables, pero la adición de surfactantes las estabiliza (fenómeno conocido como efecto Marangoni). De manera similar, los surfactantes permiten la estabilidad de las emulsiones, como las diminutas gotas de aceite suspendidas en agua, al reducir la tensión interfacial y evitar que se fusionen.
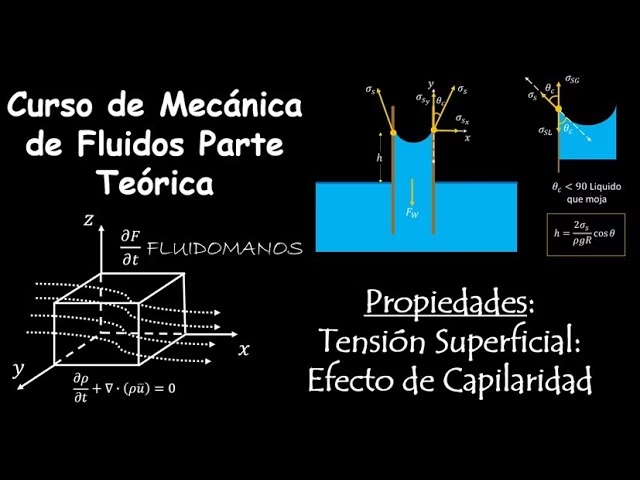
La Capilaridad: Un Vínculo con la Tensión Superficial
La capilaridad es otro fenómeno crucial directamente relacionado con la tensión superficial y las fuerzas intermoleculares entre el líquido y una superficie sólida. Es la capacidad de un líquido para ascender o descender por un tubo capilar (un tubo muy estrecho) o por un material poroso.
Líquido en Tubo Vertical (Menisco)
Cuando un líquido está en contacto con las paredes de un recipiente, su superficie puede curvarse. Esta curvatura se conoce como menisco. Si el líquido se adhiere a las paredes (es decir, las fuerzas de adhesión entre el líquido y el sólido son mayores que las fuerzas cohesivas dentro del líquido), el menisco será cóncavo (curvado hacia arriba), como el agua en un tubo de vidrio. El líquido "sube" por las paredes para maximizar el contacto con el sólido, reduciendo la energía potencial total del sistema.
Por el contrario, si el líquido no se adhiere a las paredes o las repele (fuerzas cohesivas mayores que adhesivas), el menisco será convexo (curvado hacia abajo), como el mercurio en un tubo de vidrio. En este caso, el líquido intenta minimizar el contacto con las paredes, y su superficie se deprime en el centro.
Si un tubo es lo suficientemente estrecho y la adhesión del líquido a sus paredes es fuerte, la tensión superficial puede hacer que el líquido ascienda por el tubo, un fenómeno conocido como acción capilar. La altura (h) a la que asciende la columna de líquido se rige por la Ley de Jurin:
h = (2γla cos θ) / (ρ g r)
Donde γla es la tensión superficial entre el líquido y el aire, θ es el ángulo de contacto, ρ es la densidad del líquido, g es la aceleración de la gravedad y r es el radio del capilar. Si el ángulo de contacto (θ) es mayor de 90° (como el mercurio en vidrio), el líquido será deprimido en lugar de elevado.
Charcos en una Superficie
La tensión superficial también influye en la forma de los charcos. Si viertes mercurio sobre una superficie plana de vidrio, formará un charco con un espesor perceptible, que no se extenderá indefinidamente. Esto se debe a la alta tensión superficial del mercurio, que tiende a minimizar su área de contacto con el vidrio. El resultado es un charco relativamente grueso y compacto. De manera similar, el agua sobre una superficie encerada (a la que no se adhiere) se comportará de forma parecida al mercurio en vidrio, formando gotas o charcos más altos.
Rotura de Chorros en Gotas
Un chorro de líquido que sale de una boquilla, sin importar cuán suave sea, eventualmente se romperá en gotas. Este fenómeno se conoce como Instabilidad de Plateau-Rayleigh y es una consecuencia directa de la tensión superficial. Pequeñas perturbaciones en el chorro crecen con el tiempo, y la tensión superficial actúa para pellizcar el chorro, minimizando su área superficial y dividiéndolo en esferas individuales.
Métodos de Medición de la Tensión Superficial
Dada su importancia, existen numerosos métodos para medir la tensión superficial, cada uno adecuado para diferentes condiciones y tipos de líquidos. Un instrumento utilizado para medir la tensión superficial se denomina tensiómetro.
| Método | Descripción Breve | Ventajas / Aplicaciones |
|---|---|---|
| Anillo de du Noüy | Mide la fuerza máxima necesaria para levantar un anillo de platino de la superficie del líquido. | Tradicional, poco influenciado por las propiedades de mojado. |
| Platillo de Wilhelmy | Un platillo vertical se sumerge en el líquido y se mide la fuerza de mojado. | Universal, apto para mediciones a largo plazo y superficies dinámicas. |
| Gota Rotante | Se mide el diámetro de una gota de un líquido suspendida en otro, mientras ambos rotan. | Ideal para tensiones interfaciales muy bajas. |
| Gota Colgante | Se analiza ópticamente la geometría de una gota que cuelga de una jeringa. | Permite mediciones a altas temperaturas y presiones. |
| Presión de Burbuja (Jaeger) | Se mide la presión máxima requerida para formar una burbuja en la punta de un capilar sumergido. | Útil para determinar la tensión superficial a edades superficiales cortas (dinámica). |
| Volumen de Gota | Se bombea un líquido en otro de diferente densidad y se mide el tiempo entre la formación de gotas. | Determina la tensión interfacial en función de la edad interfacial. |
| Elevación Capilar | Se mide la altura a la que un líquido asciende dentro de un tubo capilar. | Simple, se relaciona directamente con la Ley de Jurin. |
| Estalagmómetro | Mide el peso o el número de gotas que se forman y caen de un capilar. | Método de ponderación y lectura directa de gotas. |
| Gota Fija (Sessile Drop) | Se deposita una gota sobre un sustrato y se mide su ángulo de contacto. | Determina tensión superficial y densidad, útil para mojabilidad. |
| Du Noüy-Padday | Versión miniaturizada del método de Du Noüy, usando una aguja fina y micro-balanza. | Para volúmenes de muestra muy pequeños y mediciones rápidas. |
| Frecuencia Vibracional de Gotas Levitadas | Se utiliza la frecuencia natural de oscilaciones de gotas levitadas magnéticamente. | Aplicado a superfluidos, como el Helio II. |
| Rebote de Gota | Basado en la deformación y oscilación de una gota que rebota tras caer desde una levitación aerodinámica. | Mide tensión superficial y viscosidad simultáneamente. |
| Por Teléfono Inteligente | Mide la longitud de onda de ondas capilares excitadas por el vibro-motor del teléfono y capturadas por la cámara. | Método accesible y moderno. |
Consideraciones Termodinámicas
Desde una perspectiva termodinámica, la tensión superficial está intrínsecamente ligada a la energía libre de la superficie de un sistema. J. W. Gibbs desarrolló una teoría basada en la idea de superficies de discontinuidad, donde la energía libre de superficie (Ωs) es proporcional al área superficial (A), es decir, Ωs = γA. Esto implica que para aumentar el área superficial de un líquido, se debe añadir una cierta cantidad de energía. Los sistemas mecánicos tienden a minimizar su energía potencial, y en el caso de los líquidos, esto se logra minimizando su área superficial.
La famosa Ecuación de Young-Laplace, Δp = γ (1/Rx + 1/Ry), describe cómo la curvatura de una superficie líquida se relaciona con la diferencia de presión a través de ella y la tensión superficial. Esta ecuación es fundamental para entender la forma de las gotas, burbujas y meniscos.
Tensión Superficial del Agua y del Agua de Mar
El agua, el líquido más abundante en la Tierra, tiene una tensión superficial particularmente alta debido a sus enlaces de hidrógeno. La International Association for the Properties of Water and Steam (IAPWS) ha establecido correlaciones precisas para la tensión superficial del agua pura en contacto con su vapor. Por ejemplo, a 25 °C, la tensión superficial del agua es de aproximadamente 71.97 mN/m.
Para el agua de mar, la tensión superficial es ligeramente diferente debido a la presencia de sales. Nayar et al. publicaron datos de referencia que muestran cómo la salinidad y la temperatura influyen en este valor. La IAPWS ha adoptado una correlación para el agua de mar que tiene en cuenta estos factores, demostrando que la salinidad generalmente aumenta la tensión superficial del agua.
Datos Tabulados de Tensión Superficial
A continuación, se presenta una tabla con la tensión superficial de varios líquidos en contacto con el aire, a diferentes temperaturas. Las unidades son dinas/cm, que son equivalentes a mN/m (milinewtons por metro).
| Líquido | Temperatura (°C) | Tensión Superficial (mN/m) |
|---|---|---|
| Ácido acético | 20 | 27.60 |
| Ácido acético (45.1%) + agua | 30 | 40.68 |
| Ácido acético (10.0%) + agua | 30 | 54.56 |
| Acetona | 20 | 23.70 |
| Sangre | 22 | 55.89 |
| Dietil éter | 20 | 17.00 |
| Etanol | 20 | 22.27 |
| Etanol (40%) + agua | 25 | 29.63 |
| Etanol (11.1%) + agua | 25 | 46.03 |
| Glicerol | 20 | 63.00 |
| n-Hexano | 20 | 18.40 |
| Ácido hidroclórico 17.7 M solución acuosa | 20 | 65.95 |
| Isopropanol | 20 | 21.70 |
| Helio II líquido | -273 | 0.37 |
| Nitrógeno líquido | -196 | 8.85 |
| Oxígeno líquido | -182 | 13.2 |
| Mercurio | 15 | 487.00 |
| Metanol | 20 | 22.60 |
| Cloruro de plata derretido | 650 | 163 |
| Cloruro de sodio / Cloruro de calcio derretidos (47 / 53 mol %) | 650 | 139 |
| n-Octano | 20 | 21.80 |
| Cloruro de sodio 6.0 M solución acuosa | 20 | 82.55 |
| Sacarosa (55%) + agua | 20 | 76.45 |
| Agua | 0 | 75.64 |
| Agua | 25 | 71.97 |
| Agua | 50 | 67.91 |
| Agua | 100 | 58.85 |
| Tolueno | 25 | 27.73 |
| Benceno | 28.85 | |
| Tetracloruro de Carbono | 26.95 | |
| Acetato de etilo | 23.9 | |
| Éter etílico | 17.01 |
Preguntas Frecuentes sobre Tensión Superficial y Capilaridad
1. ¿Por qué el agua tiene una tensión superficial tan alta comparada con otros líquidos?
El agua posee una tensión superficial excepcionalmente alta debido a la presencia de fuertes enlaces de hidrógeno entre sus moléculas. Estos enlaces crean una cohesión intermolecular muy potente, lo que significa que las moléculas de agua se atraen fuertemente entre sí, resistiendo la expansión de su superficie más que otros líquidos con fuerzas intermoleculares más débiles (como las fuerzas de Van der Waals).
2. ¿Cómo permite la tensión superficial que los insectos caminen sobre el agua?
Los insectos como los zapateros de agua tienen patas hidrofóbicas (no mojables), lo que significa que el agua no se adhiere a ellas. Cuando el insecto ejerce una ligera presión sobre el agua, la tensión superficial del agua se deforma pero resiste romperse, creando una fuerza hacia arriba que contrarresta el peso del insecto. La superficie del agua actúa como una "membrana elástica" que soporta el peso.
3. ¿Qué es el menisco y por qué es cóncavo o convexo?
El menisco es la curvatura que adopta la superficie de un líquido en un recipiente o tubo capilar. Es cóncavo (curvado hacia arriba) cuando las fuerzas de adhesión entre el líquido y el material del recipiente son mayores que las fuerzas de cohesión dentro del líquido (ej. agua en vidrio). Es convexo (curvado hacia abajo) cuando las fuerzas de cohesión del líquido son mayores que las de adhesión con el recipiente (ej. mercurio en vidrio). La forma del menisco busca minimizar la energía total del sistema.
4. ¿Cuál es la importancia de la capilaridad en la naturaleza y la tecnología?
La capilaridad es vital en muchos procesos. En la naturaleza, permite que las plantas absorban agua y nutrientes del suelo a través de sus raíces y tallos, ascendiendo contra la gravedad. En la tecnología, es fundamental en la absorción de líquidos por materiales porosos (como papel o esponjas), en la fabricación de dispositivos microfluídicos, en la impresión de tinta y en la lubricación, entre otras aplicaciones.
5. ¿Qué papel juegan los surfactantes en la tensión superficial?
Los surfactantes son sustancias que reducen significativamente la tensión superficial de un líquido. Lo hacen interponiéndose entre las moléculas del líquido en la superficie, debilitando las fuerzas de cohesión. Esta propiedad es crucial en la formulación de detergentes (para que el agua "moje" mejor la suciedad), en la estabilización de emulsiones (mezclas de líquidos inmiscibles como mayonesa) y en la formación de espumas y burbujas estables.
Conclusión
La tensión superficial y la capilaridad son mucho más que conceptos físicos abstractos; son fuerzas omnipresentes que dan forma a nuestro mundo. Desde la delicada danza de los insectos sobre el agua hasta la vital absorción de nutrientes en las plantas, y desde la estabilidad de las burbujas de jabón hasta la precisión de los dispositivos microfluídicos, estas propiedades de los líquidos son esenciales para la vida y la tecnología. Comprender cómo las fuerzas intermoleculares se manifiestan en la superficie de los líquidos nos permite apreciar la complejidad y la elegancia del universo que nos rodea, revelando que incluso los fenómenos más simples esconden una profunda ciencia.
Si quieres conocer otros artículos parecidos a El Secreto de la Superficie: Tensión y Capilaridad puedes visitar la categoría Cabello.