25/11/2013
La proliferación de células endoteliales es un proceso fundamental en la biología de nuestro cuerpo, esencial para la formación de nuevos vasos sanguíneos, un fenómeno conocido como angiogénesis. Este intrincado proceso es vital para el desarrollo, la curación de heridas e incluso en la progresión de diversas enfermedades. Lejos de ser un evento simple, la multiplicación de estas células, que recubren el interior de nuestros vasos, está finamente regulada por una compleja red de señales que involucran tanto a su entorno físico, la matriz extracelular, como a mensajeros químicos, los factores de crecimiento. Comprender estos mecanismos nos permite vislumbrar la asombrosa precisión con la que nuestro organismo mantiene su equilibrio y reacciona ante los desafíos.
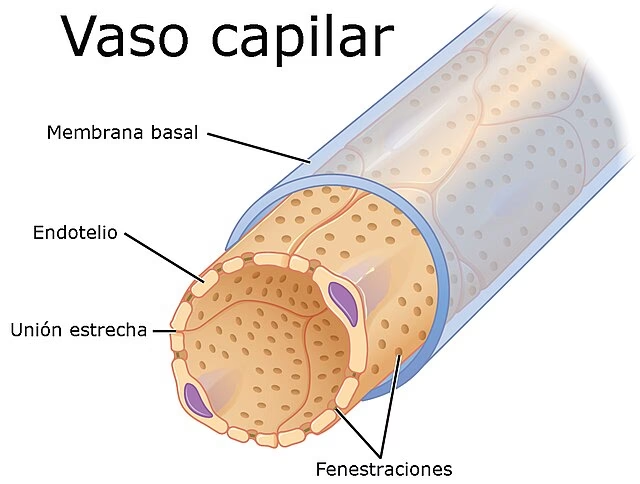
La capacidad de las células para proliferar no es intrínseca, sino que depende en gran medida de su interacción con el entorno que las rodea. Un componente crucial de este entorno es la matriz extracelular (MEC), una compleja red de proteínas y otras moléculas que proporciona soporte estructural y bioquímico a los tejidos. La interacción entre las células y la MEC se produce a través de receptores específicos en la superficie celular, como las integrinas. Estas interacciones son fundamentales para la supervivencia y el crecimiento celular, a menudo trabajando en conjunto con factores de crecimiento o receptores de citocinas.
El Papel Crucial de la Matriz Extracelular y los Receptores
Un concepto clave en la proliferación celular es la dependencia de anclaje, que establece que las células requieren estar adheridas a un sustrato para poder entrar en la fase S del ciclo celular, es decir, la fase de síntesis de ADN. Incluso en presencia de factores de crecimiento, las células no avanzarán en su ciclo de división si no están ancladas. Esta dependencia subraya la importancia de la MEC como plataforma para el crecimiento celular.
Además de promover la proliferación, la adhesión de las células a las moléculas de la MEC juega un papel muy importante en la regulación de su supervivencia. La pérdida de adhesión celular a la matriz a menudo desencadena un proceso de apoptosis, o muerte celular programada, conocido como anoikis. Este mecanismo es una forma de control de calidad, eliminando células que se han desprendido de su ubicación adecuada. La pérdida de la adhesión mediada por integrinas puede inducir la translocación de proteínas pro-apoptóticas como Bax hacia las mitocondrias, promoviendo así la muerte celular. Sin embargo, la activación de la proteína FAK (quinasa de adhesión focal) puede prevenir la anoikis y promover la supervivencia en células como fibroblastos y células epiteliales, a través de vías de señalización complejas que pueden variar según el tipo celular.
Las integrinas no solo previenen la anoikis, sino que también promueven la proliferación celular a través de múltiples vías de señalización. Muchas de estas vías implican la activación de las cascadas de las quinasas activadas por mitógenos (MAPK). Numerosos estudios demuestran que la señalización de las integrinas es fundamental para la proliferación celular. Por ejemplo, la deficiencia de la integrina α1β1, un receptor primario de colágeno, ha demostrado reducir la proliferación de fibroblastos. De manera similar, la sobreexpresión de una subunidad de integrina β1 dominante-negativa en células epiteliales mamarias resulta en una proliferación reducida.
Las interacciones integrina-MEC pueden activar la proteína Rac1 a través de la vía FAK/Src/p130CAS/DOCK180, lo que a su vez induce la activación de JNK, estimulando la expresión de ciclina D y la división celular. Otras MAP quinasas, como ERK1/2, también pueden activarse mediante la unión de integrinas. Esta activación conduce a la fosforilación de factores de transcripción y a la expresión de genes de respuesta temprana involucrados en la progresión del ciclo celular. La señalización posterior a la unión célula-MEC también facilita la degradación de inhibidores del ciclo celular, impulsando aún más la proliferación.
La Sinergia entre Integrinas y Factores de Crecimiento
La proliferación celular es a menudo un esfuerzo cooperativo. La unión integrina-MEC trabaja de la mano con la señalización de los receptores de factores de crecimiento para estimular la proliferación celular. Factores de crecimiento individuales pueden requerir interacciones específicas integrina-matriz para mediar la señalización posterior. Por ejemplo, la angiogénesis inducida por bFGF requiere la integrina αvβ3, mientras que la inducida por VEGF requiere la αvβ5.
Las integrinas y los factores de crecimiento pueden aumentar la activación de quinasas de fosfatidilinositol fosfato, elevando los niveles de PIP2. El PIP2 sirve entonces como sustrato para la fosfolipasa Cγ (PLCγ), que es activada tanto por factores de crecimiento como por la unión de integrinas, llevando finalmente a la activación de la proteína quinasa C (PKC) y promoviendo la proliferación celular. La adhesión celular a la fibronectina, por ejemplo, puede inducir la autofosforilación y activación del Receptor del Factor de Crecimiento Epidérmico (EGFR), un paso crítico en la proliferación.
Existen múltiples mecanismos que interconectan la adhesión célula-matriz y la señalización del receptor del factor de crecimiento. Estos incluyen la interacción directa entre integrinas y factores de crecimiento o sus receptores, la regulación alterada de los receptores de integrinas o factores de crecimiento, y la unión de la matriz a los factores de crecimiento o sus receptores. Por ejemplo, el VEGF puede unirse directamente a la integrina α9β1, y tanto esta integrina como VEGFR2 son necesarios para la fosforilación posterior de paxilina y ERK, lo que sugiere un papel crucial en la proliferación inducida por VEGF. Otros factores de crecimiento como IGF-1 y FGF-2 también interactúan con la integrina αvβ3.
Además, algunos receptores de factores de crecimiento, como PDGFRβ y VEGFR2, interactúan físicamente con subunidades de integrinas, y la adhesión celular mediada por integrinas aumenta aún más la activación del receptor y la mitogenicidad. La interacción de VEGFR2 con integrinas participa en la inducción de VEGF de la vía Ras/ERK en células endoteliales. El EGFR también interactúa con integrinas después de la adhesión celular a la matriz, formando un complejo que promueve la fosforilación del EGFR.
Finalmente, muchas moléculas de la MEC pueden unirse a factores de crecimiento o a sus receptores para regular su actividad. Por ejemplo, el IGF-1 interactúa con la vitronectina, promoviendo su señalización a través del IGFR. La fibronectina y la vitronectina también se unen a HGF, promoviendo la formación de complejos integrina-receptor de HGF (Met) y aumentando la proliferación celular. El VEGF también se une a la fibronectina, aumentando significativamente su capacidad para estimular la activación de VEGFR2 y Erk en células endoteliales. Los proteoglicanos de sulfato de heparán son otro ejemplo, ya que pueden secuestrar factores de crecimiento como FGF-2, FGF-10, PDGF, VEGF e IL-2 dentro de la matriz o presentarlos a sus receptores, facilitando la activación del receptor y la proliferación celular.
Factores que Impulsan la Proliferación: El Rol de VEGF y HDAC7
El VEGF (Factor de Crecimiento Endotelial Vascular) es un regulador clave de la proliferación y migración de las células endoteliales. Su acción es fundamental en la angiogénesis, el proceso de formación de nuevos vasos sanguíneos, que es crítico para el desarrollo vascular normal y en la patogénesis de numerosas enfermedades vasculares. La sensibilidad de las células endoteliales a la señalización del VEGF es tan elevada que incluso la alteración de un solo alelo de VEGF en ratones puede resultar en anomalías vasculares letales.
La unión del VEGF a sus receptores induce la dimerización del receptor y la autofosforilación, lo que activa varias quinasas posteriores, incluyendo la proteína quinasa C y D (PKC y PKD), la fosfatidilinositol 3-quinasa (PI3K) y la MAPK. Esta compleja cascada de señalización lleva a la activación de numerosos genes que median las respuestas biológicas al VEGF. Sin embargo, los mecanismos nucleares exactos por los que el VEGF regula la transcripción génica y la angiogénesis no siempre están completamente definidos.
Aquí es donde entran en juego las histonas acetiltransferasas y las histonas desacetilasas (HDACs), que son reguladores clave de la estructura de la cromatina y la expresión génica. Las HDACs de clase IIa (HDAC4, -5, -7 y -9) son particularmente interesantes, ya que contienen una extensión N-terminal que interactúa con otros cofactores transcripcionales y confiere sensibilidad a las señales extracelulares. La fosforilación de una serie de residuos de serina conservados en el dominio regulador N-terminal de las HDACs de clase IIa por quinasas como CaMK y PKD, crea sitios de acoplamiento para proteínas chaperonas 14-3-3, lo que impulsa a estas HDACs del núcleo al citoplasma y desreprime la expresión génica.
Mecanismos Moleculares Detrás de la Activación de HDAC7
Estudios recientes han revelado que el VEGF induce la fosforilación de tres residuos de serina conservados en la histona desacetilasa 7 (HDAC7) a través de la proteína quinasa D (PKD). Esta fosforilación promueve la exportación nuclear de HDAC7 y la activación de genes que responden al VEGF en las células endoteliales. La expresión de una proteína mutante de HDAC7 resistente a la señalización (HDAC7-S/A) en células endoteliales inhibe la proliferación y migración en respuesta al VEGF, lo que demuestra que la fosforilación de HDAC7 actúa como un interruptor molecular clave para mediar la señalización del VEGF y la función endotelial.
El VEGF-A induce robustamente la fosforilación de HDAC7 en los tres residuos de serina (Ser-178, Ser-344 y Ser-479). Esta fosforilación es rápida, alcanzando su punto máximo entre los 5 y 10 minutos después del tratamiento con VEGF. La fosforilación de HDAC7 se acompaña de su unión a la proteína 14-3-3, lo que es esencial para su exportación del núcleo al citoplasma. Consistentemente, la HDAC7, que se localiza exclusivamente en el núcleo en condiciones de reposo, se exporta al citoplasma tras el tratamiento con VEGF, un proceso que es dinámico y reversible.
La vía PKC/PKD ha demostrado ser necesaria y suficiente para la fosforilación de HDAC7 inducida por VEGF. Inhibidores de PKC y PKD, como Gö6983 y Gö6976, bloquean la fosforilación de HDAC7 inducida por VEGF. Además, la supresión de PKD1 mediante ARN de interferencia (siRNA) reprime la fosforilación de HDAC7 en las células endoteliales. Por otro lado, una PKD constitutivamente activa (PKD-CA) es suficiente para inducir la fosforilación y exportación nuclear de HDAC7, incluso en ausencia de VEGF. Esto subraya el papel central de la PKD en esta vía de señalización.
Implicaciones Funcionales: Proliferación y Migración Celular
La importancia funcional de la fosforilación de HDAC7 inducida por VEGF es evidente en la proliferación y migración de las células endoteliales. La sobreexpresión de la mutante HDAC7-S/A, que es resistente a la fosforilación, atenúa significativamente la proliferación celular en respuesta al VEGF. De manera similar, la sobreexpresión de HDAC7-S/A reprime la migración de las células endoteliales inducida por VEGF en ensayos de herida por raspado.
Estos resultados demuestran que los sitios de fosforilación en HDAC7 que responden al VEGF son críticos para la proliferación y migración endotelial inducidas por este factor de crecimiento. El fracaso de la HDAC7 en ser fosforilada por VEGF impone un bloqueo a la migración celular, lo que sugiere que genes clave necesarios para la migración son reprimidos de manera irreversible por la mutante HDAC7 resistente a la señalización. En resumen, la HDAC7 actúa como un interruptor molecular dependiente de VEGF que gobierna funciones esenciales de las células endoteliales, como su capacidad de dividirse y moverse, procesos fundamentales en la formación y reparación de los vasos sanguíneos.
Preguntas Frecuentes (FAQs)
- ¿Qué es la angiogénesis?
- La angiogénesis es el proceso fisiológico de formación de nuevos vasos sanguíneos a partir de vasos preexistentes. Es crucial para el desarrollo embrionario, la cicatrización de heridas y la respuesta a la isquemia (falta de oxígeno).
- ¿Por qué es importante la 'dependencia de anclaje' para las células endoteliales?
- La dependencia de anclaje significa que las células endoteliales (y muchas otras) necesitan estar adheridas a un sustrato (como la matriz extracelular) para poder dividirse y proliferar. Sin esta adhesión, no pueden avanzar en su ciclo celular.
- ¿Qué es la anoikis?
- La anoikis es una forma de apoptosis (muerte celular programada) que ocurre cuando las células pierden su adhesión a la matriz extracelular. Es un mecanismo de control para asegurar que las células permanezcan en su ubicación adecuada.
- ¿Cómo afecta el VEGF a las células endoteliales?
- El VEGF (Factor de Crecimiento Endotelial Vascular) es un factor de crecimiento clave que estimula la proliferación, migración y supervivencia de las células endoteliales, promoviendo así la formación de nuevos vasos sanguíneos (angiogénesis).
- ¿Qué es HDAC7 y por qué es importante en la proliferación endotelial?
- HDAC7 es una histona desacetilasa que regula la expresión génica. En las células endoteliales, su fosforilación por la vía del VEGF/PKD es esencial para su exportación del núcleo al citoplasma, lo que desreprime genes necesarios para la proliferación y migración de estas células. Sin esta fosforilación, la proliferación y migración se ven afectadas.
Si quieres conocer otros artículos parecidos a La Proliferación de Células Endoteliales: Claves Biológicas puedes visitar la categoría Cabello.