21/05/2021
La electroforesis es una de las técnicas más fundamentales y poderosas en el campo de la bioquímica, la biología molecular y la química analítica. Su principio básico radica en la separación de moléculas cargadas (como proteínas, ácidos nucleicos, o incluso iones pequeños) bajo la influencia de un campo eléctrico. Las moléculas se mueven a través de una matriz o un medio líquido, y su velocidad de migración depende de su carga, tamaño y forma. Esta capacidad de separar y analizar componentes complejos de una muestra ha transformado nuestra comprensión de los sistemas biológicos y ha impulsado avances significativos en la investigación científica, el diagnóstico clínico y la medicina forense. Dos de las variantes más prominentes son la electroforesis en gel y la electroforesis capilar, cada una con sus propias ventajas y un amplio abanico de aplicaciones.

La electroforesis, en su esencia, aprovecha la diferencia en la relación carga-masa de las moléculas para lograr su separación. Al aplicar un campo eléctrico a través de un medio, las partículas cargadas positivamente (cationes) migran hacia el cátodo (electrodo negativo), mientras que las partículas cargadas negativamente (aniones) se dirigen hacia el ánodo (electrodo positivo). La velocidad de esta migración no solo está influenciada por la magnitud de la carga, sino también por el tamaño y la forma de la molécula, así como por las propiedades del medio a través del cual se mueven. Este principio simple pero elegante ha dado lugar a métodos altamente sofisticados y sensibles.
- Electroforesis Capilar: Precisión y Velocidad en un Tubo Delgado
- Electroforesis en Gel: Un Pilar de la Biología Molecular
- Impacto y Futuro de la Electroforesis
- Preguntas Frecuentes (FAQs)
- ¿Cuál es la principal diferencia entre la electroforesis capilar y la electroforesis en gel?
- ¿Por qué es importante la conformación del ADN en la electroforesis en gel?
- ¿Qué es EMSA y para qué se usa?
- ¿Qué tipo de muestras se pueden analizar con electroforesis?
- ¿Qué factores afectan la separación en electroforesis?
Electroforesis Capilar: Precisión y Velocidad en un Tubo Delgado
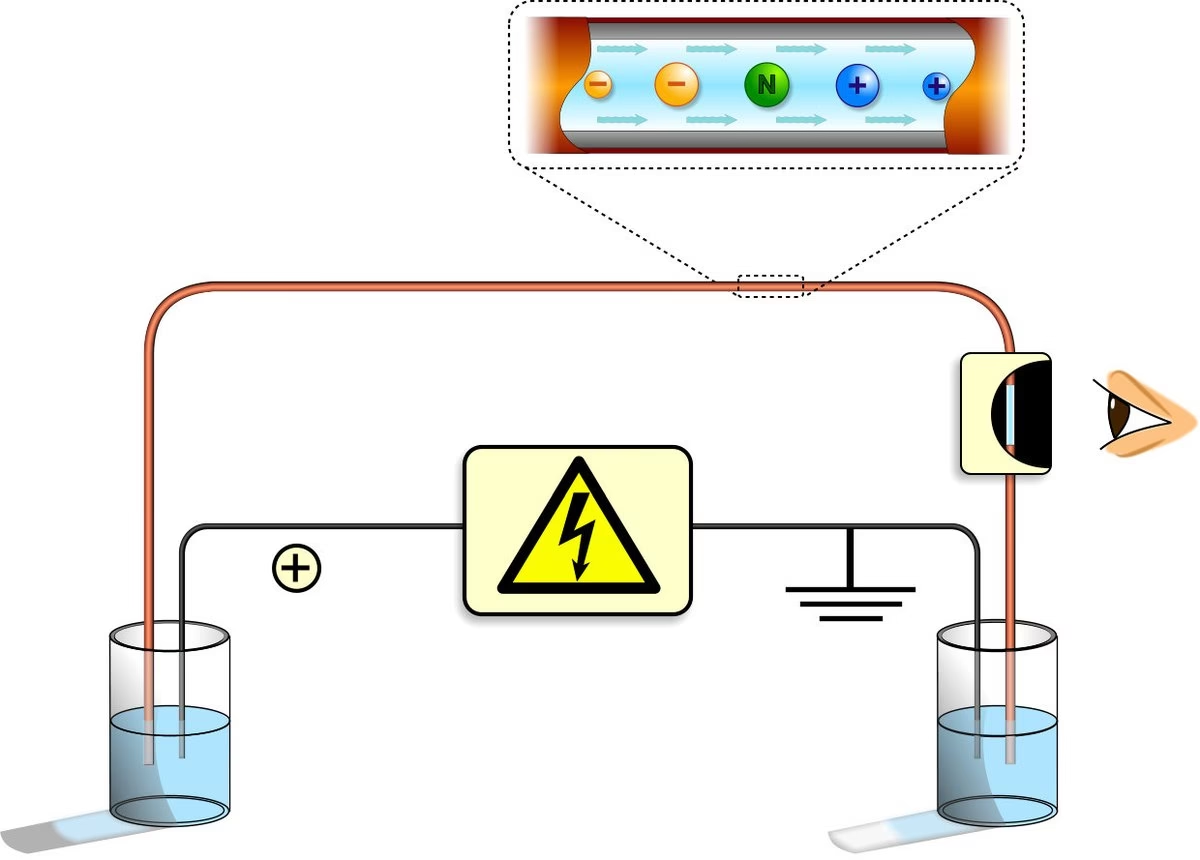
La electroforesis capilar (EC) es una técnica de separación de alta resolución que utiliza capilares de sílice fundida muy estrechos (con diámetros internos de 10 a 100 micrómetros) llenos de un electrolito. A diferencia de la electroforesis en gel, la EC no requiere una matriz de soporte porosa, aunque a veces se utilizan geles poliméricos dentro del capilar para aplicaciones específicas como la secuenciación de ADN. La separación en EC se basa principalmente en la diferente movilidad electroforética de los analitos y el flujo electroosmótico (FEO), que es el movimiento global del tampón a través del capilar.
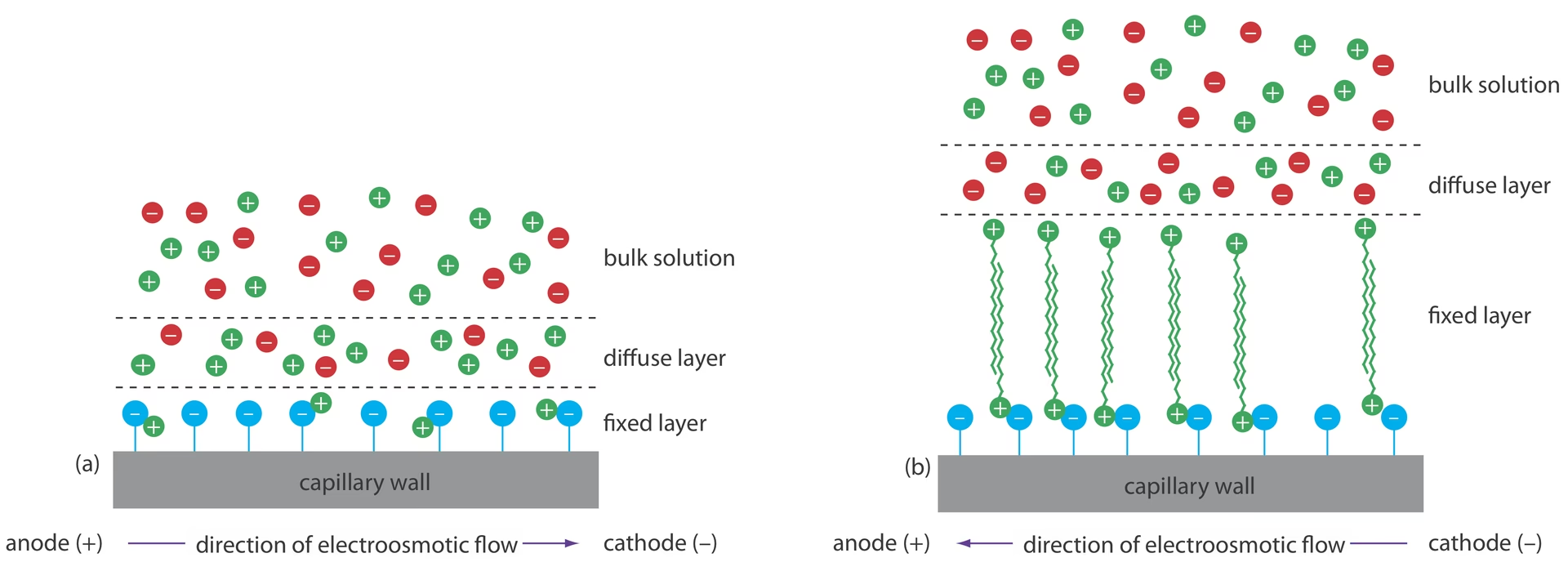
El FEO es un fenómeno que ocurre en las paredes del capilar de sílice, que tienen grupos silanol cargados negativamente. Estos grupos atraen iones positivos del tampón, formando una doble capa eléctrica. Cuando se aplica un campo eléctrico, los iones positivos en esta capa se mueven hacia el cátodo, arrastrando consigo el resto del tampón, creando un flujo de masa uniforme. Este flujo permite que incluso las moléculas neutras se desplacen a través del capilar y sean detectadas, ampliando el rango de analitos que pueden ser separados.
Aplicaciones Clave de la Electroforesis Capilar
La EC ha encontrado una amplia gama de aplicaciones en diversos campos debido a su alta eficiencia, rapidez, bajo consumo de muestra y su capacidad de automatización.
- Análisis de Ácidos Nucleicos: La EC es excepcionalmente útil para el análisis de ADN y ARN. Permite la separación de fragmentos de ADN de diferentes tamaños con una resolución asombrosa, lo que es crucial para la verificación de productos de PCR, el análisis de polimorfismos de un solo nucleótido (SNP), y la detección de mutaciones. Es capaz de distinguir pequeñas diferencias de tamaño, lo que la hace superior a la electroforesis en gel para muchas aplicaciones de alta resolución. Por ejemplo, en la evaluación de la integridad del ARN, la EC puede generar un índice de calidad del ARN (RIN) que es mucho más preciso que la visualización en gel.
- Secuenciación del Genoma: Una de las aplicaciones más revolucionarias de la EC ha sido en la secuenciación de ADN, particularmente en el método de Sanger. La EC automatizada fue la tecnología central detrás del Proyecto Genoma Humano. Permite la separación de los fragmentos de ADN marcados con fluorescencia generados en la reacción de secuenciación, con diferentes colores representando cada base (A, T, C, G). La lectura de estos colores en tiempo real a medida que pasan por el detector permite determinar la secuencia de ADN de manera rápida y precisa.
- Huellas Dactilares de ADN (DNA Fingerprinting): En medicina forense y pruebas de paternidad, la EC es la técnica de elección para el análisis de repeticiones cortas en tándem (STRs). Los STRs son regiones del ADN altamente polimórficas que varían en el número de repeticiones entre individuos. La EC separa estos fragmentos de STRs marcados con fluorescencia por tamaño, generando un perfil único para cada individuo. Esta técnica es extremadamente sensible y requiere muy poca muestra, lo que la hace ideal para muestras biológicas limitadas encontradas en escenas del crimen.
- Separación de Coenzimas y Metabolitos: La EC es una herramienta valiosa para el análisis de moléculas pequeñas y medianas, incluyendo coenzimas, vitaminas, aminoácidos y metabolitos. Permite la identificación y cuantificación de estos compuestos en matrices biológicas complejas, lo que es fundamental para estudios metabólicos, el descubrimiento de biomarcadores y el control de calidad farmacéutico.
- Identificación y Caracterización de Proteínas: Aunque las proteínas son más complejas debido a su variabilidad de carga y estructura tridimensional, la EC se ha adaptado para su análisis. Se utiliza para la evaluación de la pureza de proteínas terapéuticas, la detección de isoformas, la caracterización de glicosilación y otras modificaciones post-traduccionales, y el análisis de péptidos. La EC puede ofrecer una resolución superior para separar variantes de proteínas que difieren sutilmente en carga o tamaño.
Electroforesis en Gel: Un Pilar de la Biología Molecular
La electroforesis en gel es quizás la técnica electroforética más familiar y ampliamente utilizada en laboratorios de biología molecular y bioquímica. En este método, las moléculas se separan a medida que migran a través de una matriz de gel porosa, que actúa como un tamiz molecular. Los geles más comunes son el agarosa (para ADN y ARN de gran tamaño) y la poliacrilamida (para ADN/ARN más pequeños y proteínas).
El gel está sumergido en un tampón conductor y se aplica un campo eléctrico a través de él. Las moléculas cargadas negativamente, como el ADN y el ARN, migran hacia el ánodo, mientras que las proteínas, que pueden tener cargas variables, a menudo se tratan con dodecil sulfato de sodio (SDS) para conferirles una carga negativa uniforme y permitir la separación por tamaño. El tamaño de los poros del gel es crucial; las moléculas más pequeñas se mueven más fácilmente a través de los poros y, por lo tanto, migran más rápido que las moléculas más grandes.
Aplicaciones Clave de la Electroforesis en Gel
La electroforesis en gel es una herramienta versátil con aplicaciones fundamentales en el estudio de ácidos nucleicos y proteínas.
- Evaluación de la Conformación del ADN: El ADN plasmídico de la misma secuencia puede mostrar diferentes movilidades electroforéticas dependiendo de su conformación. Esto es extremadamente útil para evaluar la calidad y la integridad de las preparaciones de plásmidos. Por ejemplo, un plásmido puede existir en varias formas: superenrollado (la forma más compacta y rápida en gel), relajado (cuando una hebra está rota, migra más lento), o lineal (cuando ambas hebras están cortadas, migra aún más lento). La capacidad de distinguir estas formas es vital en la investigación de clonación, terapia génica y producción de vacunas, donde la forma superenrollada es a menudo la deseada. Esta característica permite a los investigadores asegurar la integridad y funcionalidad de sus constructos de ADN.
- Complejos Ácido Nucleico-Proteína (EMSA o Gel Shift Assay): El Ensayo de Movilidad Electroforética Modificada (EMSA), también conocido como ensayo de desplazamiento en gel o ensayo de retardo en gel, es una técnica poderosa utilizada para detectar interacciones entre proteínas y ácidos nucleicos (ADN o ARN) en una muestra. El principio es simple pero efectivo: cuando un fragmento de ácido nucleico se une a una proteína, el complejo resultante es significativamente más grande y, por lo tanto, migra más lentamente a través del gel que el fragmento de ácido nucleico libre y sin unir.
El paso de electroforesis en EMSA proporciona una 'instantánea' del equilibrio entre el ADN unido y el ADN libre en la muestra. Para optimizar el ensayo, es fundamental utilizar un tampón de baja fuerza iónica tanto en la preparación del gel como en la corrida electroforética. Esto es crucial porque ayuda a estabilizar el complejo ácido nucleico-proteína. Las interacciones entre proteínas y ácidos nucleicos son a menudo no covalentes y pueden ser sensibles a las condiciones iónicas. Un tampón de baja fuerza iónica minimiza la interferencia de iones libres que podrían competir o desestabilizar el complejo, permitiendo una visualización clara del desplazamiento del gel.
Las aplicaciones de EMSA son vastas e incluyen:
- Identificación de Factores de Transcripción: Determinar qué proteínas se unen a secuencias reguladoras específicas del ADN para controlar la expresión génica.
- Estudio de Vías de Señalización: Analizar cómo las señales celulares afectan la unión de proteínas al ADN.
- Descubrimiento de Fármacos: Identificar compuestos que pueden inhibir o potenciar la interacción entre proteínas y ácidos nucleicos.
- Análisis de la Especificidad de Unión: Realizar experimentos de competencia con sondas frías (no marcadas) para confirmar que la unión es específica a la secuencia.
Tabla Comparativa: Electroforesis Capilar vs. Electroforesis en Gel
| Característica | Electroforesis Capilar (EC) | Electroforesis en Gel (EG) |
|---|---|---|
| Medio de Separación | Capilar de sílice fundida (líquido o con gel polimérico) | Matriz de gel porosa (agarosa o poliacrilamida) |
| Resolución | Muy alta (separación de moléculas con diferencias mínimas) | Buena a muy buena (depende del tipo y concentración del gel) |
| Velocidad | Rápida (minutos a decenas de minutos) | Más lenta (horas a varias horas) |
| Automatización | Alta (sistemas robotizados) | Baja a moderada (requiere manipulación manual) |
| Volumen de Muestra | Muy pequeño (nanolitros) | Pequeño (microlitros) |
| Detección | Generalmente en línea (UV, fluorescencia, espectrometría de masas) | Post-separación (tinción, autorradiografía, inmunodetección) |
| Cuantificación | Precisa y automatizada | Menos precisa, a menudo visual o densitométrica |
| Aplicaciones Típicas | Secuenciación de ADN, huellas dactilares de ADN, análisis de pureza de fármacos, separación de metabolitos, análisis de proteínas. | EMSA, análisis de conformación de ADN, separación de fragmentos de ADN/ARN, análisis de proteínas por SDS-PAGE. |
| Costo por Muestra | Más alto (debido a equipos especializados) | Más bajo (equipo estándar de laboratorio) |
| Formato | Líquido, cerrado, automatizado | Gel sólido, abierto, manual |
La elección entre electroforesis capilar y electroforesis en gel a menudo depende de los requisitos específicos del experimento, la resolución necesaria, la cantidad de muestra disponible y el nivel de automatización deseado. Ambas técnicas han demostrado ser herramientas indispensables en sus respectivos nichos.
Impacto y Futuro de la Electroforesis
Las aplicaciones de la electroforesis, tanto en su formato capilar como en gel, han tenido un impacto profundo en la biología, la medicina y la biotecnología. Han permitido a los científicos desentrañar los misterios de la vida a nivel molecular, desde la identificación de genes responsables de enfermedades hasta la comprensión de cómo las proteínas regulan los procesos celulares. En el ámbito clínico, la electroforesis es una herramienta diagnóstica esencial para detectar anomalías genéticas, enfermedades infecciosas y trastornos metabólicos.
El futuro de la electroforesis apunta hacia una mayor integración con otras técnicas (como la espectrometría de masas), la miniaturización (lab-on-a-chip), y la mejora de la automatización para aumentar el rendimiento y la velocidad. Los avances en microfluídica están permitiendo el desarrollo de dispositivos portátiles que podrían llevar las capacidades de la electroforesis a entornos de punto de atención, revolucionando el diagnóstico rápido. La continua evolución de estas técnicas promete seguir impulsando la investigación y la innovación en el análisis molecular.
Preguntas Frecuentes (FAQs)
¿Cuál es la principal diferencia entre la electroforesis capilar y la electroforesis en gel?
La principal diferencia radica en el medio de separación y la resolución. La electroforesis capilar utiliza un capilar delgado lleno de un electrolito líquido o un gel polimérico, ofreciendo una alta resolución y velocidad. La electroforesis en gel, por otro lado, utiliza una matriz de gel porosa (agarosa o poliacrilamida) como tamiz molecular, siendo más adecuada para la separación de moléculas de mayor tamaño y para la visualización directa de bandas.
¿Por qué es importante la conformación del ADN en la electroforesis en gel?
La conformación del ADN es crucial porque afecta directamente su movilidad en el gel. El ADN plasmídico, por ejemplo, puede existir en formas superenrolladas, relajadas o lineales. Cada una de estas formas tiene una estructura tridimensional diferente que interactúa de manera distinta con la matriz del gel, resultando en velocidades de migración únicas. Evaluar la conformación es vital para asegurar la calidad y la integridad de las preparaciones de plásmidos utilizadas en experimentos de clonación o terapia génica.
¿Qué es EMSA y para qué se usa?
EMSA (Ensayo de Movilidad Electroforética Modificada) es una técnica utilizada para detectar y estudiar la interacción entre proteínas y ácidos nucleicos (ADN o ARN). Se basa en el principio de que un complejo de proteína-ácido nucleico migra más lentamente en un gel que el ácido nucleico libre. Se utiliza ampliamente para identificar factores de transcripción, estudiar la regulación génica y caracterizar la especificidad de unión de proteínas a secuencias de ADN o ARN.
¿Qué tipo de muestras se pueden analizar con electroforesis?
La electroforesis puede analizar una amplia variedad de muestras biológicas y químicas que contienen moléculas cargadas. Esto incluye ácidos nucleicos (ADN, ARN, oligonucleótidos), proteínas (enzimas, anticuerpos, factores de transcripción), péptidos, metabolitos, coenzimas, aminoácidos e incluso iones inorgánicos. La elección de la técnica específica (capilar o en gel) dependerá del tipo de molécula y el objetivo del análisis.
¿Qué factores afectan la separación en electroforesis?
Varios factores influyen en la separación electroforética. Estos incluyen la carga y el tamaño de las moléculas a separar, la fuerza del campo eléctrico aplicado, la concentración y la composición del gel o el electrolito (especialmente el pH y la fuerza iónica del tampón), la temperatura y la duración de la corrida. Un control cuidadoso de estos parámetros es esencial para obtener resultados óptimos y reproducibles.
Si quieres conocer otros artículos parecidos a Aplicaciones de la Electroforesis: Un Vistazo Profundo puedes visitar la categoría Cabello.