06/08/2019
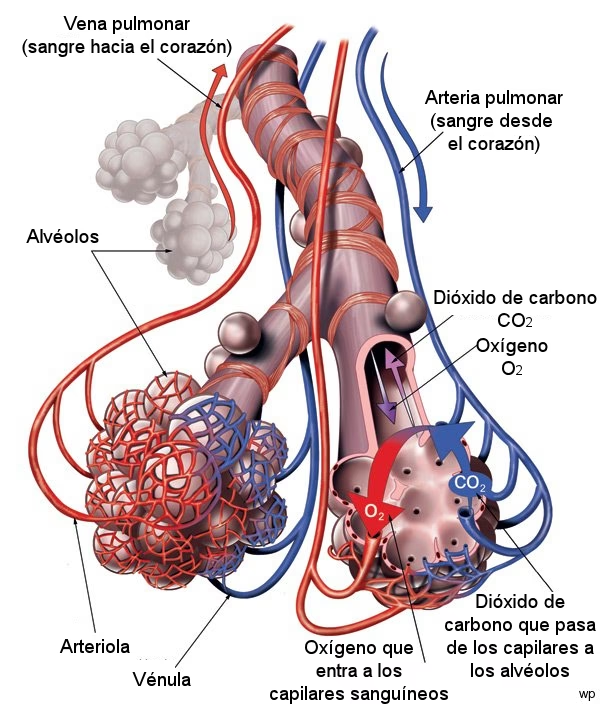
La vida, tal como la conocemos, depende de un proceso aparentemente simple pero extraordinariamente complejo: el intercambio gaseoso. En cada respiración, nuestros pulmones orquestan una danza vital entre el aire que inhalamos y la sangre que fluye por nuestro cuerpo, garantizando que el oxígeno llegue a cada célula y el dióxido de carbono sea eliminado. El corazón de esta operación reside en una estructura microscópica, pero de vital importancia: la unidad alveolo-capilar. Esta maravilla biológica es el punto donde la naturaleza ha perfeccionado la eficiencia, permitiendo que billones de moléculas de oxígeno y dióxido de carbono crucen una barrera casi imperceptiblemente delgada, pero fundamental para nuestra existencia.
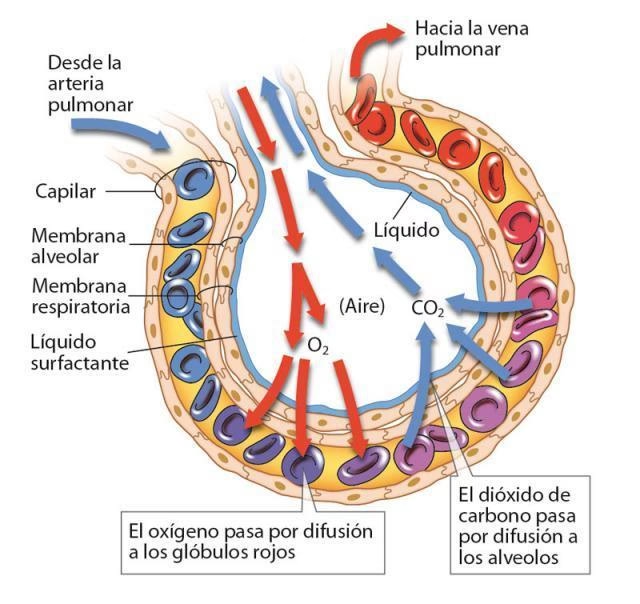
La unidad alveolo-capilar, el epicentro del intercambio gaseoso, está compuesta por el endotelio capilar y su membrana basal, el espacio intersticial, y el epitelio alveolar con su propia membrana basal. De esta forma, la barrera alveolo-capilar que separa el espacio aéreo de la sangre capilar es de un grosor asombrosamente reducido: solo 0,5 micras. Esta delgadez extrema es la clave de su eficiencia, permitiendo una rápida y eficaz difusión de gases, siempre y cuando la ventilación de los alvéolos sea la adecuada.
El Intercambio Gaseoso en Condiciones Normales: Una Sinfonía Perfecta
Para comprender las complejidades de las alteraciones, primero debemos asentar las bases del funcionamiento normal. El intercambio de gases en los pulmones se produce gracias a un acoplamiento casi perfecto entre la ventilación (el flujo de aire hacia y desde los alvéolos) y la perfusión (el flujo de sangre a través de los capilares pulmonares). Esta relación se conoce como el cociente ventilación/perfusión (V/Q).
En reposo, la ventilación alveolar, que es el volumen de aire fresco que realmente llega a los alvéolos para el intercambio (descontando el espacio muerto anatómico), es de aproximadamente 5 litros por minuto. Sorprendentemente, este valor es muy similar al gasto cardíaco, que es el volumen de sangre que el corazón bombea a través de los pulmones cada minuto. Dado que la totalidad del gasto cardíaco transita por los pulmones, la relación V/Q global del sistema cardiopulmonar es aproximadamente 1. Esta proporción ideal asegura que cada unidad alveolar bien ventilada esté también bien perfundida, maximizando la eficiencia del intercambio.
Sin embargo, a nivel local, el cuerpo no es una máquina perfecta. Los cocientes V/Q pueden variar considerablemente dentro del pulmón debido a factores como el efecto hidrostático y las diferencias intrarregionales en la distribución del flujo sanguíneo. Esta heterogeneidad, aunque mínima en condiciones normales, puede aumentar con la edad o en presencia de afectaciones pulmonares, ya sea por una distribución irregular de la ventilación, de la perfusión, o de ambas. Las áreas donde el cociente V/Q es muy elevado indican una ventilación ineficaz. En su extremo, cuando la ventilación es máxima pero la perfusión es nula (V/Q tiende a infinito), se produce lo que se conoce como efecto espacio muerto. Por otro lado, las áreas con un cociente V/Q bajo, donde hay poca o ninguna ventilación pero sí perfusión (V/Q tiende a cero), causan hipoxemia, un fenómeno conocido como efecto shunt. A pesar de estas variaciones locales, en condiciones normales, la cantidad mínima de unidades con cocientes V/Q alejados de la unidad no altera el efecto mayoritario de las unidades normales, manteniendo el V/Q global cerca de 1.
Incluso durante el ejercicio, cuando la demanda de oxígeno aumenta drásticamente, el cuerpo mantiene esta relación V/Q. El aumento de la ventilación se ajusta al aumento del gasto cardíaco, preservando el equilibrio. La capacidad de aumentar la ventilación es mucho mayor que la del gasto cardíaco, lo que significa que cualquier disminución del V/Q en estas condiciones debe atribuirse a una afectación directa del sistema respiratorio y no a un aumento aislado del gasto cardíaco, como podría ocurrir en casos de fiebre o tirotoxicosis. El diagnóstico posterior implicaría diferenciar entre causas de disminución de la ventilación (como sedantes o encefalopatía) y causas intrapulmonares que reducen el V/Q a pesar de una ventilación minuto adecuada.
Factores Extrapulmonares que Desafían el Intercambio Gaseoso
Aunque el pulmón es el actor principal, el intercambio gaseoso puede verse afectado por factores externos a él. La gasometría arterial es una herramienta crucial para evaluar estas alteraciones. Por ejemplo, el dolor, especialmente en pacientes con traumatismos torácicos o abdominales o postoperados, puede llevar a una disminución de la ventilación alveolar debido a la inhibición de la inspiración. El fallo cardíaco severo también puede causar hipoxemia no pulmonar; la sangre venosa que llega a los pulmones tiene una saturación de oxígeno extremadamente baja, magnificando el efecto del shunt fisiológico. Además, los cortocircuitos arteriovenosos intracardíacos o periféricos, como las fístulas en pacientes en diálisis crónica, pueden generar un efecto shunt. En contraste, situaciones que aumentan desproporcionadamente el volumen minuto, como la fiebre alta o la ansiedad, pueden provocar disminuciones de la presión parcial de CO2 (PaCO2) que no reflejan una alteración real del V/Q.
El Síndrome de Distrés Respiratorio Agudo (SDRA): Un Ataque al Intercambio Gaseoso
El SDRA es una condición devastadora que altera profundamente el intercambio gaseoso. Se caracteriza por un edema pulmonar debido a un aumento de la permeabilidad de la barrera alveolo-capilar. La alteración inicial es la ocupación alveolar por un edema rico en proteínas, lo que reduce drásticamente la superficie alveolar disponible para el intercambio gaseoso. Esto se traduce en un aumento de las áreas con una relación V/Q pobre o nula. Ante esta alteración y la hipoxemia resultante, el sistema respiratorio intenta compensar con un aumento de la ventilación minuto. Sin embargo, debido a la ocupación física de los alvéolos, esta ventilación adicional se dirige a las zonas ya bien aireadas, hiperventilando áreas preservadas sin corregir las zonas con efecto shunt. Por lo tanto, en esta fase inicial, la gasometría típicamente muestra hipoxemia, acompañada de hipocapnia y alcalosis.
Es crucial recordar que el SDRA es un síndrome que refleja una lesión pulmonar, ya sea por una afectación cercana (causa pulmonar) o distante (causa extrapulmonar). Casi todos los casos de SDRA van acompañados de un síndrome de respuesta inflamatoria sistémica (SIRS), lo que introduce una serie de factores extrapulmonares que interfieren en la evaluación del intercambio gaseoso. Un factor significativo es el aumento del gasto cardíaco, que en el SDRA incrementa la perfusión de las zonas no ventiladas y recluta capilares previamente cerrados, lo que a menudo empeora el efecto shunt y la hipoxemia. Si además coexiste hipoperfusión periférica debido a la sepsis, la saturación venosa central de oxígeno (SvO2) puede ser muy baja, lo que agrava aún más la hipoxemia de la sangre arterial a su paso por el pulmón.
Los mediadores inflamatorios liberados durante el SIRS pueden afectar el intercambio gaseoso de diversas maneras. Algunos pueden causar broncoconstricción, aumentando las desigualdades V/Q. Otros pueden provocar vasoconstricción pulmonar, incrementando la velocidad del flujo sanguíneo a través de los pulmones y reduciendo el tiempo disponible para el intercambio gaseoso en el alvéolo. Si esta vasoconstricción afecta principalmente al esfínter precapilar, se reducirá el flujo sanguíneo pulmonar, lo que podría mitigar la producción de edema. Por el contrario, si afecta mayoritariamente al esfínter postcapilar, habrá una mayor estasis capilar pulmonar, aumentando la presión capilar y el edema. En los casos más severos de vasoconstricción pulmonar, puede desarrollarse un fallo ventricular derecho (cor pulmonale agudo), lo que agravaría el deterioro de la SvO2 y su impacto en la hipoxemia.
La Progresión del SDRA: Fenómenos Vasculares y Atelectasias
A medida que el SDRA avanza, se producen fenómenos vasculares que alteran aún más el intercambio gaseoso. Las zonas mal ventiladas, debido a la ocupación alveolar, reaccionan a la hipoxia local con vasoconstricción localizada, reduciendo el flujo sanguíneo a estas áreas y redirigiéndolo hacia las zonas mejor ventiladas. Más tarde, pueden ocurrir fenómenos de microtrombosis en pequeños vasos pulmonares, creando zonas parcheadas de espacio muerto y aumentando los desequilibrios V/Q. Esto explica por qué muchos casos letales de SDRA evolucionan hacia una hipercapnia progresiva, a pesar del aumento progresivo de la ventilación minuto con el ventilador en las fases finales.
Un factor adicional que empeora el intercambio gaseoso progresivo en el SDRA es la formación de atelectasias en las zonas declives del pulmón. Estas se ven favorecidas por el decúbito supino prolongado, la sedación profunda (con o sin parálisis muscular), la ausencia de contracción diafragmática activa y, finalmente, la reabsorción del gas inspirado cuando se utilizan concentraciones elevadas de oxígeno, un fenómeno conocido como atelectasias por desnitrogenización. Estas zonas de muy bajo o nulo V/Q se suman a las ya existentes, configurando un cuadro de hipoxemia refractaria al aumento del oxígeno inspirado. Aunque la gravedad del shunt ha sido el marcador más común para evaluar la severidad del SDRA, el espacio muerto ha resurgido como un marcador adicional de gravedad. Estudios han demostrado que el Vd/Vt (cociente entre el volumen de espacio muerto y el volumen corriente) es un factor independiente asociado a la mortalidad, con valores superiores a 0,7 asociados a una mortalidad significativamente alta.
El Impacto de la Ventilación Mecánica: Un Arma de Doble Filo
Las intervenciones terapéuticas, especialmente la ventilación mecánica, tienen un efecto significativo en el intercambio gaseoso durante el SDRA. La ventilación con presión positiva, universalmente aplicada de forma invasiva, implica la intubación y, a menudo, sedación con o sin parálisis muscular. La sedación, junto con el decúbito supino y la ausencia de tono de la musculatura respiratoria, reduce el volumen intrapulmonar a expensas de la capacidad residual funcional. Esto provoca una reducción del V/Q en zonas dependientes que antes eran normales, y puede llevar al shunt por colapso alveolar en zonas que ya tenían un V/Q bajo.
Para contrarrestar esto, la Presión Positiva Telespiratoria (PEEP) se utiliza comúnmente en niveles bajos (5 a 7 cmH2O) para evitar el colapso pulmonar. En pacientes con obesidad mórbida o presión intraabdominal elevada, niveles superiores de PEEP (10 a 12 cmH2O) pueden ser beneficiosos. La respiración espontánea, incluso con sedación menor, ha demostrado mejorar la relación PaO2/FiO2, aumentar el gasto cardíaco y reducir el shunt, sin afectar significativamente la PaCO2 o el espacio muerto.
La ventilación mecánica busca lograr la mayor ventilación alveolar con la menor lesión pulmonar. Esto implica usar niveles de PEEP que mantengan abiertos el mayor número de alvéolos, evitando su colapso durante la espiración, sin provocar una sobredistensión significativa de las áreas sanas. En términos de V/Q, el objetivo es reducir las áreas de shunt y V/Q bajo, minimizando el aumento de áreas con V/Q elevado o espacio muerto.
Las maniobras de reclutamiento alveolar buscan abrir áreas colapsadas aplicando una gran presión intraalveolar transitoria, para luego mantenerlas abiertas con PEEP moderada. Sin embargo, durante estas maniobras, las unidades sanas pueden sobredistenderse, creando un efecto de espacio muerto significativo y desviando el flujo vascular. Si las zonas consolidadas no se abren, se podría aumentar su perfusión, empeorando el efecto shunt. Algunos estudios incluso han correlacionado los mínimos beneficios de estas maniobras con aumentos en los desequilibrios V/Q debido a la redistribución del flujo pulmonar hacia zonas no ventiladas.
El patrón de flujo inspiratorio también influye. Aunque el flujo constante es común, el flujo decelerado (mayor al inicio y decreciente durante la inspiración) se ha propuesto para mejorar la ventilación, permitiendo la insuflación de áreas con V/Q bajo o constante de tiempo lenta en la segunda fase. No obstante, esta ventaja teórica no se ha demostrado claramente en pacientes reales. Por el contrario, alargar el tiempo inspiratorio o la pausa inspiratoria puede reducir mínimamente las desigualdades V/Q y la hipercapnia.
Un aspecto innovador es el decúbito prono, que ha demostrado consistentemente mejorar la hipoxemia refractaria en muchos pacientes. Sus mecanismos son complejos, incluyendo la redistribución del flujo sanguíneo hacia zonas no colapsadas, la reducción del gradiente vertical de presión transpulmonar que disminuye el colapso de las zonas dependientes, y la eliminación del colapso provocado por el corazón y el mediastino sobre el pulmón adyacente. La rapidez con la que las alteraciones V/Q reaparecen al reposicionar al paciente en supino subraya la naturaleza dinámica y reversible del reclutamiento alveolar y vascular en esta posición.
Tratamientos Farmacológicos: Buscando el Equilibrio V/Q
La búsqueda de fármacos que manipulen las alteraciones V/Q ha sido constante. La almitrina, un fármaco inicialmente usado como estimulante respiratorio, se abandonó por falta de efectos definidos y por causar hipertensión arterial pulmonar. Su mecanismo de potenciar la vasoconstricción hipóxica, aunque buscaba reducir el flujo a zonas mal ventiladas en el SDRA, no logró un efecto suficiente para reducir las dosis de oxígeno a niveles no tóxicos ni modificó significativamente la evolución de los pacientes. El efecto nocivo sobre la hipertensión pulmonar probablemente contrarresta cualquier beneficio.
Más recientemente, el óxido nítrico inhalatorio ha ofrecido una alternativa. Es un potente vasodilatador endógeno con una vida media muy corta, lo que significa que, administrado por vía inhalatoria, solo actúa sobre los alvéolos bien ventilados, provocando vasodilatación local y un efecto de "robo de flujo" de las zonas mal ventiladas. Esta mejoría del intercambio gaseoso, principalmente por reducción del efecto shunt, se ha comprobado en la mayoría de los pacientes con SDRA en fase aguda. Su efecto aditivo con el decúbito prono refuerza esta hipótesis: cuando el prono abre más alvéolos funcionales, el óxido nítrico potencia la reducción del shunt. Sin embargo, es importante destacar que, a pesar de estos beneficios sobre el intercambio gaseoso, no se han traducido en una mejor evolución de los pacientes con SDRA.
La Resolución del SDRA y sus Consecuencias a Largo Plazo
La resolución del SDRA es muy variable y no siempre se correlaciona fiablemente con las alteraciones anatomopatológicas o las pruebas de función pulmonar. Clínicamente, la mejora más precoz suele ser la hipoxemia, incluso cuando la mecánica pulmonar sigue muy alterada y los requerimientos de volumen minuto elevados, sugiriendo la persistencia del aumento del espacio muerto. Es probable que esta mejora del shunt se deba a la reducción de factores coadyuvantes como la parálisis muscular, el decúbito prolongado y la ausencia de respiración espontánea.
Al alta de la Unidad de Cuidados Intensivos, muchos pacientes aún presentan un aumento de la elastancia pulmonar y un incremento del trabajo respiratorio. Este aumento, junto con la debilidad muscular generalizada tras un SDRA, conduce a un patrón respiratorio rápido y superficial, lo que reduce la ventilación alveolar efectiva y aumenta el efecto espacio muerto. Estas alteraciones se resuelven muy lentamente, y pueden encontrarse afectaciones residuales del intercambio gaseoso incluso un año después de haber sufrido un episodio de SDRA. La capacidad de difusión a través de la membrana alveolo-capilar, que se vería afectada por la formación de membranas hialinas y fibrosis pulmonar a partir de la primera semana de evolución, podría ser un factor adicional en el empeoramiento progresivo del intercambio gaseoso en las fases más avanzadas.
Tabla Comparativa: Intercambio Gaseoso Normal vs. SDRA
| Característica | Condiciones Normales | Síndrome de Distrés Respiratorio Agudo (SDRA) |
|---|---|---|
| Grosor Barrera Alveolo-Capilar | 0,5 micras (óptimo para difusión) | Aumentado por edema y fibrosis (deteriora difusión) |
| Intercambio Gaseoso | Eficiente y rápido | Severamente comprometido |
| Relación V/Q Global | Aproximadamente 1 | Altamente heterogénea y alterada |
| Efecto Shunt | Mínimo (fisiológico) | Significativamente aumentado (hipoxemia refractaria) |
| Efecto Espacio Muerto | Mínimo (fisiológico) | Aumentado (ventilación ineficaz, hipercapnia) |
| Presencia de Edema | Ausente | Edema rico en proteínas (aumento de permeabilidad) |
| Superficie Alveolar Funcional | Máxima | Reducida por ocupación alveolar y colapso |
| Mecánica Pulmonar | Normal | Elastancia pulmonar aumentada, compliancia disminuida |
| Respuesta a Oxígeno Suplementario | No aplica (saturación normal) | Hipoxemia refractaria (respuesta limitada) |
Preguntas Frecuentes sobre el Intercambio Gaseoso y el SDRA
¿Cuál es el grosor exacto de la membrana alveolo-capilar en condiciones normales?
En condiciones normales, la barrera alveolo-capilar tiene un grosor de solo 0,5 micras. Esta extrema delgadez es crucial para el eficiente intercambio de gases entre el aire alveolar y la sangre capilar.
¿Qué significa la relación V/Q y por qué es importante?
La relación V/Q (ventilación/perfusión) es el cociente entre el volumen de aire que llega a los alvéolos para el intercambio gaseoso (ventilación) y el volumen de sangre que fluye a través de los capilares pulmonares (perfusión). Es fundamental porque un equilibrio adecuado (V/Q cercano a 1) garantiza que el oxígeno llegue a la sangre y el dióxido de carbono sea eliminado de manera eficiente. Desequilibrios en esta relación son la principal causa de alteraciones en el intercambio gaseoso.
¿Cómo afecta el SDRA el intercambio gaseoso?
El SDRA causa un edema pulmonar debido a un aumento de la permeabilidad de la barrera alveolo-capilar. Este edema inunda los alvéolos, reduciendo la superficie disponible para el intercambio gaseoso. Esto lleva a un aumento significativo de las áreas con bajo V/Q (efecto shunt) y, a medida que progresa, también de las áreas de espacio muerto, resultando en hipoxemia severa y, en fases avanzadas, hipercapnia.
¿Qué es el efecto shunt y el efecto espacio muerto?
El efecto shunt ocurre cuando hay perfusión sanguínea en zonas del pulmón que no están ventiladas (V/Q cercano a cero), lo que significa que la sangre pasa por los pulmones sin oxigenarse adecuadamente. El efecto espacio muerto se da cuando hay ventilación en zonas del pulmón que no están perfundidas (V/Q tiende a infinito), lo que implica que el aire llega a zonas donde no puede realizarse el intercambio gaseoso, siendo una ventilación ineficaz.
¿Por qué el decúbito prono mejora la oxigenación en pacientes con SDRA?
El decúbito prono (boca abajo) mejora la oxigenación al redistribuir el flujo sanguíneo hacia zonas pulmonares mejor ventiladas. También reduce el gradiente vertical de presión transpulmonar, lo que disminuye el colapso de las zonas dependientes. Además, alivia el colapso provocado por el corazón y el mediastino sobre el pulmón adyacente, aumentando el número de alvéolos funcionales y mejorando la relación V/Q.
¿El óxido nítrico inhalatorio cura el SDRA?
Aunque el óxido nítrico inhalatorio es un vasodilatador potente que puede mejorar agudamente el intercambio gaseoso al reducir el efecto shunt en muchos pacientes con SDRA, no ha demostrado una mejora significativa en la evolución general o la mortalidad de los pacientes. Sus efectos son principalmente sintomáticos y temporales, no curativos.
Si quieres conocer otros artículos parecidos a El Velo Vital: La Barrera Alveolo-Capilar y el Intercambio Gaseoso puedes visitar la categoría Cabello.