07/12/2013
En el vasto universo de la química analítica, la capacidad de separar y cuantificar los componentes de una mezcla es fundamental para la investigación, el desarrollo de productos y el control de calidad. Desde la composición de un fármaco hasta la pureza de una muestra biológica, la necesidad de técnicas eficientes y precisas es constante. Es en este contexto que emerge una de las herramientas más sofisticadas y versátiles de los últimos tiempos: la Electroforesis Capilar (EC), una técnica que ha transformado la manera en que abordamos la separación de una amplia gama de sustancias.
La Electroforesis Capilar no es simplemente un método; es un paradigma de eficiencia y versatilidad que permite desentrañar la complejidad de mezclas que antes resultaban inabordables. Su principio se basa en la migración diferencial de los analitos dentro de un capilar estrecho bajo la influencia de un campo eléctrico, una característica que le confiere una capacidad de resolución excepcional. Pero, ¿qué hace exactamente a la EC tan especial y cuáles son sus considerables ventajas y sus inevitables limitaciones?
¿Qué es la Electroforesis Capilar (EC)?
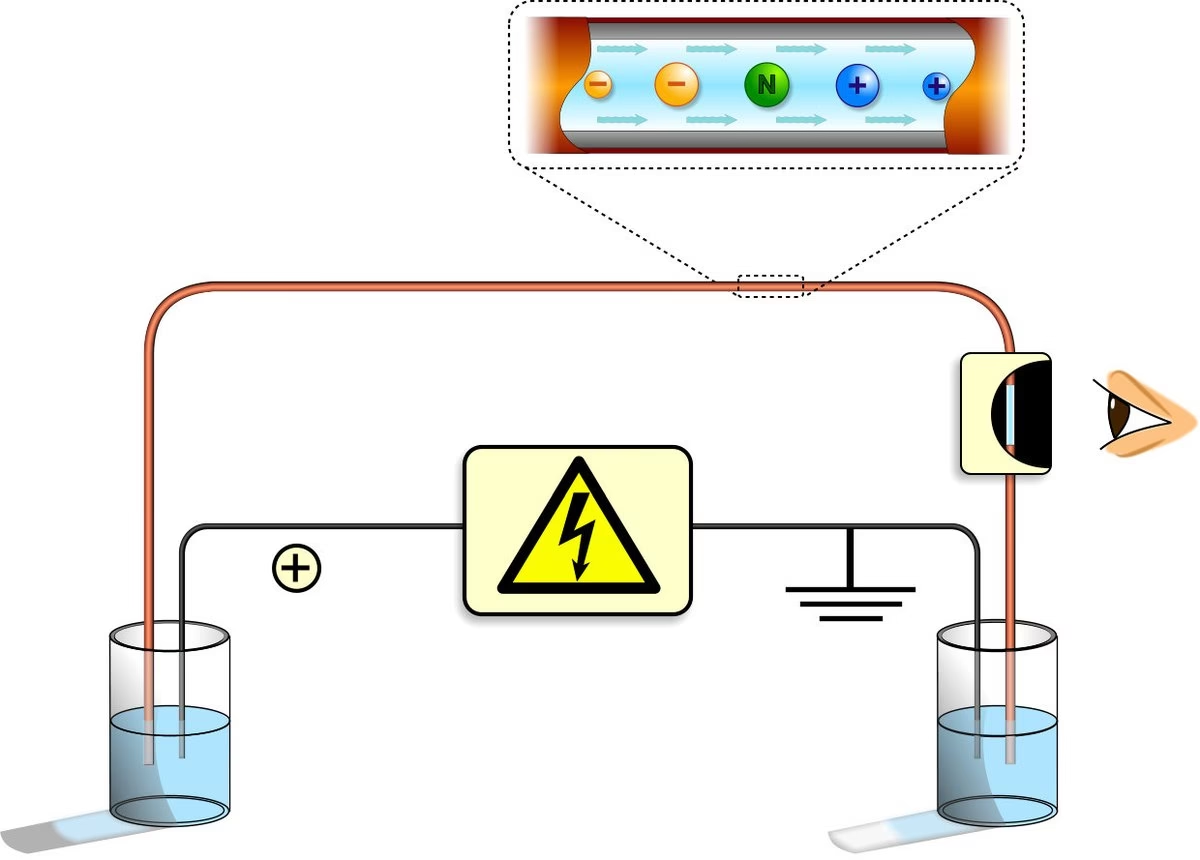
La Electroforesis Capilar (EC) es una poderosa técnica de separación analítica que se fundamenta en la migración de iones en solución bajo la influencia de un campo eléctrico. A diferencia de las técnicas de electroforesis tradicionales que utilizan geles como medio de soporte, la EC realiza la separación dentro de un capilar de sílice fundida extremadamente delgado, generalmente con diámetros internos que oscilan entre 20 y 100 micrómetros. Este diseño minimiza el calentamiento Joule (generación de calor por el paso de corriente), lo que permite aplicar voltajes muy altos (hasta 30 kV) y, por ende, lograr separaciones rápidas y altamente eficientes.
El principio fundamental de la EC radica en la diferente relación carga/masa de los analitos. Cuando se aplica un alto voltaje a través del capilar lleno de una solución tampón (electrolito de fondo), los iones cargados de la muestra migran hacia el electrodo de polaridad opuesta. Los iones con mayor relación carga/masa y menor tamaño experimentarán una movilidad electroforética más rápida y, por lo tanto, llegarán al detector primero. Este movimiento se combina con un fenómeno conocido como flujo electroosmótico (EOF). El EOF es el movimiento global del tampón dentro del capilar, generado por la interacción entre la superficie cargada del capilar y los iones en la solución tampón. En la mayoría de los casos, el EOF es lo suficientemente fuerte como para arrastrar incluso a las moléculas neutras hacia el detector, lo que amplía enormemente el rango de analitos que pueden ser separados.
Esta combinación de movilidad electroforética y flujo electroosmótico permite a la EC separar una amplia gama de analitos, desde pequeños iones inorgánicos y compuestos orgánicos simples hasta macromoléculas complejas como proteínas, péptidos, ácidos nucleicos e incluso células enteras. Es una técnica verdaderamente versátil, capaz de manejar tanto moléculas cargadas como no cargadas, lo que la convierte en una herramienta indispensable en campos como la farmacéutica, la biotecnología, la química clínica y el análisis ambiental.
Componentes Clave de un Sistema de Electroforesis Capilar
Un sistema de Electroforesis Capilar típico consta de varios componentes esenciales que trabajan en conjunto para lograr la separación y detección de los analitos:
- Fuente de alto voltaje: Suministra la corriente eléctrica necesaria para la migración de los iones y la generación del flujo electroosmótico.
- Capilar: El corazón del sistema, generalmente de sílice fundida, recubierto externamente con poliamida para mayor resistencia mecánica. Su estrecho diámetro es crucial para la alta eficiencia.
- Viales de muestra y tampón: Contenedores para la muestra a analizar y los tampones de electroforesis, ubicados en ambos extremos del capilar.
- Electrodos: Sumergidos en los viales de tampón, aplican el campo eléctrico a través del capilar.
- Detector: Situado en el extremo de salida del capilar, registra la llegada de los analitos separados. Los detectores más comunes son los de absorbancia UV-Vis, pero también se utilizan detectores de fluorescencia, conductividad y espectrometría de masas.
- Autosampler: Permite la inyección automatizada y precisa de las muestras en el capilar.
- Software de control y adquisición de datos: Gestiona el sistema, procesa los datos y presenta los resultados en forma de electroferogramas.
Ventajas de la Electroforesis Capilar
A pesar de sus desafíos, la EC ofrece una serie de ventajas significativas que la han posicionado como una técnica analítica de elección en numerosos laboratorios:
- Alta Eficiencia de Separación: La principal fortaleza de la EC es su capacidad para lograr resoluciones extremadamente altas, a menudo superando a otras técnicas cromatográficas. Esto se debe al estrecho diámetro del capilar y a la ausencia de fase estacionaria, lo que minimiza la dispersión de banda.
- Rapidez: Los tiempos de análisis son generalmente muy cortos, a menudo de minutos, lo que permite un alto rendimiento de muestras.
- Bajo Consumo de Muestra y Reactivos: La EC requiere volúmenes de muestra y tampón del orden de nanolitros, lo que es invaluable cuando la muestra es escasa o costosa.
- Versatilidad: Como se mencionó, puede separar una amplia gama de compuestos, desde iones pequeños hasta macromoléculas, tanto cargadas como neutras (mediante variantes como MEKC).
- Automatización: Los sistemas de EC modernos son altamente automatizables, lo que facilita el análisis de grandes lotes de muestras y reduce la intervención manual.
- Cuantificación Precisa: Permite la cuantificación de los analitos con alta precisión y reproducibilidad.
Desventajas de la Electroforesis Capilar
Si bien la Electroforesis Capilar es una herramienta analítica formidable, no está exenta de limitaciones. La información proporcionada destaca una de las más cruciales:
Sensibilidad del Detector UV-Vis
El sistema de detección más ampliamente utilizado en Electroforesis Capilar es el de absorbancia en el rango UV-Vis. Su popularidad se debe a varias razones: es posible detectar un gran número de compuestos, especialmente aquellos que poseen cromóforos (grupos que absorben luz UV-Vis), y su coste es relativamente bajo en comparación con otros detectores. Sin embargo, su principal inconveniente, y quizás la limitación más significativa de la EC en general, es su menor sensibilidad en comparación con otros sistemas de detección más avanzados, como la fluorescencia inducida por láser (LIF) o la espectrometría de masas (MS).
La razón detrás de esta menor sensibilidad del detector UV-Vis en EC es inherente al diseño del sistema. La ley de Beer-Lambert establece que la absorbancia es directamente proporcional a la concentración del analito, al coeficiente de absortividad molar y a la longitud de la trayectoria óptica (el camino que recorre la luz a través de la muestra). En la EC, el capilar tiene un diámetro interno muy pequeño (micrómetros), lo que se traduce en una longitud de trayectoria óptica extremadamente corta en comparación con las celdas de cubeta utilizadas en espectrofotómetros convencionales o incluso con las celdas de flujo en HPLC. Esta corta longitud de trayectoria óptica limita la cantidad de luz que puede ser absorbida por los analitos, incluso si están presentes en concentraciones detectables por otras técnicas. En consecuencia, para detectar analitos con detectores UV-Vis en EC, a menudo se requieren concentraciones más altas en la muestra, lo que puede ser un problema para analitos de baja abundancia o muestras biológicas diluidas. Para superar esta limitación, se han desarrollado estrategias como la inyección de grandes volúmenes de muestra o la preconcentración en línea, pero estas pueden añadir complejidad al método.
Otras Desventajas a Considerar
Además de la sensibilidad del detector UV-Vis, existen otras consideraciones que pueden presentarse como desventajas en ciertos contextos:
- Limitaciones de Volumen de Muestra: Aunque el bajo consumo es una ventaja, también significa que la cantidad total de analito inyectado es muy pequeña. Esto puede ser un problema si la concentración del analito es extremadamente baja o si se necesita una cantidad mayor para análisis posteriores (es una técnica analítica, no preparativa).
- Efectos de Matriz: Las matrices complejas pueden interactuar con la superficie del capilar o con los analitos, afectando la reproducibilidad de los tiempos de migración y la forma de los picos. La preparación de la muestra es crucial para minimizar estos efectos.
- Calibración y Reproducibilidad: La reproducibilidad en EC puede ser un desafío, especialmente para el tiempo de migración, debido a la sensibilidad a cambios sutiles en la composición del tampón, la temperatura o la carga de la superficie del capilar. Se requiere una buena práctica de laboratorio y un control riguroso de las condiciones.
- Dificultad para Escalar: La EC es inherentemente una técnica analítica y no es fácilmente escalable para la producción a gran escala o la purificación de compuestos, a diferencia de algunas técnicas cromatográficas.
- Requerimientos de Personal Calificado: Aunque los sistemas son automatizados, el desarrollo de métodos y la resolución de problemas en EC requieren un conocimiento profundo de los principios electroforéticos y de las interacciones químico-físicas.
Comparación: Electroforesis Capilar vs. Otras Técnicas de Separación
Para comprender mejor el lugar de la EC en el panorama analítico, es útil compararla con otras técnicas de separación ampliamente utilizadas:
| Característica | Electroforesis Capilar (EC) | Cromatografía Líquida de Alta Eficiencia (HPLC) | Electroforesis en Gel (EG) |
|---|---|---|---|
| Principio de Separación | Movilidad iónica en campo eléctrico + Flujo electroosmótico. | Interacciones diferenciales entre fase móvil y estacionaria. | Movilidad iónica en matriz de gel porosa. |
| Medio de Separación | Capilar de sílice fundida (líquido). | Columna empaquetada con fase estacionaria (sólida). | Gel polimérico (sólido/gel). |
| Eficiencia de Separación | Muy alta (millones de platos teóricos). | Alta (decenas de miles de platos teóricos). | Moderada a alta (depende del gel y la técnica). |
| Velocidad de Análisis | Rápida (minutos). | Moderada a rápida (minutos a horas). | Lenta (horas a días). |
| Consumo de Muestra | Muy bajo (nL). | Bajo a moderado (µL). | Moderado a alto (µL). |
| Rango de Analitos | Iones, moléculas pequeñas, proteínas, ADN, células (cargadas y neutras). | Moléculas pequeñas, polímeros, proteínas (amplio). | Proteínas, ADN, ARN (principalmente macromoléculas). |
| Detección Común | UV-Vis (sensibilidad limitada), LIF, MS. | UV-Vis, DAD, MS, ELSD, RI. | Tinción (Coomassie, plata), fluorescencia. |
| Presión de Operación | Baja (atmosférica). | Alta (cientos de bares). | Baja (atmosférica). |
| Automatización | Alta. | Alta. | Moderada. |
| Costo de Equipamiento | Moderado a alto. | Alto. | Bajo a moderado. |
Aplicaciones de la Electroforesis Capilar
La versatilidad de la EC se refleja en su amplia gama de aplicaciones en diversas disciplinas científicas e industriales:
- Farmacéutica: Control de calidad de fármacos, análisis de pureza, separación de isómeros quirales, estudios de estabilidad, monitoreo de procesos de fabricación, caracterización de productos biofarmacéuticos (proteínas terapéuticas, anticuerpos monoclonales).
- Biotecnología y Ciencias de la Vida: Análisis de proteínas y péptidos (huellas dactilares peptídicas, pureza, modificaciones postraduccionales), secuenciación y fragmentación de ADN, análisis de polimorfismos genéticos, caracterización de oligosacáridos, estudios de interacciones biomoleculares.
- Química Clínica y Diagnóstico: Detección de biomarcadores de enfermedades, análisis de metabolitos en fluidos biológicos (sangre, orina, LCR), separación de isoenzimas, monitoreo de niveles de fármacos en sangre.
- Análisis Ambiental: Detección de contaminantes en agua y suelo, análisis de pesticidas, herbicidas y otros compuestos orgánicos e inorgánicos.
- Análisis de Alimentos y Bebidas: Determinación de aditivos, vitaminas, aminoácidos, contaminantes, autenticación de productos y control de calidad.
- Ciencias Forenses: Análisis de drogas de abuso, explosivos, tintas, fibras y fluidos biológicos para identificación y comparación.
Preguntas Frecuentes sobre la Electroforesis Capilar
¿Para qué tipo de muestras es ideal la EC?
La EC es ideal para muestras líquidas que contienen una mezcla compleja de componentes, especialmente si son iones o moléculas que pueden ser ionizadas. Es particularmente útil cuando la cantidad de muestra es limitada y se necesita una alta resolución, como en el análisis de productos farmacéuticos, muestras biológicas (suero, orina, extractos celulares) o muestras ambientales.

¿Es la Electroforesis Capilar una técnica destructiva?
Sí, la Electroforesis Capilar es una técnica analítica destructiva en el sentido de que la muestra inyectada y separada no se recupera intacta para análisis posteriores. Sin embargo, debido a los volúmenes extremadamente pequeños de muestra utilizados (nanolitros), la cantidad de material destruido es insignificante.
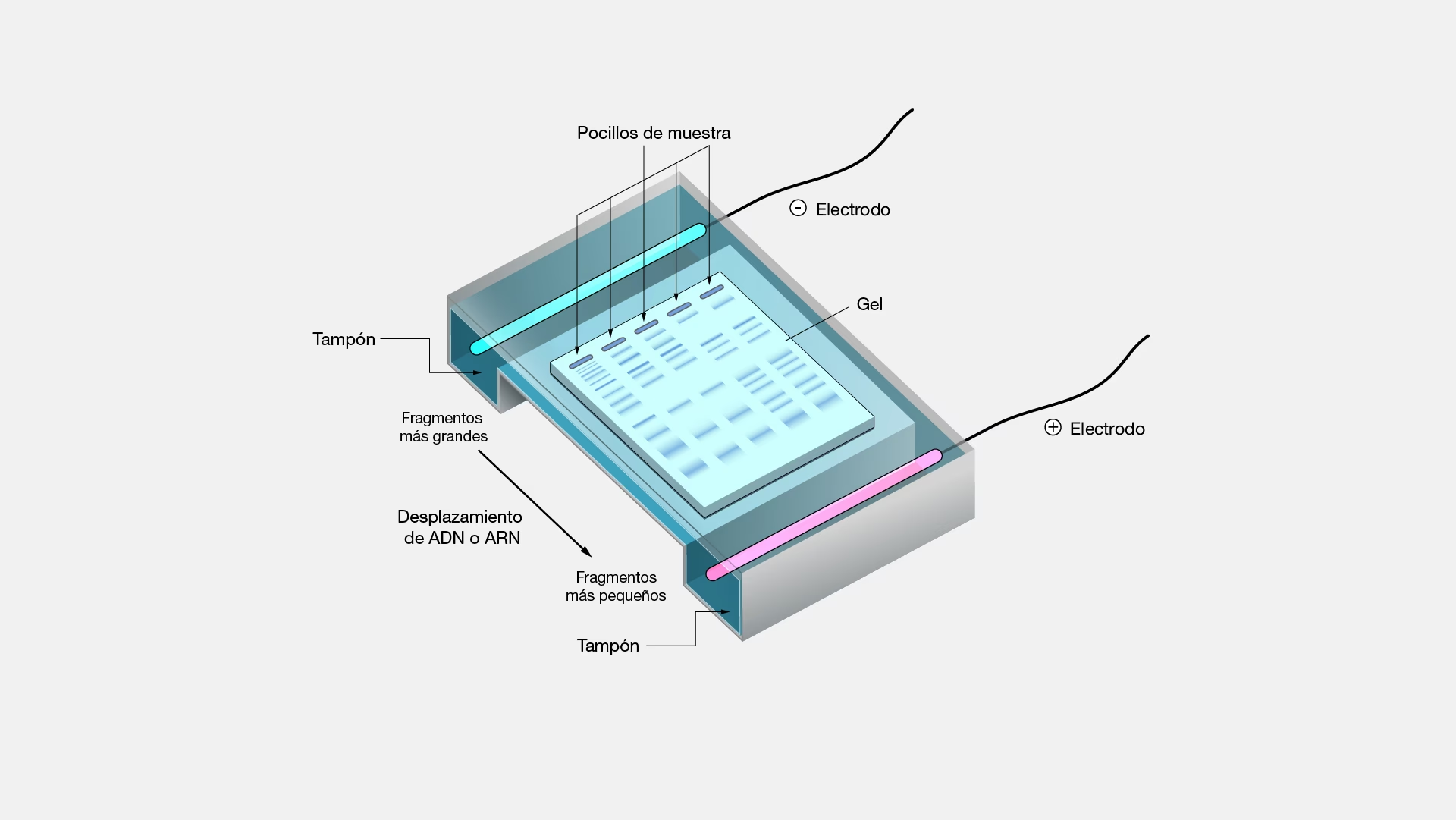
¿Qué diferencia a la EC de la electroforesis en gel tradicional?
La principal diferencia radica en el medio de separación y la escala. La EC utiliza un capilar estrecho lleno de un tampón líquido, lo que permite una disipación de calor muy eficiente y la aplicación de voltajes mucho más altos, resultando en separaciones más rápidas y de mayor resolución. La electroforesis en gel utiliza un gel polimérico como matriz de soporte, es más lenta, tiene menor resolución y consume más muestra, pero es excelente para separar macromoléculas muy grandes.
¿Se puede usar la EC para separar moléculas grandes como el ADN?
Sí, la Electroforesis Capilar es ampliamente utilizada para separar moléculas grandes como el ADN, el ARN y las proteínas. Existen variantes de la EC, como la electroforesis capilar de geles (CGE) o la electroforesis capilar de micelas (MEKC), que se adaptan para manejar diferentes tipos y tamaños de macromoléculas, incluyendo la secuenciación de ADN y el análisis de fragmentos.
¿Cuál es el factor clave que afecta la sensibilidad de detección en EC?
El factor clave que afecta la sensibilidad de detección en EC, especialmente con detectores de absorbancia UV-Vis, es la corta longitud de la trayectoria óptica del capilar. Debido al diámetro interno diminuto del capilar, la luz tiene muy poco camino para interactuar con los analitos, lo que limita la absorbancia medida y, por ende, la sensibilidad de detección. Para analitos que no absorben UV-Vis, la ausencia de un cromóforo también es un factor limitante, requiriendo derivatización o el uso de detectores más específicos como la espectrometría de masas.
En conclusión, la Electroforesis Capilar representa un pilar fundamental en la química analítica moderna. Su capacidad para ofrecer separaciones de alta resolución en tiempos reducidos y con un consumo mínimo de muestra la convierte en una herramienta invaluable en una multitud de campos. Aunque la sensibilidad de sus detectores UV-Vis puede ser una limitación, los continuos avances en la instrumentación y en las estrategias de mejora de la señal están ampliando constantemente sus horizontes, consolidando su posición como una de las técnicas más potentes y prometedoras para el análisis de mezclas complejas.
Si quieres conocer otros artículos parecidos a Electroforesis Capilar: Una Mirada Profunda puedes visitar la categoría Cabello.