08/10/2018
Los capilares, a menudo subestimados por su tamaño microscópico, son, sin embargo, los vasos sanguíneos más cruciales de nuestro cuerpo. Constituyen una intrincada red que se extiende por cada órgano y tejido, actuando como los puntos de intercambio vital donde la sangre entrega sus preciados recursos y recoge los desechos. Imagina una vasta autopista que se ramifica en incontables callejones estrechos y eficientes, cada uno llegando directamente a la puerta de cada célula. Esa es la esencia de la función capilar: una entrega de “víveres” y una recolección de “basura” que ocurre incesantemente en cada rincón de nuestro organismo.
¿Qué son los Capilares y Cuáles son sus Características Principales?
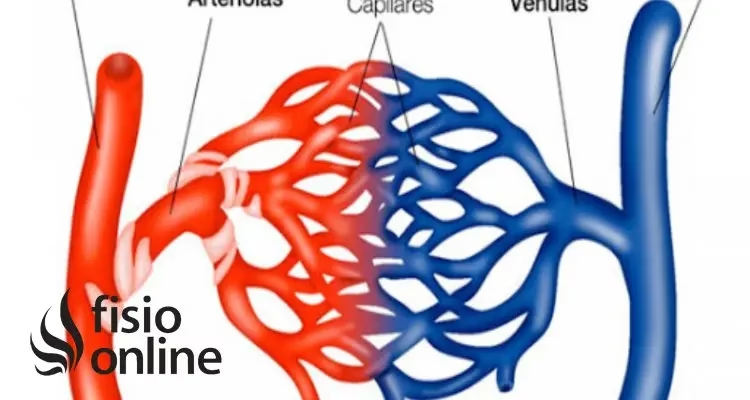
Los capilares son vasos sanguíneos increíblemente delicados y delgados, con paredes de apenas una célula de grosor. Esta característica es fundamental, ya que permite que los nutrientes, el oxígeno y otras sustancias pasen fácilmente desde la sangre hacia las células circundantes, y que los productos de desecho, como el dióxido de carbono, se muevan en la dirección opuesta, desde las células hacia la sangre para ser eliminados.
- Delgadez Extrema: Sus paredes son tan finas que facilitan la difusión rápida y eficiente de gases y moléculas.
- Red Extensa: Se encuentran en todo el cuerpo, formando redes densas que aseguran que ninguna célula esté lejos de un suministro de sangre.
- Función de Intercambio: Son los sitios primarios donde ocurre el intercambio de oxígeno, nutrientes, hormonas y desechos entre la sangre y los tejidos.
- Conexión Arterial y Venosa: Actúan como puentes entre las arteriolas (pequeñas arterias) y las vénulas (pequeñas venas), completando el circuito sanguíneo.
Existen diferentes tipos de capilares, que varían en su estructura para adaptarse a las necesidades específicas de los tejidos donde se encuentran. Aunque la información detallada sobre sus formas específicas va más allá del alcance de este artículo, es importante saber que esta diversidad estructural les permite llevar a cabo una amplia gama de funciones vitales en distintos sistemas orgánicos.
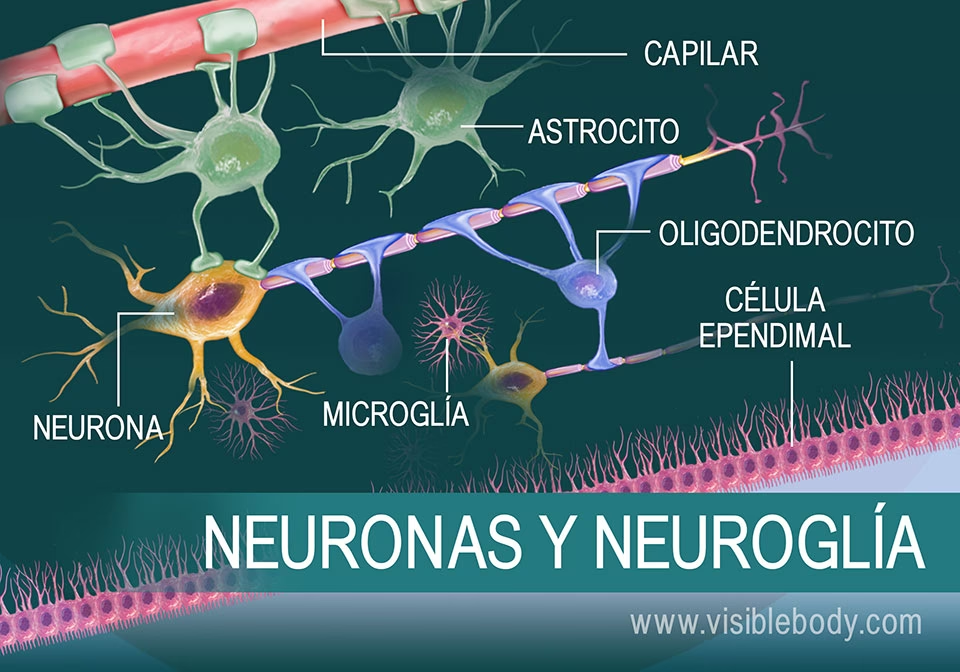
Los Capilares en el Sistema Nervioso: La Intrincada Barrera Hematoencefálica
Los capilares en el sistema nervioso central (SNC) poseen características únicas que los distinguen de los capilares en otras partes del cuerpo. Aquí, forman una estructura altamente especializada conocida como la barrera hematoencefálica (BHE o BBB, por sus siglas en inglés), un sistema de protección vital que aísla el delicado entorno cerebral de las fluctuaciones y posibles amenazas presentes en la sangre circulante. Esta barrera es fundamental para mantener la homeostasis del SNC, controlando estrictamente qué sustancias pueden entrar al cerebro.
Desarrollo y Estructura de la Barrera Hematoencefálica
La formación de la BHE en el SNC de los mamíferos es un proceso complejo. Los capilares cerebrales se desarrollan a partir de cordones sólidos de células endoteliales que, con el tiempo, forman una luz (espacio interior) y aumentan su calibre. Nuevos cordones brotan de capilares más maduros, invadiendo el tejido nervioso en desarrollo. Estas estructuras recién formadas están separadas de las neuronas adyacentes por una membrana basal y son progresivamente envueltas por astrocitos residentes.
El crecimiento más rápido de los capilares coincide con períodos de proliferación de células gliales y desarrollo dendrítico neuronal, lo que sugiere una estrecha relación entre la vascularización y el crecimiento cerebral. Se cree que la densidad de los capilares cerebrales en diversas regiones del SNC está directamente correlacionada con la actividad metabólica y el consumo de oxígeno inherente a cada área específica. Este desarrollo vascular es crucial; las deficiencias en el suministro sanguíneo durante las etapas críticas del desarrollo pueden comprometer seriamente el desarrollo del SNC, ya que no se desarrollan suministros sanguíneos colaterales.

A diferencia de la mayoría de los capilares periféricos, los capilares cerebrales no son fenestrados (no tienen poros), lo que los hace menos permeables. La característica distintiva y principal de la barrera hematoencefálica reside en las uniones estrechas (zonulae occludentes) entre las células endoteliales. Estas uniones son tan herméticas que restringen significativamente el paso de moléculas, incluso iones pequeños, lo que les confiere una alta resistencia eléctrica. Históricamente, se pensó que los procesos de los astrocitos formaban la barrera restrictiva, pero estudios de microscopía electrónica de la década de 1950 demostraron que la verdadera barrera a la difusión se encuentra en estas uniones estrechas entre las células endoteliales.
El Rol de los Astrocitos en la Barrera Hematoencefálica: ¿Inductores o Moduladores?
Aunque los astrocitos no forman directamente la barrera física, su papel en la inducción y el mantenimiento de las propiedades de la BHE ha sido objeto de intensa investigación y debate. Desde principios del siglo XX, se reconoció que las terminaciones astrocíticas, llamadas “pies terminales” (end-feet), rodeaban los capilares cerebrales. Esta observación llevó a la especulación, errónea como se mencionó, de que los astrocitos formaban la base física de la BHE.
Sin embargo, estudios más recientes, particularmente con cocultivos de células endoteliales y astrocitos, han demostrado que los astrocitos son cruciales para la inducción y el mantenimiento de las uniones estrechas entre las células endoteliales de la BHE. Se ha sugerido que los astrocitos proporcionan factores tróficos que inducen las propiedades de la barrera. A continuación, se presenta un análisis de la evidencia que apoya y refuta la participación de los astrocitos en la inducción y el mantenimiento de la BHE:
Evidencia a Favor del Rol de los Astrocitos
- Inducción de Uniones Estrechas: Cuando las células endoteliales se cultivan solas, sus uniones estrechas son fragmentarias. Al cocultivarlas con astrocitos, la longitud, anchura y complejidad de estas uniones aumentan, asemejándose a las observadas in vivo. Si se sustituyen los astrocitos por otros tipos celulares, como fibroblastos, las uniones permanecen fragmentarias.
- Cambios Ultrastructurales: Cultivar células endoteliales con medios condicionados por astrocitos ha mostrado características ultraestructurales indicativas de la síntesis e inserción de componentes de las uniones estrechas en la membrana plasmática.
- Resistencia Eléctrica: Los cocultivos de células endoteliales y astrocitos muestran un aumento en la resistencia eléctrica transfiltro, indicando una menor conductancia y una barrera más restrictiva.
- Expresión de Enzimas Específicas: La actividad de la gamma-glutamil transpeptidasa (γ-GT), un marcador específico de las células endoteliales del SNC, se induce en células endoteliales cerebrales cuando se cocultivan con astrocitos. Esta actividad se suprime en ausencia de astrocitos y se reexpresa al añadirlos.
- Transporte de Nutrientes: La adición de astrocitos a cultivos de células endoteliales aumenta la incorporación de aminoácidos neutros por parte de estas últimas.
- Regulación de Transportadores: La expresión de la isoforma GLUT-1 del transportador de glucosa, un marcador específico de la barrera, se reduce en cultivos de células endoteliales cerebrales en ausencia de factores tróficos derivados del cerebro o de astrocitos, y se recupera con su presencia. Esto subraya el papel de los astrocitos en el transporte de nutrientes esencial para el cerebro.
- Angiogénesis: Los astrocitos de tipo I pueden inducir angiogénesis (formación de nuevos vasos sanguíneos) y algunas propiedades de la BHE en células endoteliales de origen no neural. La expresión del factor de crecimiento endotelial vascular (VEGF), un factor de crecimiento angiogénico, se induce y regula al alza en glioblastomas malignos, lo que sugiere un papel en la angiogénesis cerebral embrionaria.
- Experimentos de Trasplante: La formación de la BHE depende en gran medida del entorno del SNC. Capilares de tejido sistémico trasplantados al SNC desarrollan una BHE. La inyección de cultivos primarios de astrocitos en la cámara anterior del ojo o en la membrana corioalantoidea del pollo indujo una barrera de permeabilidad en los capilares de estos tejidos que de otro modo carecerían de ella.
Evidencia que Cuestiona o Matiza el Rol Inductor de los Astrocitos
- Variaciones en Especies: En algunos elasmobranquios, los capilares cerebrales están envueltos por astrocitos, pero sus células endoteliales no expresan uniones estrechas, sino poros abiertos que son permeables a moléculas grandes. Esto sugiere que los astrocitos no siempre garantizan la formación de uniones estrechas.
- Capilares Fenestrados con Astrocitos: Los astrocitos también se encuentran en estrecha asociación con los pituicitos, sin embargo, el endotelio en el lóbulo neural es fenestrado y permeable a ciertos tintes.
- Barrera Funcional sin Astrocitos: Células endoteliales clonadas in vitro pueden establecer una barrera funcionalmente restrictiva con una resistencia relativamente alta (hasta 700-800 ohm.cm²), incluso sin la presencia de astrocitos. Sin embargo, la diferenciación morfológica y la inducción de proteínas específicas de la BHE sí parecen ser influenciadas por los astrocitos.
- Resultados de Injertos Mixtos: Los astrocitos no forman injertos ricamente vascularizados cuando se inyectan solos. Los vasos asociados a injertos de astrocitos no cambian su ultraestructura para parecerse a capilares cerebrales. Además, los injertos de astrocitos pueden provocar una respuesta inflamatoria, lo que complica la interpretación de los resultados sobre la permeabilidad de los vasos.
- Evolución de la Barrera: Las barreras más tempranas en la evolución (como en los moluscos cefalópodos) se formaban entre las células gliales y no entre las células endoteliales. Se sugiere que, en los vertebrados, la barrera ha evolucionado de las células gliales a las endoteliales, quizás para permitir una mayor complejidad y control del entorno intersticial del SNC por parte de las células gliales, superponiéndose a una barrera que impedía grandes y rápidos cambios en la sangre.
A pesar de la abundante evidencia, el papel preciso de los astrocitos perivasculares en la inducción y el mantenimiento del endotelio cerebral como barrera estructural y funcional aún no se ha dilucidado completamente. Es claro que la inducción de la BHE ocurre en ciertas etapas del desarrollo y hay evidencia circunstancial de que los astrocitos pueden ser responsables, pero la situación sigue siendo compleja.
Funciones Adicionales de los Astrocitos en la Homeostasis del SNC
Más allá de su interacción con la BHE, los astrocitos desempeñan una multitud de funciones críticas en la homeostasis del SNC, disipando la antigua idea de que eran meros "pegamentos" estructurales para las neuronas. Su rol es activo y dinámico:
- Regulación del K+ Extracelular: Una de las primeras funciones propuestas para los astrocitos fue el control del potasio extracelular (amortiguación espacial de K+), eliminando localmente el K+ liberado por las neuronas activas.
- Respuesta y Reparación de Daños: Reaccionan y reparan el daño neural inducido por traumatismos físicos o agresiones químicas.
- Captación de Neurotransmisores: Poseen sistemas de captación muy potentes para una variedad de neurotransmisores de aminoácidos (como glutamato, glicina, taurina y GABA) y monoaminas (como serotonina). Esto es crucial para terminar la señalización sináptica y prevenir la excitotoxicidad.
- Regulación del Metabolismo del Glucógeno: Juegan un papel en el almacenamiento y liberación de glucógeno, una fuente de energía para las neuronas.
- Interacciones con Neuronas en Desarrollo: Son fundamentales en el desarrollo del SNC, guiando la migración de los cuerpos celulares neuronales y el crecimiento de los axones. Las moléculas de adhesión en su superficie promueven la motilidad del cono de crecimiento neuronal y proporcionan señales direccionales.
- Receptores de Neurotransmisores: Poseen una amplia gama de receptores de neurotransmisores, lo que les permite responder a las mismas señales que actúan sobre las neuronas, integrando y modulando la actividad sináptica.
| Evidencia a Favor | Evidencia que Matiza / Cuestiona |
|---|---|
| Inducen uniones estrechas más complejas y funcionales en cocultivos. | Algunas especies con astrocitos no tienen uniones estrechas en sus capilares cerebrales. |
| Aumentan la resistencia eléctrica transendotelial en vitro. | Células endoteliales clonadas pueden formar una barrera funcional sin astrocitos. |
| Inducen la expresión de enzimas y transportadores específicos de la BHE (ej. γ-GT, GLUT-1). | Capilares fenestrados pueden estar asociados con astrocitos (ej. lóbulo neural). |
| Favorecen la angiogénesis y el desarrollo de propiedades de BHE en trasplantes. | Resultados de injertos de astrocitos pueden ser afectados por inflamación o falta de cambio ultraestructural. |
| Regulan el transporte de nutrientes y la captación de aminoácidos por las células endoteliales. | La evolución de la barrera sugiere un cambio de barreras gliales a endoteliales. |
Preguntas Frecuentes sobre los Capilares y la Barrera Hematoencefálica
¿Cuál es la función principal de los capilares?
La función principal de los capilares es facilitar el intercambio de sustancias entre la sangre y los tejidos del cuerpo. Actúan como los “puntos de entrega y recolección” donde el oxígeno y los nutrientes pasan de la sangre a las células, y el dióxido de carbono y otros productos de desecho son recogidos de las células para ser transportados y eliminados.
¿Qué hace que los capilares sean tan eficientes para el intercambio?
Su eficiencia se debe principalmente a sus paredes extremadamente delgadas, que suelen tener solo una célula de grosor. Esta delgadez permite una difusión rápida y fácil de gases, líquidos y nutrientes a través de sus paredes, directamente hacia y desde las células circundantes.
¿Qué es la barrera hematoencefálica y por qué es tan importante?
La barrera hematoencefálica es una estructura altamente selectiva formada por los capilares cerebrales y células gliales, que protege el cerebro de sustancias potencialmente dañinas en la sangre. Es crucial porque mantiene un ambiente estable y controlado en el cerebro, esencial para el funcionamiento neuronal adecuado, y previene la entrada de toxinas, patógenos y fluctuaciones químicas que podrían alterar la actividad cerebral.
¿Los astrocitos forman la barrera hematoencefálica?
Originalmente se pensó que los astrocitos formaban la barrera física de la BHE. Sin embargo, estudios más detallados han demostrado que la barrera restrictiva principal está formada por las uniones estrechas entre las células endoteliales de los capilares cerebrales. Los astrocitos, no obstante, desempeñan un papel crucial en la inducción, modulación y mantenimiento de las propiedades de estas uniones estrechas y de la funcionalidad general de la BHE, liberando factores tróficos y participando en la homeostasis del SNC.
¿Qué ocurre si la barrera hematoencefálica se daña?
Un daño en la barrera hematoencefálica puede tener consecuencias graves, ya que permitiría el paso de sustancias que normalmente estarían excluidas del cerebro, incluyendo toxinas, patógenos y células inmunes. Esto puede llevar a inflamación cerebral, infecciones, disfunción neuronal y diversas enfermedades neurológicas.
En resumen, los capilares son componentes fundamentales de nuestro sistema circulatorio, orquestando el delicado balance de intercambio de sustancias necesario para la vida celular. En el cerebro, su especialización en la formación de la barrera hematoencefálica es un testimonio de la complejidad y la maravilla de la biología humana, protegiendo nuestro centro de control más vital. Comprender su función no solo nos da una visión más profunda de nuestro cuerpo, sino que también resalta la increíble eficiencia con la que la naturaleza ha diseñado nuestros sistemas internos.
Si quieres conocer otros artículos parecidos a Los Capilares: Vías Cruciales del Cuerpo puedes visitar la categoría Cabello.
