01/04/2018
La determinación del punto de fusión es una técnica fundamental en el laboratorio, especialmente en la química orgánica. Permite no solo identificar sustancias desconocidas, sino también, y quizás lo más crucial, evaluar su pureza. Una sustancia pura posee un punto de fusión bien definido y estrecho, mientras que la presencia de impurezas suele provocar un descenso del punto de fusión y un rango de fusión más amplio. Entre los diversos métodos disponibles, el método del tubo capilar se destaca por su simplicidad, eficacia y bajo costo, siendo ampliamente utilizado tanto en entornos educativos como de investigación.
¿Qué es el Punto de Fusión?
El punto de fusión de una sustancia cristalina se define como la temperatura a la cual cambia de estado sólido a estado líquido bajo una presión determinada. Es una propiedad física característica e intensiva, lo que significa que no depende de la cantidad de sustancia. Para una sustancia pura, este proceso ocurre en un rango de temperatura muy estrecho, a menudo de 0.5 a 1.0 °C. Las impurezas, al interferir con la red cristalina del sólido, generalmente disminuyen el punto de fusión y amplían el rango en el que ocurre la fusión.
El Método Capilar: Un Procedimiento Detallado
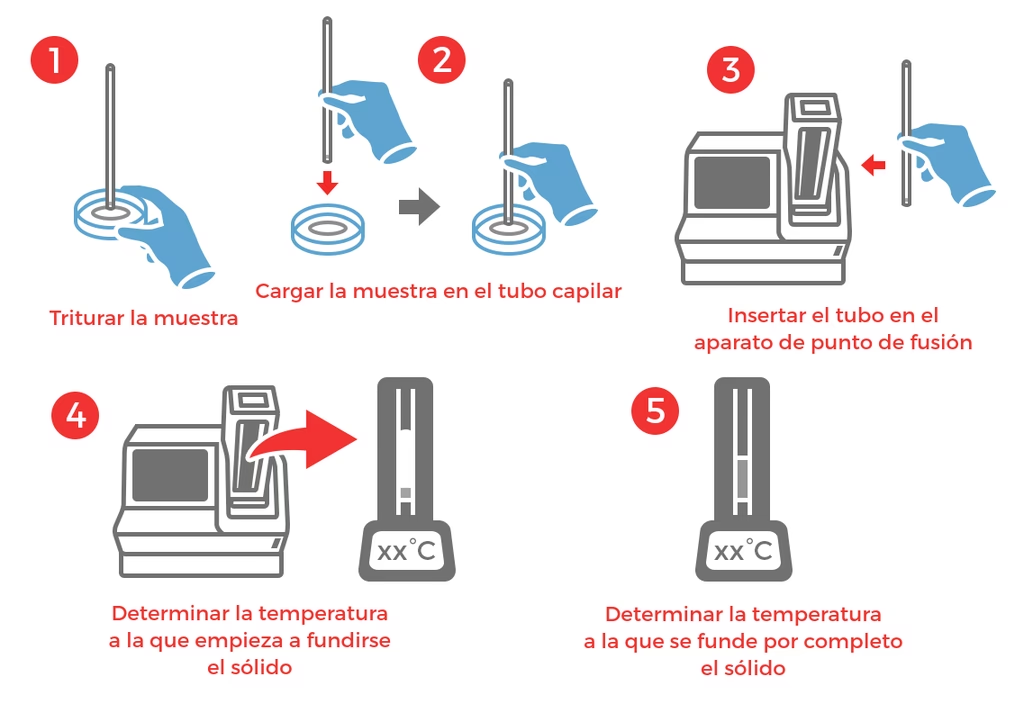
El método capilar es el procedimiento más común y accesible para determinar el punto de fusión en el laboratorio. Se basa en calentar lentamente una pequeña cantidad de la muestra dentro de un tubo capilar de vidrio delgado, observando el momento exacto en que comienza y termina la fusión.
Materiales y Equipos Necesarios:
- Muestra sólida a analizar (finamente pulverizada).
- Tubos capilares de vidrio de paredes finas, cerrados por un extremo.
- Mechero Bunsen o quemador de alcohol (para cerrar capilares si es necesario).
- Mortero y mano (para pulverizar la muestra).
- Espátula pequeña.
- Termómetro de precisión (con rango adecuado, por ejemplo, de 0 a 300 °C).
- Aparato para la determinación del punto de fusión (Tubo de Thiele o Aparato Fisher Johns).
- Fuente de calor (placa calefactora, manta calefactora o mechero para el Tubo de Thiele).
- Aceite de silicona o parafina (para el Tubo de Thiele).
- Pinzas o soporte universal.
Pasos del Procedimiento:
1. Preparación del Tubo Capilar:
Si no se dispone de tubos capilares pre-cerrados, se puede cerrar un extremo de un tubo capilar abierto haciéndolo girar suavemente sobre la llama de un mechero Bunsen. El vidrio se ablandará y sellará el orificio. Es crucial asegurarse de que el cierre sea completo y liso para evitar que la muestra se caiga.
2. Preparación de la Muestra:
La muestra sólida debe estar completamente seca y finamente pulverizada. Si la muestra es un sólido grande o cristalino, se debe moler cuidadosamente en un mortero hasta obtener un polvo fino. Esto asegura un empaquetamiento uniforme y una transferencia de calor eficiente dentro del capilar.
3. Llenado del Tubo Capilar:
Se introduce una pequeña cantidad de la muestra pulverizada en el extremo abierto del tubo capilar. La forma más común de hacer esto es golpear suavemente el extremo cerrado del capilar sobre una superficie dura (como una mesa) o hacer vibrar el capilar para que la muestra se asiente en el fondo. Se busca una columna de muestra compacta de aproximadamente 2-4 mm de altura. Un empaquetamiento adecuado es crucial; si la muestra está demasiado suelta, la fusión puede ser errática; si está demasiado compacta, la lectura de la temperatura puede no ser precisa.
4. Configuración del Aparato de Fusión:
Existen dos configuraciones principales para calentar la muestra y determinar el punto de fusión:
a) Uso del Tubo de Thiele:
El Tubo de Thiele es un aparato de vidrio con una forma peculiar que permite la convección del líquido calentador (generalmente aceite de silicona o parafina) para asegurar un calentamiento uniforme. Se llena el tubo de Thiele con el líquido hasta el nivel indicado. El termómetro se sujeta de manera que el bulbo esté al mismo nivel que la muestra en el capilar, y el capilar se adhiere al termómetro (por ejemplo, con un pequeño anillo de goma o hilo) de modo que la muestra esté visible y alineada con el bulbo del termómetro. Se calienta el brazo lateral del Tubo de Thiele con un mechero Bunsen de forma gradual. El líquido caliente ascenderá por un lado y descenderá por el otro, creando una corriente de convección que calienta uniformemente el termómetro y el capilar.
b) Uso del Aparato Fisher Johns (o similar):
Este aparato es una placa metálica calentada eléctricamente, generalmente con un control de temperatura y una lente de aumento. Se coloca una pequeña cantidad de la muestra sobre la placa calentada, se baja el termómetro sobre la muestra y se observa a través de la lente. Estos aparatos suelen ser más precisos y fáciles de controlar que el Tubo de Thiele, con una escala que generalmente va de 0 a 300 °C.
5. Calentamiento y Observación:
El calentamiento debe ser lento y controlado, especialmente a medida que la temperatura se acerca al punto de fusión esperado de la sustancia. Una velocidad de calentamiento de 1-2 °C por minuto es ideal en las proximidades del punto de fusión. Se observa atentamente la muestra a través de la lupa o directamente. Se registran dos temperaturas:
- Temperatura inicial de fusión: El momento en que la primera gota de líquido aparece en la muestra o cuando la muestra comienza a compactarse o volverse transparente.
- Temperatura final de fusión: El momento en que toda la muestra se ha convertido en líquido transparente.
Este rango de temperaturas es el punto de fusión observado. Para una sustancia pura, este rango debe ser muy estrecho.
6. Repetición:
Es recomendable realizar al menos dos o tres determinaciones para asegurar la consistencia y precisión de los resultados.
Factores que Afectan la Precisión del Punto de Fusión
- Velocidad de Calentamiento: Un calentamiento demasiado rápido puede llevar a lecturas erróneas, ya que el termómetro puede no registrar la temperatura real de la muestra en el momento de la fusión.
- Tamaño de la Muestra: Una columna de muestra demasiado grande puede causar un calentamiento no uniforme.
- Compactación de la Muestra: Una muestra mal empaquetada puede fundirse de manera irregular.
- Pureza del Termómetro: El termómetro debe estar calibrado y su bulbo completamente sumergido en el medio de calentamiento para una lectura precisa.
- Impurezas: La presencia de impurezas siempre disminuirá el punto de fusión y aumentará el rango de fusión.
- Descomposición: Algunas sustancias se descomponen antes de fundirse, lo que puede observarse como un oscurecimiento o burbujeo. En estos casos, se registra la temperatura de descomposición junto con la observación.
Comparación de Aparatos para Punto de Fusión
| Característica | Tubo de Thiele | Aparato Fisher Johns (o similar) |
|---|---|---|
| Principio de Calentamiento | Convección de líquido (aceite/parafina) | Placa calefactora eléctrica |
| Control de Temperatura | Manual, con mechero | Electrónico, más preciso |
| Seguridad | Riesgo de quemaduras con aceite caliente, vapores | Menor riesgo de quemaduras, sin vapores (generalmente) |
| Costo | Bajo | Moderado a alto |
| Precisión | Buena, pero depende de la habilidad del operador | Muy buena, reproducible |
| Mantenimiento | Limpieza del aceite, cambio ocasional | Calibración, limpieza de la placa |
| Uso Común | Laboratorios educativos, básica | Investigación, control de calidad, avanzada |
Preguntas Frecuentes (FAQ)
¿Por qué es tan importante determinar el punto de fusión?
Es crucial por dos razones principales: la identificación y la determinación de la pureza. Cada sustancia cristalina pura tiene un punto de fusión característico. Si se desconoce una sustancia, su punto de fusión puede compararse con valores conocidos para su identificación. Además, un rango de fusión estrecho (idealmente de 0.5 a 1.0 °C) es un fuerte indicador de la pureza de la muestra; un rango amplio o un punto de fusión bajo sugieren la presencia de impurezas.
¿Qué tipo de muestras se pueden analizar con el método capilar?
Este método es adecuado para la mayoría de los sólidos cristalinos que tienen un punto de fusión definido y que no se descomponen significativamente antes de fundir. Es ampliamente utilizado para compuestos orgánicos e inorgánicos.
¿Qué hago si mi muestra se descompone antes de fundir?
Algunas sustancias se descomponen (cambian químicamente, a menudo oscureciéndose o burbujeando) antes de alcanzar su punto de fusión. En estos casos, se debe registrar la temperatura a la cual comienza la descomposición junto con la observación de que la muestra no fundió limpiamente. Esto indica que el punto de fusión no puede determinarse por este método y se necesitarían otras técnicas.
¿Cómo puedo asegurar la mayor precisión en mi determinación?
Para maximizar la precisión, asegúrate de que la muestra esté seca y finamente pulverizada, llena el capilar con una altura de muestra adecuada (2-4 mm) y bien compactada. Utiliza un termómetro calibrado y, lo más importante, controla la velocidad de calentamiento a 1-2 °C por minuto cuando te acerques al punto de fusión esperado. Repite la determinación al menos dos veces.
¿Es el método capilar adecuado para todas las sustancias?
No, no es adecuado para sustancias que subliman (pasan directamente de sólido a gas) antes de fundir, para sustancias que se descomponen extensamente, o para polímeros que no tienen un punto de fusión definido sino un rango de ablandamiento.
En conclusión, el método capilar para la determinación del punto de fusión es una técnica de laboratorio invaluable. A pesar de su aparente simplicidad, requiere atención al detalle y un procedimiento cuidadoso para obtener resultados precisos y confiables. Dominar esta técnica es un paso esencial para cualquier estudiante o profesional en el campo de la química, proporcionando información crítica sobre la identidad y la pureza de las sustancias.
Si quieres conocer otros artículos parecidos a Determinación del Punto de Fusión por Método Capilar puedes visitar la categoría Cabello.
