24/09/2018
Los riñones son órganos vitales encargados de filtrar la sangre, eliminar los productos de desecho y mantener el equilibrio de líquidos y electrolitos en el cuerpo. Dentro de cada riñón, la unidad funcional básica es la nefrona, y una de las estructuras más cruciales de la nefrona es el glomérulo. El glomérulo es una intrincada red de capilares que actúa como el principal sitio de filtración. Pero, ¿cómo logra esta estructura tan compleja su función de filtro? La respuesta reside en la membrana capilar glomerular, una barrera altamente especializada y selectiva que permite el paso de agua y pequeños solutos, mientras retiene proteínas y células sanguíneas. Comprender la función de esta membrana es fundamental para entender la fisiología renal y las patologías que la afectan.
- La Glomérulo: Un Filtro Sofisticado del Cuerpo
- Principios Fundamentales de la Filtración Glomerular: Las Fuerzas de Starling
- El Glomérulo como un Modelo de Tubo Único: Primeras Aproximaciones
- El Desafío del Tamaño: Teoría de los Poros y Permeabilidad a Solutos
- La Membrana Capilar Glomerular: Una Barrera Compuesta por Tres Capas
- El Papel Crucial de la Carga: La Selectividad Iónica de la Membrana
- El Descubrimiento de la Glucocáliz Endotelial: La Pieza Clave del Rompecabezas
- Aplicaciones Clínicas y Disfunciones Renales: Entendiendo la Enfermedad
- Preguntas Frecuentes sobre la Membrana Glomerular
- ¿Qué es la membrana capilar glomerular?
- ¿Cuáles son las tres capas principales de la barrera de filtración glomerular?
- ¿Cómo influyen las fuerzas de Starling en la filtración glomerular?
- ¿Qué papel juega la glucocáliz en la filtración glomerular?
- ¿Por qué es importante entender la función de la membrana glomerular?
- Conclusión
La Glomérulo: Un Filtro Sofisticado del Cuerpo
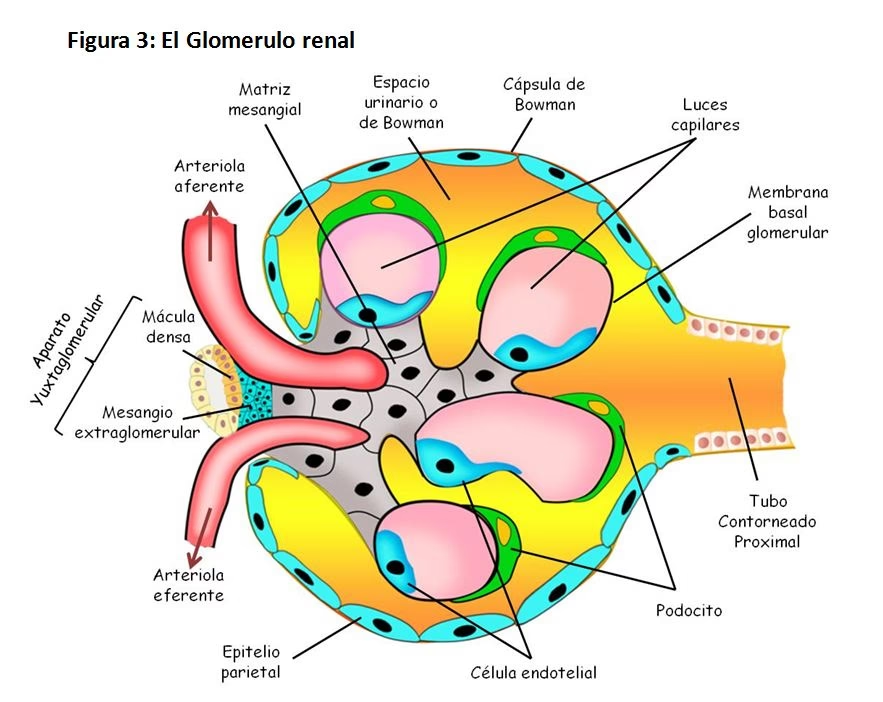
El glomérulo no es simplemente un conjunto de capilares; es una red densa y ramificada de capilares fenestrados, que se originan de una única arteriola aferente y convergen en una arteriola eferente. Esta disposición única permite un control preciso del flujo sanguíneo y la presión dentro del glomérulo. La filtración del plasma sanguíneo ocurre a través de estos capilares hacia el espacio de Bowman, un compartimento que rodea el glomérulo y cuya cavidad se vacía en el túbulo proximal, el inicio del sistema tubular de la nefrona.
El flujo sanguíneo capilar dentro del glomérulo es modulado por células especializadas llamadas pericitos. Estas células, cuya contracción está controlada hormonalmente (por ejemplo, por la angiotensina II), tienen la capacidad de reducir sustancialmente el área capilar disponible para la filtración. Esta modulación es un mecanismo clave para regular la tasa de filtración glomerular y adaptarla a las necesidades fisiológicas del organismo, asegurando que el riñón pueda ajustar su capacidad de filtrado en respuesta a diversas condiciones.
Principios Fundamentales de la Filtración Glomerular: Las Fuerzas de Starling
Un avance crítico en la comprensión de la función glomerular provino de la idea de que este complejo ovillo capilar podía representarse como un solo tubo. Este modelo simplificado permitió conceptualizar la filtración glomerular como un proceso impulsado por fuerzas hidrostáticas y oncóticas, conocidas como las fuerzas de Starling. La tasa de cambio en el flujo de plasma capilar glomerular (QGC) se consideró proporcional a la fuerza de ultrafiltración local (PUF), de acuerdo con una permeabilidad hidráulica, conocida como Kf.
La ecuación fundamental que describe este proceso es:
dQGC/dX = - Kf * PUF
Donde PUF es la fuerza de ultrafiltración neta, determinada por la siguiente relación:
PUF = (PGC - PT) - πGC
En esta ecuación, PGC representa la diferencia de presión hidrostática entre el capilar glomerular y el túbulo proximal temprano, PT es la presión hidrostática en el espacio de Bowman, y πGC es la fuerza oncótica (presión osmótica generada por las proteínas) dentro del capilar glomerular. La fuerza oncótica, a su vez, se determina a partir de la concentración de proteínas capilares (CGC) utilizando la ecuación de Landis-Pappenheimer, que considera la relación no lineal entre la concentración de proteínas y la presión oncótica. La comprensión de estas fuerzas es esencial para analizar cómo el líquido se mueve a través de la membrana y cómo los cambios en estas presiones pueden afectar la función renal.
El Glomérulo como un Modelo de Tubo Único: Primeras Aproximaciones
El modelo de “tubo único” fue un hito que permitió a los investigadores calcular la tasa de filtración glomerular de una sola nefrona (SNGFR) integrando el flujo de plasma a lo largo del capilar. Este modelo se validó con datos experimentales obtenidos de estudios de micropunción en ratas, que revelaron que la concentración de proteínas en la arteriola eferente era tal que la presión oncótica al final del capilar y la presión hidrostática capilar glomerular eran iguales. Cuando prevalece este equilibrio de presión de filtración, el modelo indica que la SNGFR es proporcional al flujo de plasma de la arteriola aferente.
Este modelo sirvió como marco para estudios posteriores sobre la disfunción renal. Por ejemplo, en la insuficiencia renal aguda isquémica, se observó que la disminución de la SNGFR se debía a una reducción en el flujo de plasma glomerular (QGC), sin cambios en la permeabilidad hidráulica (Kf). En la hipertrofia renal, el aumento de la SNGFR fue paralelo a un incremento en QGC. Además, se descubrió que la nefrotoxicidad de ciertos medicamentos, como el antibiótico gentamicina, incluía una disminución en Kf. Estos estudios también revelaron que el impacto de las proteínas séricas en la filtración glomerular es más complejo que un simple cambio en la presión oncótica; por ejemplo, en la hiperproteinemia, hubo un aumento en Kf, lo que atenuaría una disminución esperada en SNGFR, mientras que una baja concentración de proteínas séricas disminuía Kf. Esto demuestra la intrincada interacción de factores que regulan la función glomerular.
El Desafío del Tamaño: Teoría de los Poros y Permeabilidad a Solutos
Un capítulo importante en el estudio de la función glomerular se centró en la filtración de solutos en relación con su tamaño. La idea seminal se atribuye a Pappenheimer y Renkin, quienes concibieron el transporte de solutos microvasculares como el paso de esferas duras a través de cilindros rígidos durante el flujo laminar. Este enfoque teórico permitió predecir cómo diferentes moléculas serían filtradas basándose en su tamaño efectivo y la geometría de los poros de la membrana.
Los estudios de Verniory et al. aplicaron este análisis a la depuración renal de una gama de tamaños de polivinilpirrolidona (PVP) infundida en perros, estimando un radio de poro de 5 nm. Posteriormente, Chang et al. realizaron un examen meticuloso de la filtración de dextrano neutro en el riñón de rata, revelando que no había restricción para solutos con un radio inferior a 1.8 nm, y una restricción completa por encima de 4.4 nm. Para solutos con un radio superior a 2.8 nm, sus cálculos de modelo arrojaron una estimación consistente para el radio del poro de aproximadamente 5 nm. Esto proporcionó evidencia empírica sólida para la existencia de una barrera de tamaño en la membrana glomerular.
Sin embargo, el modelo de poro único resultó ser limitado para explicar la complejidad de algunas enfermedades renales. En la enfermedad renal proteinúrica, por ejemplo, se observó una disminución de la filtración para solutos más pequeños y una filtración mejorada de moléculas más grandes. Esto llevó a la postulación de que en el riñón dañado aparecía un poro adicional (o una distribución de poros) responsable de la depuración de moléculas grandes, lo que complicaba la visión simplista de un filtro uniforme.
La Membrana Capilar Glomerular: Una Barrera Compuesta por Tres Capas
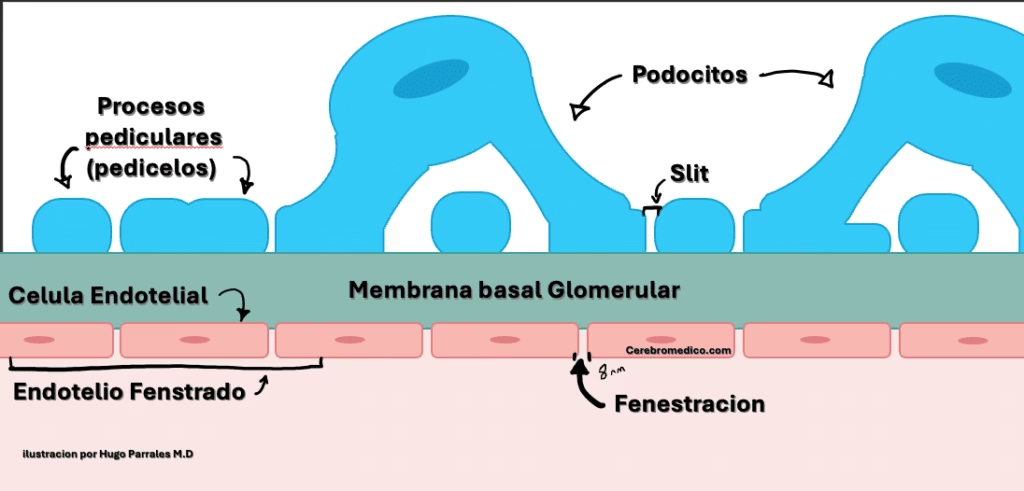
A pesar de la elegancia de los modelos de poros, finalmente se reconoció que la barrera glomerular a la transferencia de masa no es un simple poro, sino una estructura compuesta por tres capas dispuestas en serie: la célula endotelial, la membrana basal y el podocito epitelial. Esta visión tridimensional y multicapa es fundamental para entender la verdadera complejidad de la filtración.
Drummond y Deen abordaron el problema del flujo de agua a través de esta configuración, conceptualizando una disposición regular de poros endoteliales (fenestras) y poros epiteliales (diafragmas de hendidura), separados por una matriz de fibras (la membrana basal). Su análisis reveló que aproximadamente la mitad de la resistencia a la filtración se atribuía a la membrana basal glomerular y la otra mitad al diafragma de hendidura de los podocitos. Esto significa que ambas capas son igualmente importantes para regular el paso de líquido.
Cuando se investigó el daño renal experimental, como el causado por la administración de adriamicina, se observó que la pérdida de permeabilidad glomerular se debía a una disminución en el número de hendiduras epiteliales. Esto subraya la importancia de la integridad de los podocitos en el mantenimiento de la función de barrera. La extensión de este enfoque a las enfermedades humanas también indicó un aumento de la resistencia en el componente epitelial de la barrera en pacientes con daño renal.
Tabla Comparativa: Resistencia a la Filtración de Agua por Capa Glomerular
| Capa de la Membrana Glomerular | Resistencia al Flujo de Agua (%) |
|---|---|
| Membrana Basal Glomerular | ~50% |
| Diafragma de Hendidura (Podocitos Epiteliales) | ~50% |
El Papel Crucial de la Carga: La Selectividad Iónica de la Membrana
Además de la selectividad por tamaño, la membrana glomerular exhibe una notable selectividad por carga. Se ha observado que los flujos de aniones (moléculas con carga negativa) son menores y los flujos de cationes (moléculas con carga positiva) son mayores que los de moléculas neutras de tamaño comparable. Este hallazgo fue una exposición más definitiva de la observación temprana de que la albúmina, una proteína con carga negativa, es en gran parte excluida de la membrana basal.
Para explicar este efecto de carga, Deen et al. hipotetizaron que la membrana basal contenía cargas negativas fijas, creando potenciales de Donnan que actuaban como una barrera para el paso de aniones. Sin embargo, exámenes posteriores del transporte a través de membranas basales desnudas (sin células) no lograron identificar una selectividad de carga significativa, lo que sugería que la membrana basal por sí sola podría no ser la única, o incluso la principal, fuente de esta selectividad de carga.
El Descubrimiento de la Glucocáliz Endotelial: La Pieza Clave del Rompecabezas
Un avance crítico en la conceptualización del transporte de solutos capilares provino del trabajo de Curry y Michel, quienes propusieron que la glucocáliz luminal (una capa de glicoproteínas y proteoglicanos en la superficie de las células endoteliales) era una barrera importante en serie con las uniones celulares. Esta capa, con su estructura de matriz de fibras, podría describir las propiedades de transporte de manera más precisa.
El apoyo a esta premisa fundamental provino de experimentos en los que la digestión de la glucocáliz endotelial duplicó con creces la permeabilidad hidráulica capilar. Esto demostró de manera contundente la contribución de la glucocáliz a la resistencia al flujo de líquido. Modelos más sofisticados incorporaron el carácter de matriz de fibras de la glucocáliz, asignándole una resistencia hidráulica y difusiva sustancial, y la colocaron en serie con las uniones estrechas endoteliales.
Haraldsson y sus colaboradores identificaron la relevancia de la glucocáliz endotelial para la fisiología glomerular. Sus estudios en riñones de rata aislados y perfundidos, donde manipularon las propiedades de permeación dependientes del tamaño y la carga, los llevaron a concluir que la glucocáliz de la célula endotelial era la principal barrera de carga. Experimentos de digestión en el riñón perfundido aislado demostraron que la disolución morfológica de la glucocáliz se asociaba con un aumento de la permeación tanto de la albúmina cargada como del Ficoll neutro. Datos de apoyo adicionales provienen de células glomerulares en cultivo, que elaboran una glucocáliz que puede modificarse para producir cambios en la permeabilidad de solutos cargados y no cargados de la monocapa.
Una observación intrigante es que la glucocáliz es una estructura dinámica, cuyas propiedades de transporte pueden ser modificadas por señales hormonales, como el VEGF (factor de crecimiento endotelial vascular). El VEGF no solo impacta las propiedades de transporte de la glucocáliz, sino que también afecta las fenestraciones de los capilares glomerulares, lo que sugiere un mecanismo de regulación finamente ajustado. En general, el esfuerzo por racionalizar la filtración de fluidos y la permeación de solutos glomerulares en términos cuantitativos ha identificado contribuciones distintas de las células endoteliales y epiteliales a esta barrera compuesta.
Aplicaciones Clínicas y Disfunciones Renales: Entendiendo la Enfermedad
La comprensión detallada de la membrana capilar glomerular y sus componentes tiene profundas implicaciones clínicas. Desde una perspectiva traslacional, esta visión de una barrera compuesta es atractiva por su coherencia con los trastornos clínicos conocidos de las células endoteliales y epiteliales, cada uno manifestado como cantidades anormales de excreción de proteínas en la orina (proteinuria). Por ejemplo, ciertas enfermedades renales se caracterizan por el daño predominante a los podocitos (como la nefropatía por cambios mínimos o la glomeruloesclerosis focal y segmentaria), mientras que otras afectan principalmente al endotelio o a la membrana basal.
El análisis de la filtración glomerular, especialmente la curva de tamizaje (sieving curve) para moléculas de diferentes tamaños y cargas, se ha utilizado en pacientes con diversas afecciones renales. Por ejemplo, en pacientes con función renal alterada después de una cirugía a corazón abierto, se observó que la curva de tamizaje se desplazaba hacia arriba, lo que sugería un aumento en el componente difusivo de la depuración de dextrano, prediciendo una disminución en la presión de filtración glomerular. Esto demuestra cómo el conocimiento de la mecánica de la membrana puede ayudar a diagnosticar y comprender la fisiopatología de las enfermedades renales, permitiendo un enfoque más preciso en el tratamiento y manejo de estas condiciones.
Preguntas Frecuentes sobre la Membrana Glomerular
¿Qué es la membrana capilar glomerular?
La membrana capilar glomerular es una barrera altamente especializada dentro del riñón, compuesta por tres capas principales (endotelio fenestrado, membrana basal y podocitos epiteliales con diafragmas de hendidura), que filtra la sangre para formar la orina, permitiendo el paso de agua y pequeños solutos, pero reteniendo proteínas y células sanguíneas.
¿Cuáles son las tres capas principales de la barrera de filtración glomerular?
Las tres capas principales son: 1) El endotelio capilar, que tiene poros (fenestras); 2) La membrana basal glomerular, una capa acelular; y 3) Los podocitos epiteliales, que forman uniones interdigitadas con diafragmas de hendidura.
¿Cómo influyen las fuerzas de Starling en la filtración glomerular?
Las fuerzas de Starling (presiones hidrostáticas y oncóticas) son el motor de la filtración. La presión hidrostática en el capilar glomerular impulsa el líquido hacia el espacio de Bowman, mientras que la presión oncótica en el capilar y la presión hidrostática en el espacio de Bowman se oponen a esta filtración. El equilibrio de estas fuerzas determina la tasa neta de filtración.
¿Qué papel juega la glucocáliz en la filtración glomerular?
La glucocáliz endotelial, una capa de glicoproteínas en la superficie luminal del endotelio, es crucial como la principal barrera de carga de la membrana glomerular. Ayuda a repeler moléculas cargadas negativamente, como la albúmina, y contribuye significativamente a la resistencia hidráulica de la barrera de filtración.
¿Por qué es importante entender la función de la membrana glomerular?
Comprender la función de la membrana glomerular es vital porque permite explicar cómo se filtra la sangre y cómo se mantienen los equilibrios corporales. Además, es fundamental para el diagnóstico y la comprensión de las enfermedades renales, especialmente aquellas que cursan con proteinuria (exceso de proteínas en la orina), ya que estas a menudo se deben a un daño en esta compleja barrera de filtración.
Conclusión
La membrana capilar glomerular es una maravilla de la ingeniería biológica, un filtro altamente sofisticado y selectivo cuya función es indispensable para la vida. Desde los primeros modelos simplificados que explicaban la filtración por fuerzas de Starling y permeabilidad hidráulica, hasta la comprensión actual de una barrera compuesta por múltiples capas y la crucial contribución de la glucocáliz endotelial, la ciencia ha desvelado la intrincada mecánica detrás de la depuración sanguínea renal. Cada componente, desde las fenestras endoteliales hasta los diafragmas de hendidura de los podocitos y la compleja matriz de la membrana basal, juega un papel vital en el equilibrio entre permitir el paso de desechos y retener elementos esenciales. Esta comprensión profunda no solo enriquece nuestro conocimiento de la fisiología humana, sino que también proporciona las bases para el diagnóstico, tratamiento y desarrollo de terapias innovadoras para las diversas y a menudo devastadoras enfermedades que afectan la función renal.
Si quieres conocer otros artículos parecidos a La Membrana Glomerular: El Filtro Maestro del Riñón puedes visitar la categoría Cabello.