26/10/2011
El aire que respiramos, el aroma de un café recién hecho, o incluso la forma en que los contaminantes se dispersan en la atmósfera, son fenómenos gobernados por un principio fundamental de la física: la difusión de gases. A menudo subestimada, esta danza molecular invisible es esencial para la vida misma y para innumerables procesos industriales. Pero, ¿qué significa realmente que un gas se difunda? No es simplemente el movimiento del aire por una ráfaga de viento, sino un proceso mucho más sutil y constante, impulsado por las diferencias en la concentración individual de cada gas. Comprender la difusión es desentrañar cómo las moléculas, en su perpetuo movimiento aleatorio, buscan su propio equilibrio, moviéndose de forma autónoma a través de espacios y barreras.
A diferencia de un flujo de aire forzado, donde todas las moléculas se mueven en conjunto, la difusión es un ballet individual de partículas, cada una respondiendo a su propio llamado interno. Este fenómeno no solo nos permite oler las flores o detectar una fuga de gas, sino que también es el motor silencioso detrás de procesos biológicos vitales, como el intercambio de oxígeno y dióxido de carbono en nuestros pulmones. Profundicemos en este concepto fundamental para entender cómo los gases, por su propia naturaleza, tienden a esparcirse y mezclarse.
¿Qué es la Difusión de Gases?
En su esencia, la difusión de un gas se produce cuando hay un movimiento neto de moléculas desde un área donde ese gas en particular ejerce una presión parcial alta hacia un área donde ejerce una presión parcial más baja. Para visualizar esto, imagine un recipiente dividido en dos por una membrana permeable. Si en un lado tenemos una alta concentración de moléculas de oxígeno y en el otro una baja, las moléculas de oxígeno comenzarán a cruzar la membrana hacia el lado de menor concentración. Este movimiento no es orquestado; es el resultado de millones de colisiones y rebotes aleatorios de las moléculas. Cada molécula se mueve de manera independiente, chocando con otras moléculas de su propio tipo y de otros gases, así como con las paredes del recipiente. Aunque el movimiento es aleatorio y bidireccional, estadísticamente, habrá más moléculas moviéndose del área de alta concentración a la de baja, simplemente porque hay más moléculas en el lado de mayor concentración disponibles para realizar ese movimiento. Este flujo neto continuará hasta que la presión parcial del gas sea uniforme en ambas áreas, es decir, hasta que se alcance el equilibrio.
Es importante destacar que, incluso en el equilibrio, las moléculas no dejan de moverse. Simplemente, la tasa de movimiento en una dirección es igual a la tasa de movimiento en la dirección opuesta, lo que resulta en un movimiento neto cero. Sin embargo, en sistemas biológicos dinámicos como los pulmones, este equilibrio nunca se alcanza completamente para el oxígeno y el dióxido de carbono, ya que estos gases están constantemente entrando y saliendo, manteniendo un gradiente que impulsa el intercambio continuo.
Difusión vs. Flujo Masivo: Una Diferencia Crucial
Es fundamental distinguir la difusión del “flujo masivo” (o movimiento de masa o convección), ya que ambos describen el movimiento de gases pero bajo principios muy diferentes. Mientras que la difusión se rige por los gradientes de presión parcial individuales de cada gas, el flujo masivo obedece a diferencias en la presión total del sistema. En el flujo masivo, todas las moléculas de los diferentes gases se mueven juntas en la misma dirección, impulsadas por un gradiente de presión general, como el aire que se mueve a través de una tubería o el viento. Este movimiento es análogo a un río, donde toda el agua se mueve en la misma dirección debido a la pendiente.
En contraste, durante la difusión, los diferentes gases se mueven según sus propios gradientes de presión parcial individuales y la transferencia de gas se produce por un movimiento aleatorio molecular. Esto significa que el oxígeno puede moverse en una dirección mientras el dióxido de carbono se mueve en la opuesta, si sus respectivos gradientes de presión parcial así lo dictan. Esta distinción es vital, por ejemplo, en el sistema respiratorio humano, donde el aire se mueve por flujo masivo a través de las vías respiratorias conductoras (tráquea, bronquios) pero el intercambio de gases en los alvéolos (oxígeno hacia la sangre, dióxido de carbono hacia los alvéolos) se produce por difusión, aprovechando las diferencias de presión parcial.
Para clarificar estas diferencias, considere la siguiente tabla comparativa:
| Característica | Difusión | Flujo Masivo (Convección) |
|---|---|---|
| Fuerza Impulsora Principal | Gradiente de presión parcial de cada gas | Gradiente de presión total del gas |
| Movimiento de Moléculas | Independiente, movimiento aleatorio | Junto, en la misma dirección |
| Dependencia de la Composición | Cada gas se mueve según su propio gradiente | Todos los gases se mueven juntos |
| Escala de Operación Típica | Distancias cortas (ej. alvéolos, membranas) | Distancias largas (ej. vías respiratorias, viento) |
| Mecanismo | Movimiento molecular aleatorio | Movimiento de masa de fluidos |
Factores que Afectan la Tasa de Difusión
La velocidad a la que un gas se difunde no es constante; está influenciada por varios factores clave, lo que la hace un proceso dinámico y adaptable. Comprender estos factores es esencial para predecir y manipular el comportamiento de los gases en diversos entornos:
- Gradiente de Presión Parcial: Como se mencionó, la fuerza impulsora principal de la difusión es la diferencia de presión parcial entre dos áreas. Cuanto mayor sea este gradiente, más rápido será el movimiento neto de gas. Es por esto que en los pulmones, la concentración de oxígeno es mucho mayor en los alvéolos que en la sangre desoxigenada, creando un gradiente empinado que impulsa rápidamente el oxígeno hacia los glóbulos rojos.
- Temperatura: La temperatura juega un papel crucial. A temperaturas más altas, las moléculas de gas tienen mayor energía cinética y, por lo tanto, se mueven más rápido y chocan con mayor frecuencia. Este aumento en el movimiento molecular acelera la tasa de difusión. Por ejemplo, un ambientador libera su fragancia más rápidamente en una habitación cálida que en una fría.
- Peso Molecular (Masa Molecular): Las moléculas más ligeras se difunden más rápidamente que las moléculas más pesadas a la misma temperatura, ya que pueden moverse a velocidades promedio más altas. Esta relación se describe por la Ley de Graham, que establece que la tasa de difusión de un gas es inversamente proporcional a la raíz cuadrada de su masa molecular. Esto explica por qué el helio se escapa de un globo más rápido que el aire.
- Área de Superficie Disponible: Cuanto mayor sea el área a través de la cual puede ocurrir la difusión, más moléculas pueden cruzar simultáneamente, aumentando la tasa global de difusión. En los pulmones, la vasta área superficial de los alvéolos (aproximadamente el tamaño de una cancha de tenis) es fundamental para un intercambio de gases eficiente.
- Distancia de Difusión: La distancia que las moléculas deben recorrer también afecta la velocidad. Cuanto más delgada sea la barrera o más corta la distancia, más rápida será la difusión. Si la distancia es excesiva, la difusión puede volverse ineficaz. Las paredes alveolares y capilares en los pulmones son extremadamente delgadas (aproximadamente 0.2 a 0.6 micrómetros) para facilitar este proceso.
- Solubilidad del Gas: En el contexto de la difusión a través de una fase líquida (como en los tejidos corporales), la solubilidad del gas en ese líquido es importante. Un gas más soluble se difundirá más fácilmente a través de un medio líquido. Por ejemplo, el dióxido de carbono es mucho más soluble en el plasma sanguíneo que el oxígeno, lo que compensa su menor gradiente de presión parcial en la difusión pulmonar.
La Difusión en la Vida Cotidiana y la Biología
La difusión no es solo un concepto teórico; es un proceso omnipresente que afecta nuestra vida diaria y es fundamental para la biología.
En el hogar, cuando abrimos una botella de perfume, el aroma no tarda en llenar la habitación. Las moléculas de fragancia se difunden desde el área de alta concentración (la botella) hacia el resto del aire, donde su presión parcial es inicialmente cero. De manera similar, el olor de una comida cocinándose se extiende por la casa a medida que las moléculas volátiles se difunden. Incluso el proceso de infundir té o café depende de la difusión de las moléculas de sabor y aroma del sólido al líquido.
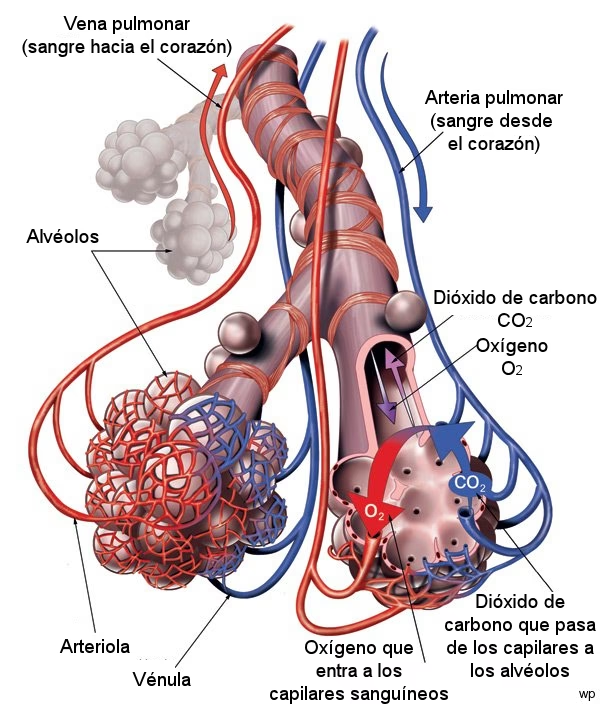
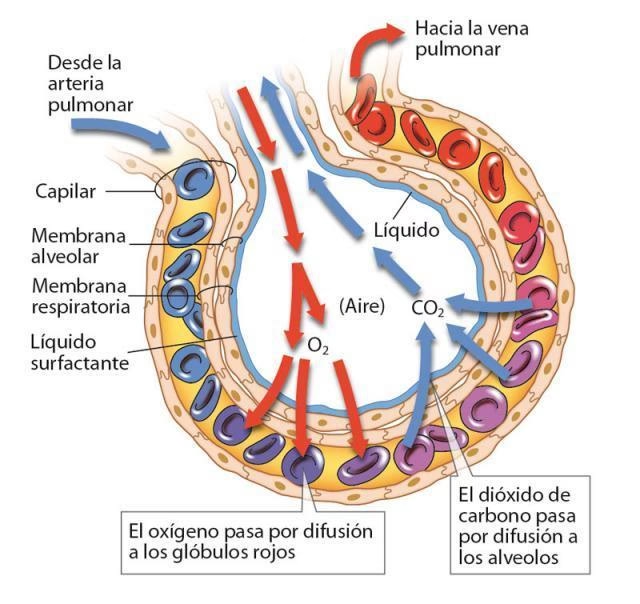
En el ámbito biológico, la difusión es un pilar de la vida. El ejemplo más claro es el intercambio de gases en los pulmones, como se mencionó anteriormente. El oxígeno (O₂) se difunde desde los alvéolos, donde su presión parcial es alta, hacia los capilares sanguíneos, donde su presión parcial es baja (debido a que la sangre que llega ha liberado su oxígeno a los tejidos). Simultáneamente, el dióxido de carbono (CO₂) se difunde en la dirección opuesta, desde los capilares (donde es un producto de desecho del metabolismo y su presión parcial es alta) hacia los alvéolos (donde su presión parcial es baja y será exhalado). Este constante movimiento garantiza que la sangre esté siempre oxigenada y libre de CO₂ excesivo.
Más allá de los pulmones, la difusión es vital para el transporte de nutrientes y productos de desecho a nivel celular. Las células obtienen oxígeno y nutrientes del líquido intersticial que las rodea y liberan dióxido de carbono y otros desechos al mismo líquido, todo ello a través de procesos de difusión a través de sus membranas celulares. Incluso la forma en que los neurotransmisores cruzan la hendidura sináptica para transmitir señales entre neuronas implica difusión, permitiendo la comunicación neuronal.
Leyes Fundamentales de la Difusión
Para cuantificar y predecir la tasa de difusión, los científicos han desarrollado leyes fundamentales. Las más conocidas son la Ley de Graham y la Ley de Fick, que proporcionan marcos matemáticos para entender este fenómeno.
Ley de Graham de la Efusión y Difusión: Formulada por Thomas Graham en 1846, esta ley establece que la tasa de efusión o difusión de un gas es inversamente proporcional a la raíz cuadrada de la masa molar de sus partículas. En términos sencillos, los gases más ligeros se difunden más rápido que los gases más pesados. Esto se debe a que las moléculas más ligeras se mueven a velocidades promedio más altas a la misma temperatura. Por ejemplo, el hidrógeno (con una masa molar de aproximadamente 2 g/mol) se difundirá mucho más rápido que el oxígeno (con una masa molar de aproximadamente 32 g/mol).
Matemáticamente, si R₁ y R₂ son las tasas de difusión de dos gases, y M₁ y M₂ son sus respectivas masas molares, entonces:R₁ / R₂ = √(M₂ / M₁)
Esta ley es crucial para procesos como la separación de gases y la comprensión de cómo los gases se dispersan en diferentes ambientes.
Ley de Fick de la Difusión: Desarrollada por Adolf Fick en 1855, esta ley describe la difusión a través de una superficie o un medio. La primera Ley de Fick establece que el flujo de difusión (la cantidad de sustancia que se difunde por unidad de área por unidad de tiempo) es proporcional al gradiente de concentración (o presión parcial) y al coeficiente de difusión. Es decir, cuanto mayor sea la diferencia de concentración y mayor la capacidad del gas para moverse a través del medio, más rápido será el flujo.
J = -D * (dC/dx)
Donde:
Jes el flujo de difusión, que representa la cantidad de sustancia que se mueve por unidad de área y tiempo.Des el coeficiente de difusión, una constante que depende de la temperatura, la viscosidad del medio y el tamaño de las partículas que se difunden.dC/dxes el gradiente de concentración (cambio de concentración con la distancia), que indica cuán pronunciada es la diferencia de concentración.
El signo negativo indica que la difusión ocurre en la dirección de la concentración decreciente. La Ley de Fick es fundamental para entender procesos como la transferencia de gases en los pulmones, la absorción de fármacos en el cuerpo y la dispersión de contaminantes en el suelo y el aire.
Aplicaciones Prácticas de la Difusión
Más allá de su importancia biológica y en la naturaleza, el principio de difusión tiene numerosas aplicaciones en la industria y la tecnología, demostrando su relevancia en el mundo moderno:
- Separación de Gases: La diferencia en las tasas de difusión entre gases con diferentes masas moleculares se utiliza para separar mezclas de gases. Un ejemplo histórico fue la separación de isótopos de uranio (U-235 y U-238) durante el Proyecto Manhattan, donde el U-235, más ligero, se difundía ligeramente más rápido a través de membranas porosas, permitiendo su enriquecimiento, un paso crítico para la producción de energía nuclear y armas.
- Tecnología de Membranas: Las membranas semipermeables se diseñan para permitir la difusión selectiva de ciertos gases, lo que se utiliza en la purificación de gases, la recuperación de hidrógeno en procesos industriales y la separación de aire para obtener nitrógeno y oxígeno puros, esenciales en la medicina y la metalurgia.
- Sensores de Gas: Muchos sensores de gas funcionan basándose en la difusión. Un gas objetivo se difunde hacia un elemento sensor, donde reacciona o altera una propiedad eléctrica, lo que indica su presencia y concentración. Estos sensores son vitales para la seguridad en entornos industriales, monitoreo ambiental y detección de fugas.
- Ingeniería Ambiental: La difusión es clave para entender cómo los contaminantes gaseosos se dispersan en la atmósfera o cómo los gases del suelo se mueven a través de las capas del suelo. Este conocimiento ayuda en la modelización de la calidad del aire, la remediación de sitios contaminados y el monitoreo de la emisión de gases de efecto invernadero.
- Industria Alimentaria: En la maduración de frutas, la difusión de etileno (un gas madurador) juega un papel crucial. También en la carbonatación de bebidas, la difusión del CO₂ en el líquido es esencial para lograr el nivel deseado de efervescencia. La difusión también interviene en la curación de quesos y carnes.
- Medicina y Farmacia: Además de la respiración, la difusión es vital para la entrega de fármacos a través de parches transdérmicos, donde el medicamento se difunde a través de la piel hacia el torrente sanguíneo a una velocidad controlada. También es relevante en la anestesia, donde los gases anestésicos se difunden a través de las membranas pulmonares hacia la sangre para inducir la inconsciencia, y en la hemodiálisis, donde los productos de desecho se difunden de la sangre a una solución de diálisis.
Preguntas Frecuentes sobre la Difusión de Gases
- ¿Por qué es importante la difusión?
- La difusión es fundamental porque permite el movimiento de sustancias a nivel molecular sin necesidad de un sistema de transporte activo. En biología, es esencial para la respiración, la nutrición celular y la eliminación de desechos. En la industria, se utiliza para separar gases, purificar sustancias y en la fabricación de diversos productos. Es un proceso pasivo que ocurre constantemente a nuestro alrededor, facilitando la mezcla y la distribución de gases en cualquier espacio.
- ¿Cómo se relaciona la difusión con la respiración?
- La difusión es el mecanismo principal para el intercambio de oxígeno y dióxido de carbono en los pulmones. El oxígeno se difunde desde los alvéolos (sacos de aire) hacia la sangre en los capilares, y el dióxido de carbono se difunde desde la sangre hacia los alvéolos para ser exhalado. Este intercambio ocurre debido a los gradientes de presión parcial de cada gas. Sin la difusión, nuestras células no recibirían el oxígeno necesario y no podrían eliminar el dióxido de carbono tóxico.
- ¿La difusión solo ocurre con gases?
- No, la difusión ocurre en gases, líquidos y sólidos, aunque es mucho más lenta en líquidos y especialmente en sólidos debido a la menor libertad de movimiento de las moléculas. Por ejemplo, el azúcar se difunde en el agua, y las aleaciones metálicas pueden formarse por difusión de átomos en estado sólido, aunque esto último puede llevar miles de años. Sin embargo, en el contexto de la "difusión de gases", nos referimos específicamente al movimiento de moléculas gaseosas.
- ¿Es lo mismo difusión que ósmosis?
- No, aunque ambos son procesos de transporte pasivo. La difusión es el movimiento de partículas (solutos) de una región de mayor concentración a una de menor concentración. La ósmosis es un tipo específico de difusión que se refiere al movimiento de moléculas de agua (o disolvente) a través de una membrana semipermeable desde una región de mayor concentración de agua a una de menor concentración de agua (o mayor concentración de soluto). La ósmosis es crucial para el equilibrio hídrico en las células.
- ¿Puede la difusión ocurrir en el vacío?
- Sí, la difusión de gases puede ocurrir en el vacío, aunque el término "difusión" implica colisiones moleculares y un medio. Si se introduce un gas en un vacío, las moléculas se dispersarán rápidamente para llenar el volumen disponible. En este caso, no hay otras moléculas con las que colisionar, por lo que el movimiento es puramente balístico hasta que las moléculas chocan con las paredes del recipiente. A medida que el volumen se llena, las colisiones entre moléculas comienzan a ocurrir, y el proceso se parece más a la difusión clásica, aunque la dispersión inicial es extremadamente rápida.
- ¿Cuánto tiempo tarda la difusión?
- El tiempo que tarda la difusión varía enormemente dependiendo de los factores mencionados: el tamaño de las moléculas, la temperatura, la distancia a recorrer y el medio. En distancias microscópicas (como a través de una membrana celular), la difusión es casi instantánea. En distancias macroscópicas (como el olor de un perfume llenando una habitación), puede tardar segundos o minutos. En medios densos o a través de grandes distancias, puede ser un proceso muy lento, lo que explica por qué el oxígeno no se difunde rápidamente a través de grandes volúmenes de agua sin ayuda de corrientes.
Si quieres conocer otros artículos parecidos a La Fascinante Difusión de Gases: Un Viaje Molecular puedes visitar la categoría Cabello.