23/11/2019
Los riñones son órganos vitales que desempeñan un papel crucial en la filtración de la sangre, eliminando desechos y excesos de líquidos para mantener nuestro cuerpo en equilibrio. Dentro de cada riñón, miles de unidades diminutas llamadas glomérulos actúan como filtros microscópicos. Sin embargo, ciertas afecciones pueden comprometer su función, y una de las más relevantes es el engrosamiento de la membrana basal glomerular. Este fenómeno, aunque suene complejo, es la clave para entender una enfermedad renal significativa: la nefropatía membranosa. Profundicemos en qué consiste este engrosamiento, por qué ocurre y cómo se maneja para preservar la salud renal.
- ¿Qué es el Engrosamiento de la Membrana Basal Glomerular?
- Las Causas Detrás del Engrosamiento: Primario y Secundario
- Síntomas y Diagnóstico: Desentrañando la Nefropatía Membranosa
- El Curso de la Enfermedad: De la Remisión Espontánea a la Progresión
- Opciones de Tratamiento para la Nefropatía Membranosa
- Nefropatía Membranosa y Trasplante Renal: Desafíos y Consideraciones
- Preguntas Frecuentes (FAQs)
- ¿Es el engrosamiento de la membrana basal glomerular reversible?
- ¿Qué tan rápido progresa la nefropatía membranosa?
- ¿Puedo llevar una vida normal con engrosamiento de la membrana basal glomerular?
- ¿La nefropatía membranosa afecta solo a los riñones?
- ¿Cómo se monitorea la enfermedad después del diagnóstico?
¿Qué es el Engrosamiento de la Membrana Basal Glomerular?
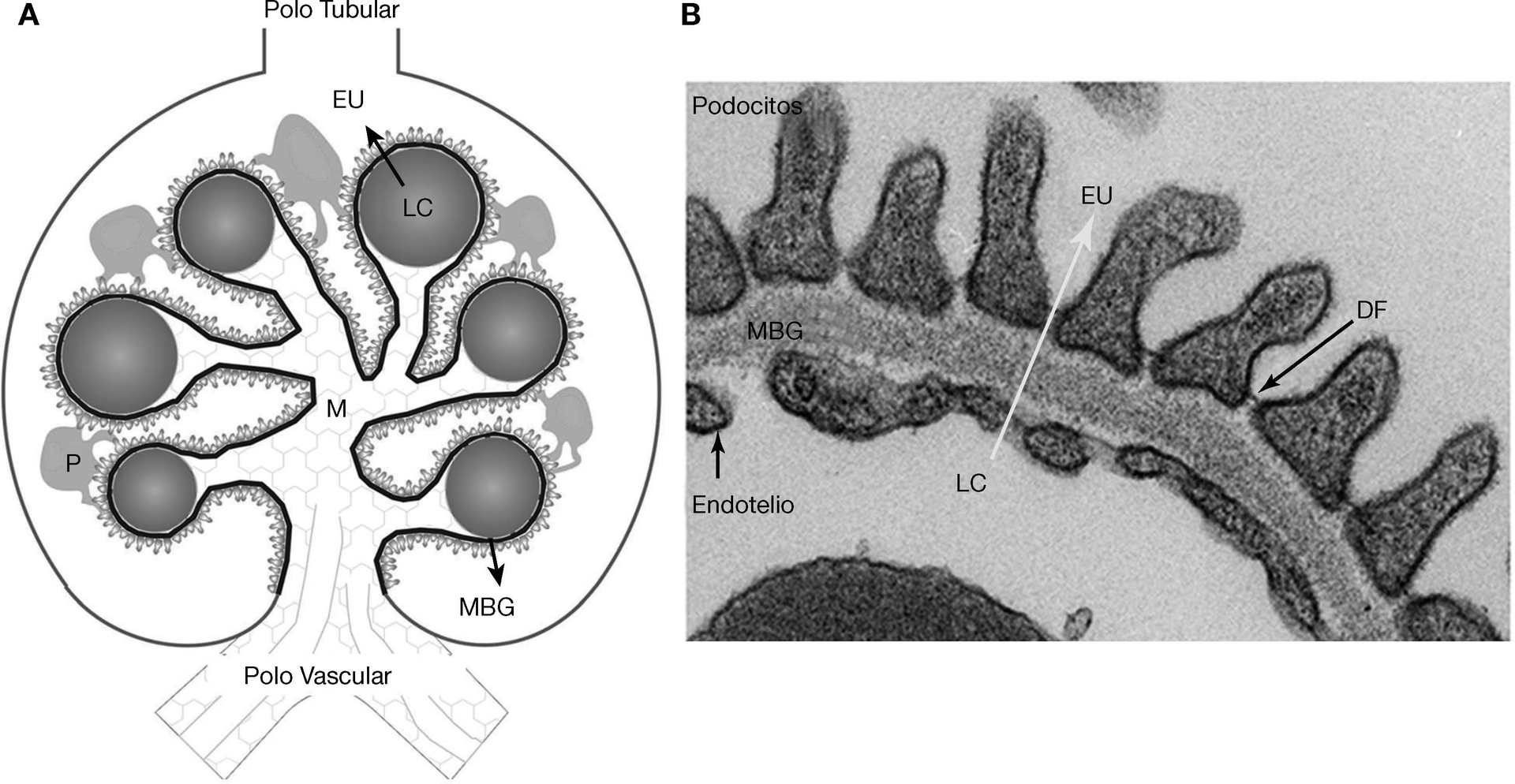
La membrana basal glomerular (MBG) es una capa especializada de tejido dentro del glomérulo renal. Su función principal es actuar como una barrera de filtración, permitiendo el paso de agua y pequeñas moléculas de desecho, mientras retiene proteínas esenciales y células sanguíneas en el torrente sanguíneo. Cuando esta membrana se engrosa, su capacidad para filtrar adecuadamente se ve comprometida.
El engrosamiento de la membrana basal glomerular es la característica distintiva de una condición llamada nefropatía membranosa. Al alterarse la estructura de esta membrana, se produce una fuga significativa de proteínas desde la sangre hacia la orina, un proceso conocido como proteinuria. Esta pérdida masiva de proteínas es la manifestación central y más perjudicial de la enfermedad, llevando a una serie de síntomas y complicaciones que, en conjunto, se denominan síndrome nefrótico.
El síndrome nefrótico es un trastorno renal que se caracteriza por:
- Proteinuria masiva: Grandes cantidades de proteína en la orina (>3.5 gramos/24 horas).
- Hipoalbuminemia: Bajos niveles de albúmina (una proteína vital) en la sangre.
- Hiperlipidemia: Niveles elevados de colesterol y triglicéridos en la sangre.
- Edema: Hinchazón, especialmente en los pies, tobillos, piernas y alrededor de los ojos, debido a la retención de líquidos.
- Mayor riesgo de coágulos de sangre: Una complicación grave debido a la pérdida de proteínas anticoagulantes en la orina.
Comprender este proceso es fundamental, ya que la nefropatía membranosa es una de las causas más comunes de síndrome nefrótico en adultos, afectando la calidad de vida y, si no se trata, pudiendo llevar a insuficiencia renal crónica.
Las Causas Detrás del Engrosamiento: Primario y Secundario
Aunque la razón exacta del engrosamiento de la membrana basal glomerular no siempre se conoce con certeza, la nefropatía membranosa se clasifica generalmente en dos grandes categorías: primaria (o idiopática) y secundaria.
Nefropatía Membranosa Primaria: Un Misterio Desvelado por la Inmunología
Históricamente, la nefropatía membranosa primaria era considerada idiopática, es decir, de causa desconocida. Sin embargo, los avances recientes en la investigación han desvelado que la mayoría de estos casos son de naturaleza autoinmune. Esto significa que el propio sistema inmunitario del cuerpo, por error, ataca sus propios tejidos. En la nefropatía membranosa primaria, el ataque se dirige contra proteínas específicas presentes en los podocitos, que son células especializadas que recubren la superficie externa de la membrana basal glomerular y son fundamentales para la filtración renal.
El principal antígeno (la sustancia atacada por el sistema inmunitario) identificado es el receptor de la fosfolipasa A2 del tipo M (PLA2R). Los anticuerpos dirigidos contra PLA2R (principalmente IgG4) atraviesan la barrera de filtración y se unen a esta proteína en la superficie externa de la membrana, formando depósitos de inmunocomplejos. Estos depósitos desencadenan una respuesta inflamatoria que daña el podocito y provoca el engrosamiento de la membrana y la fuga de proteínas. Si bien el anti-PLA2R es el responsable del 70-80% de los casos primarios, se han descubierto otros antígenos podocitarios implicados, como THSD7A, EXT1/EXT2, NELL-1, y otros, aunque son menos frecuentes.
Los mecanismos que desencadenan esta autoinmunidad no están del todo claros, pero estudios genéticos sugieren una predisposición en individuos con ciertos alelos HLA y genes relacionados con los antígenos podocitarios. Una vez que los inmunocomplejos se depositan, activan el sistema del complemento, una parte de la respuesta inmune, que contribuye significativamente al daño podocitario y a la proteinuria masiva.
Nefropatía Membranosa Secundaria: Cuando Otros Factores Son la Clave
En contraste con la forma primaria, la nefropatía membranosa secundaria se asocia con otras enfermedades, exposiciones o tratamientos. En estos casos, los inmunocomplejos se forman en respuesta a antígenos externos (infecciosos, farmacológicos o tumorales) o internos (asociados a enfermedades sistémicas), que luego se depositan en la misma localización subepitelial de la membrana basal glomerular. La identificación de la causa subyacente es crucial, ya que tratar la enfermedad primaria puede llevar a la resolución de la nefropatía.
Los factores que incrementan el riesgo de desarrollar nefropatía membranosa secundaria incluyen:
- Cánceres: Especialmente los de colon y pulmón, pero también otros tumores. Algunos antígenos como THSD7A y NELL-1 se asocian particularmente con malignidades.
- Exposición a toxinas: Como el oro y el mercurio.
- Infecciones: Hepatitis B, malaria, sífilis, y endocarditis.
- Uso de ciertos medicamentos: Penicilamina, trimetadiona, y algunas cremas para aclarar la piel.
- Trastornos autoinmunitarios: Lupus eritematoso sistémico (LES), artritis reumatoide, enfermedad de Graves, entre otros. La nefropatía membranosa lúpica es un subtipo bien reconocido de la enfermedad.
La enfermedad puede presentarse a cualquier edad, pero es más común después de los 40 años.

| Característica | Nefropatía Membranosa Primaria | Nefropatía Membranosa Secundaria |
|---|---|---|
| Causa Principal | Autoinmune (anticuerpos vs. antígenos podocitarios como PLA2R) | Asociada a otras enfermedades/factores externos |
| Antígenos Específicos | PLA2R, THSD7A, NELL-1 (menos frecuente), etc. | Relacionados con infección, fármacos, tumores, autoinmunes |
| Edad de Aparición | Común en adultos >40 años, pero puede ser a cualquier edad | Variable, según la enfermedad subyacente |
| Hallazgos Histológicos (Adicionales) | Predominio de IgG4, sin proliferación celular glomerular | IgG1-3 predominante, complejos en mesangio/subendotelio, proliferación celular, cuerpos tubuloreticulares |
| Tratamiento | Inmunosupresores específicos para el tipo autoinmune | Tratamiento de la enfermedad subyacente y soporte renal |
Síntomas y Diagnóstico: Desentrañando la Nefropatía Membranosa
El diagnóstico temprano y preciso de la nefropatía membranosa es fundamental para un manejo efectivo y para prevenir la progresión de la enfermedad renal.
El Cuadro Clínico: Más Allá de la Hinchazón
En la mayoría de los casos (aproximadamente el 80%), la nefropatía membranosa se manifiesta con un síndrome nefrótico completo. Esto significa que los pacientes notan la aparición de edema (hinchazón) de forma insidiosa, que puede ser más o menos abrupta. Esta hinchazón se localiza típicamente en las piernas, los tobillos y los pies, pero también puede afectar la cara (especialmente alrededor de los ojos) y el abdomen. La hipoalbuminemia grave, resultado de la pérdida de proteínas, es la principal responsable de este edema.
Otros síntomas y signos incluyen:
- Orina espumosa: Debido a la alta concentración de proteínas.
- Aumento de peso: Por la retención de líquidos.
- Fatiga: Relacionada con la anemia (menos común) o el estado general de la enfermedad.
Aunque la presencia de microhematuria (sangre microscópica en la orina) es relativamente común, la hematuria macroscópica (visible a simple vista) es rara y, si se presenta, debe alertar a los médicos sobre posibles complicaciones como trombosis de las venas renales o tumores urológicos.
Las complicaciones del síndrome nefrótico, como la hipercoagulabilidad, pueden ser muy graves. Los pacientes tienen un mayor riesgo de desarrollar trombosis venosas, incluyendo trombosis de las venas renales y tromboembolismo pulmonar, que en ocasiones pueden ser la primera manifestación clínica de la enfermedad.
Analíticamente, además de la proteinuria e hipoalbuminemia, se observan niveles elevados de lípidos (colesterol y triglicéridos). Los niveles de complemento sérico, a diferencia de otras glomerulonefritis, suelen ser normales en la nefropatía membranosa primaria.
En el momento del diagnóstico, la función renal suele ser normal y la presión arterial también se mantiene en rangos saludables. Sin embargo, la aparición de hipertensión arterial se relaciona frecuentemente con el desarrollo de insuficiencia renal crónica. En casos de proteinuria masiva y hipoalbuminemia severa, puede haber un deterioro progresivo de la función renal en los primeros meses. También pueden ocurrir episodios de fracaso renal agudo reversible, a menudo precipitados por el uso excesivo de diuréticos o medicamentos que afectan el sistema renina-angiotensina-aldosterona en pacientes con inestabilidad hemodinámica.
El Diagnóstico: Biopsia Renal y el Avance de los Biomarcadores
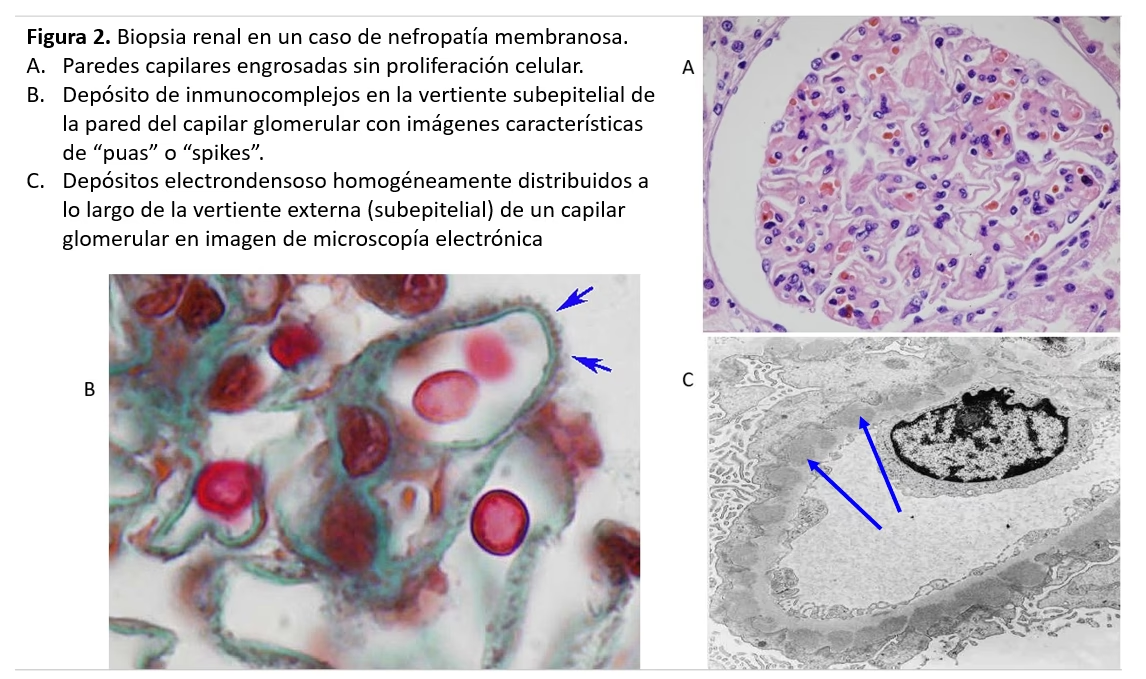
Tradicionalmente, la biopsia renal ha sido el pilar fundamental para el diagnóstico definitivo de la nefropatía membranosa. Este procedimiento consiste en tomar una pequeña muestra de tejido renal para examinarla bajo el microscopio. La microscopía óptica revelará un engrosamiento uniforme y difuso de las paredes capilares glomerulares, sin proliferación celular, y con tinciones especiales (como la plata-metenamina) se observan las características imágenes de "púas" o "spikes", que son prolongaciones espiculares de la membrana basal que intentan envolver los depósitos inmunes. La inmunofluorescencia mostrará depósitos de IgG y C3 a lo largo de la pared capilar, y la microscopía electrónica confirmará la presencia de depósitos electrondensos homogéneamente distribuidos en la vertiente subepitelial.
Sin embargo, el panorama diagnóstico ha cambiado drásticamente con el descubrimiento de los anticuerpos anti-PLA2R. En pacientes con proteinuria y síndrome nefrótico, la detección de anti-PLA2R positivos permite establecer el diagnóstico de nefropatía membranosa primaria sin necesidad de realizar una biopsia renal en muchos casos. Esta prueba ha demostrado ser un marcador diagnóstico y pronóstico muy fiable, diferenciando rápidamente las formas primarias de las secundarias.
Aun así, existen excepciones en las que la biopsia sigue siendo necesaria, como en pacientes con función renal ya deteriorada (filtrado glomerular inferior a 60 ml/min/1.73 m2), curso clínico atípico, datos analíticos que sugieran otras patologías (por ejemplo, anticuerpos antinucleares positivos para lupus), o persistencia del síndrome nefrótico a pesar de la negativización de los anti-PLA2R. Es importante destacar que en las primeras fases de la enfermedad, los anticuerpos anti-PLA2R pueden no detectarse en la sangre (efecto sumidero) porque están todos depositados en el glomérulo, pero suelen aparecer en semanas posteriores.
El Curso de la Enfermedad: De la Remisión Espontánea a la Progresión
La evolución de la nefropatía membranosa es variable y puede seguir diferentes caminos, desde la remisión completa hasta la progresión a insuficiencia renal.

Remisión Espontánea: Una Luz de Esperanza
Una característica notable de la nefropatía membranosa es la posibilidad de remisión espontánea, que ocurre en el 30-45% de los casos. Esto significa que la proteinuria disminuye o desaparece y la función renal se mantiene estable, sin necesidad de tratamiento inmunosupresor. Las remisiones pueden ser parciales (proteinuria disminuye por debajo del umbral nefrótico pero aún es detectable) o completas (proteinuria se estabiliza por debajo de 0.3 g/24h).
Factores como ser mujer, tener una menor cantidad de proteinuria al inicio y una función renal completamente preservada aumentan la probabilidad de remisión espontánea. La mayoría de estas remisiones se producen en los primeros dos años de la enfermedad y la disminución de la proteinuria suele ser gradual. El tratamiento de soporte con inhibidores de la enzima convertidora de angiotensina (IECA) o antagonistas de los receptores de angiotensina II (ARAII), además de su efecto antihipertensivo, también puede favorecer la remisión espontánea.
El pronóstico a largo plazo para los pacientes que experimentan una remisión espontánea, ya sea parcial o completa, es excelente, con muy pocas recaídas y una alta tasa de supervivencia renal.
El Riesgo de Progresión y sus Marcadores
Por otro lado, un 15-20% de los pacientes presentan un curso clínico más agresivo, con proteinuria masiva y un rápido deterioro de la función renal en los primeros 12-24 meses. Sin tratamiento, el pronóstico para estos casos es desfavorable. El resto de los pacientes (40-60%) pueden mantener un síndrome nefrótico persistente durante años, sin remisión espontánea ni deterioro renal inmediato. Sin embargo, esta situación prolongada los expone a las complicaciones crónicas del síndrome nefrótico, como trombosis y un mayor riesgo cardiovascular por la dislipemia persistente.
Para predecir la evolución de la enfermedad, los médicos utilizan diversos marcadores pronósticos:
- Monitorización de proteinuria y función renal: Los cambios en estos parámetros en los primeros meses son clave.
- Excreción urinaria de IgG y proteínas de bajo peso molecular: Como la α-1 microglobulina y la ß2-microglobulina, que son excelentes predictores de insuficiencia renal.
- Títulos seriados de anti-PLA2R: Este es, sin duda, el marcador más fiable para predecir la evolución y la respuesta al tratamiento. Títulos elevados de anti-PLA2R se asocian con un peor pronóstico y una respuesta menos favorable a la terapia. La disminución de estos títulos (remisión inmunológica) precede en semanas o meses a la remisión clínica de la proteinuria. Además, los valores altos de anti-PLA2R pueden predecir la recidiva de la enfermedad después de un trasplante renal.
Basándose en estos marcadores clínicos, analíticos y serológicos, las guías clínicas como las KDIGO proponen perfiles de riesgo (bajo, moderado, alto) que ayudan a guiar las decisiones terapéuticas.
Opciones de Tratamiento para la Nefropatía Membranosa
El tratamiento de la nefropatía membranosa ha evolucionado significativamente, buscando un enfoque personalizado que se adapte a las características y el perfil de riesgo de cada paciente.
El Enfoque Conservador: Gestión Inicial y Medidas de Soporte
Para los pacientes con bajo riesgo de progresión o aquellos que muestran una tendencia a la disminución de la proteinuria, se recomienda un período de observación de al menos 6 meses antes de iniciar un tratamiento inmunosupresor agresivo. Durante esta fase, se implementan medidas conservadoras para controlar los síntomas y reducir los riesgos asociados al síndrome nefrótico:
- Dieta sin sal: Para controlar el edema.
- Diuréticos: (Tiazidas, furosemida) en dosis adecuadas para reducir la hinchazón.
- Inhibidores de la enzima convertidora de angiotensina (IECA) o Antagonistas de los receptores de angiotensina II (ARAII): Además de controlar la presión arterial, estos fármacos reducen significativamente la proteinuria y pueden facilitar las remisiones espontáneas. Su uso debe ser cauteloso en pacientes con hipoalbuminemia severa para evitar inestabilidad hemodinámica.
- Tratamiento hipolipemiante: Con estatinas, para controlar los niveles elevados de colesterol y triglicéridos y reducir el riesgo cardiovascular.
- Anticoagulación: En casos de hipoalbuminemia significativa (<2-2.5 g/dl), especialmente si existen otros factores de riesgo de trombosis (obesidad, antecedentes de coágulos, inmovilización), para prevenir complicaciones tromboembólicas. Se debe evaluar el riesgo de sangrado individualmente.
Este período de observación no es adecuado para pacientes con deterioro progresivo de la función renal, complicaciones graves del síndrome nefrótico (como tromboembolismo pulmonar) o hipoalbuminemia extrema y edema masivo que no responde a diuréticos.
Terapias Inmunosupresoras: Un Arsenal Contra la Enfermedad
Para los pacientes de riesgo moderado o alto, o aquellos que no responden al tratamiento conservador, se recurre a terapias inmunosupresoras. Varios regímenes han demostrado eficacia:
Corticosteroides y Ciclofosfamida: La Pauta Clásica de Ponticelli
La combinación de corticosteroides y ciclofosfamida, administrada en ciclos durante 6 meses (conocida como pauta de Ponticelli), ha sido un estándar de oro. Los estudios han demostrado una tasa de remisión completa o parcial del 70-80%. La ciclofosfamida es el agente alquilante preferido debido a su menor perfil de efectos secundarios en comparación con el clorambucil. Aunque efectiva, esta pauta requiere medidas preventivas para infecciones.
Anticalcineurínicos: Eficacia con Desafíos
Fármacos como la ciclosporina y el tacrolimus (anticalcineurínicos) también son muy efectivos, induciendo remisión en más del 70-80% de los casos. Se administran por periodos de 12-18 meses y tienen un efecto antiproteinúrico directo sobre los podocitos. Sin embargo, su principal limitación es la alta tasa de recaídas (cercana al 50%) que se observa al suspender el fármaco. La administración de rituximab antes de la retirada de los anticalcineurínicos ha mostrado promesas en la reducción de estas recaídas.
Rituximab: La Promesa de la Terapia Dirigida
El rituximab, un anticuerpo monoclonal que se dirige a las células B (implicadas en la producción de anticuerpos), ha surgido como una opción de tratamiento muy importante. Induce remisión completa o parcial en el 50-60% de los casos, con buena tolerancia. Su efecto puede ser relativamente lento, pero estudios comparativos han demostrado que puede ser superior a los anticalcineurínicos a largo plazo en cuanto a tasas de remisión sostenida y prevención de recaídas.

Otras Opciones y Combinaciones
El micofenolato, aunque prometedor en estudios observacionales, no ha demostrado una eficacia superior al tratamiento conservador en estudios controlados, pero podría tener un papel en casos resistentes. La investigación actual explora combinaciones de rituximab con ciclofosfamida para maximizar la eficacia, así como el papel de nuevos fármacos renoprotectores y antialbuminúricos (como los inhibidores de SGLT2, antialdosterónicos de tercera generación y anti-endotelina) para potenciar la protección renal y mantener la proteinuria al mínimo.
Objetivos del Tratamiento: Más Allá de la Remisión Completa
Si bien el objetivo óptimo es la remisión completa (proteinuria <0.3 g/24h), en la nefropatía membranosa, la inducción de una remisión parcial (proteinuria <3.5 g/24h) ya se asocia con una supervivencia renal significativamente superior. Incluso el mantenimiento de proteinurias entre 1-3.5 g/24h a lo largo del seguimiento puede ser aceptable si no hay deterioro de la función renal, a diferencia de otras nefropatías donde estos niveles son considerados de alto riesgo.
Nefropatía Membranosa y Trasplante Renal: Desafíos y Consideraciones
Para los pacientes cuya nefropatía membranosa progresa a insuficiencia renal terminal, el trasplante renal se convierte en una opción viable. Sin embargo, la enfermedad puede recurrir en el riñón trasplantado. Es crucial distinguir entre la recurrencia de la enfermedad original (a menudo ligada a la presencia de anti-PLA2R) y una nefropatía membranosa de novo (que se desarrolla por primera vez en el injerto y suele ser anti-PLA2R negativa, asociada a factores como rechazos previos o infecciones).
Un título elevado de anti-PLA2R antes del trasplante puede desaconsejar el procedimiento hasta que los niveles disminuyan o desaparezcan, ya sea espontáneamente o con tratamiento, para reducir el riesgo de recurrencia temprana. En caso de recurrencia o desarrollo de nefropatía membranosa de novo post-trasplante, el rituximab es a menudo el tratamiento de elección, dado que los pacientes ya están bajo regímenes inmunosupresores y otros fármacos como la ciclofosfamida podrían tener efectos secundarios significativos.
Preguntas Frecuentes (FAQs)
¿Es el engrosamiento de la membrana basal glomerular reversible?
En muchos casos, especialmente con un diagnóstico y tratamiento tempranos, la nefropatía membranosa puede entrar en remisión, ya sea espontáneamente o inducida por tratamiento. Esto significa que el daño a la membrana basal glomerular puede estabilizarse o incluso mejorar, y la proteinuria disminuir. Sin embargo, en casos avanzados con fibrosis renal significativa, el daño puede ser irreversible.
¿Qué tan rápido progresa la nefropatía membranosa?
La progresión de la nefropatía membranosa es muy variable. Algunos pacientes experimentan una remisión espontánea en los primeros años, mientras que otros pueden mantener el síndrome nefrótico durante mucho tiempo sin un deterioro significativo de la función renal. Sin embargo, un subgrupo de pacientes (15-20%) puede experimentar una progresión rápida a insuficiencia renal en 12-24 meses si no se trata.
¿Puedo llevar una vida normal con engrosamiento de la membrana basal glomerular?
Muchos pacientes con nefropatía membranosa, especialmente aquellos que logran la remisión (parcial o completa) o que tienen un buen control de la proteinuria y la función renal, pueden llevar una vida plena y activa. Es fundamental seguir las recomendaciones médicas, adherirse al tratamiento, mantener una dieta adecuada y controlar los factores de riesgo cardiovascular.
¿La nefropatía membranosa afecta solo a los riñones?
Aunque la nefropatía membranosa afecta principalmente a los riñones, las consecuencias del síndrome nefrótico pueden tener un impacto sistémico. La pérdida de proteínas afecta el equilibrio de fluidos y la coagulación de la sangre, lo que puede llevar a edema generalizado, mayor riesgo de trombosis (coágulos sanguíneos) y dislipidemia (niveles altos de colesterol), aumentando el riesgo de enfermedades cardiovasculares.
¿Cómo se monitorea la enfermedad después del diagnóstico?
El monitoreo es crucial e incluye revisiones regulares cada 1-2 meses inicialmente. Se controlan los niveles de proteinuria (en orina de 24 horas o relación proteína/creatinina en orina), la función renal (creatinina sérica, filtrado glomerular), los niveles de albúmina y lípidos en sangre. En pacientes con nefropatía membranosa primaria, el seguimiento de los títulos de anticuerpos anti-PLA2R es fundamental, ya que sus cambios pueden predecir la respuesta al tratamiento y el riesgo de recaídas.
Si quieres conocer otros artículos parecidos a Engrosamiento Glomerular: ¿Qué es y Cómo Afecta? puedes visitar la categoría Cabello.