08/04/2019
Nuestro cuerpo es una intrincada red de sistemas interconectados, y uno de los procesos más fundamentales para la vida, aunque a menudo pasa desapercibido, es la filtración capilar. Este mecanismo vital es el responsable de cómo los fluidos, nutrientes y desechos se mueven entre nuestra sangre y los tejidos que la rodean. Imagina tus capilares, esos diminutos vasos sanguíneos, como una serie de filtros microscópicos, constantemente ajustando el equilibrio de líquidos para asegurar que cada célula reciba lo que necesita y se deshaga de lo que no. Comprender la filtración capilar no solo nos revela la sofisticación de nuestra fisiología, sino que también nos ayuda a entender condiciones comunes como la hinchazón o el edema. En este artículo, desentrañaremos las causas detrás de este fascinante proceso, el nombre del líquido que emerge de él, y cómo su delicado equilibrio es crucial para nuestra salud.
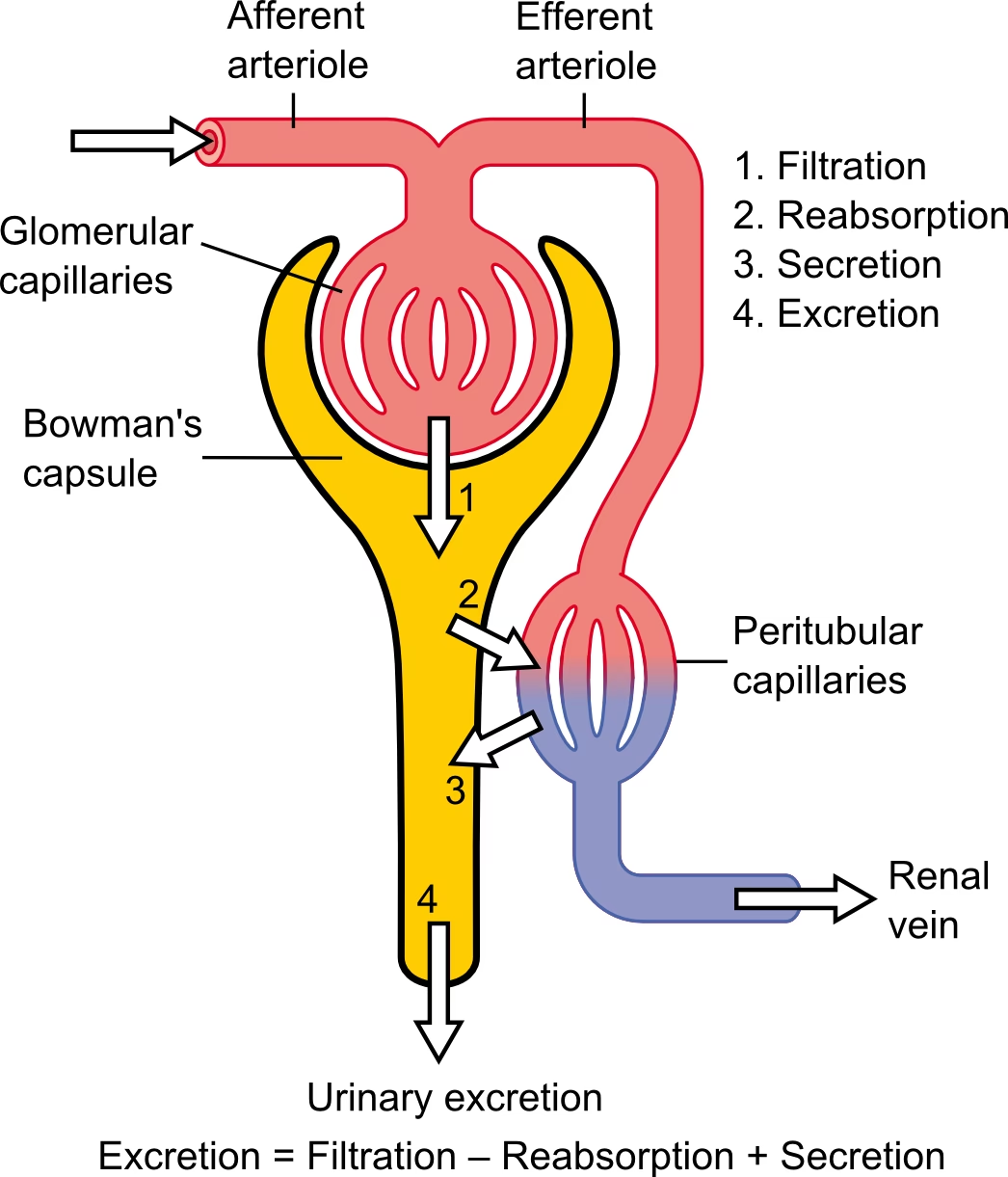
La filtración capilar, en su esencia, se refiere al movimiento neto de fluidos desde el torrente sanguíneo, específicamente desde los capilares y las vénulas postcapilares, hacia el espacio que rodea las células de los tejidos, conocido como intersticio. Este no es un flujo unidireccional o constante; es un proceso dinámico y regulado con precisión. Su propósito principal es multifacético: permite un recambio continuo del agua que baña las células de los tejidos, proporcionando el medio necesario para el transporte por difusión de oxígeno y nutrientes vitales para el metabolismo celular, al tiempo que facilita la eliminación de los subproductos metabólicos. Sin esta constante renovación, las células se asfixiarían o se envenenarían con sus propios desechos. Además, este flujo transcapilar de fluidos es fundamental para el funcionamiento del sistema linfático, que actúa como una vía de retorno crucial para las proteínas extravasadas y el exceso de líquido, garantizando que no se acumulen en el intersticio de forma perjudicial. Si no existiera este mecanismo de drenaje, la acumulación de proteínas en los espacios intersticiales pronto alteraría el equilibrio de fuerzas que regulan la filtración, llevando a una redistribución de volumen incompatible con la vida.
- Las Fuerzas de Starling: El Motor de la Filtración
- El Papel Crucial de la Albúmina y el Glicocálix
- ¿Cómo se Llama el Líquido que Sale de los Capilares?
- Cuando el Equilibrio se Rompe: La Formación de Edema
- Tipos de Capilares y su Impacto en la Filtración
- Regulación y Dinamismo de la Permeabilidad Capilar
- Preguntas Frecuentes sobre la Filtración Capilar
- Conclusión
Las Fuerzas de Starling: El Motor de la Filtración
Para comprender por qué ocurre la filtración, debemos adentrarnos en el concepto de las Fuerzas de Starling, que son los principios fundamentales que rigen el movimiento de fluidos a través de las paredes de los vasos sanguíneos. En 1896, Ernest Starling propuso que el movimiento de fluidos entre los compartimentos vasculares y tisulares cesaría cuando las fuerzas que gobiernan este movimiento estuvieran en equilibrio. A pesar de los avances y debates posteriores, sus ideas siguen siendo la base de nuestra comprensión.
Existen dos tipos principales de fuerzas que operan a través de las paredes microvasculares, y ambas tienen componentes tanto en el capilar como en el intersticio:
- La Presión Hidrostática (ΔP): Esta es la presión ejercida por el fluido dentro de un compartimento. En el contexto capilar, se refiere a la diferencia de presión entre el capilar (Pc) y el intersticio (Pt). Una presión hidrostática capilar más alta que la intersticial favorece la salida de fluido del vaso hacia el tejido. Bajo condiciones normales, la presión hidrostática capilar es la fuerza principal que impulsa el fluido fuera de los capilares. Curiosamente, la presión del líquido intersticial en muchos tejidos es ligeramente negativa en relación con la presión atmosférica en condiciones normales, lo que tiende a "tirar" el fluido hacia este espacio. Sin embargo, con el aumento de la hidratación del tejido, la presión del líquido intersticial se vuelve positiva, lo que favorece el movimiento del fluido hacia el compartimento vascular.
- La Presión Oncótica (Δπ): También conocida como presión coloidosmótica, esta fuerza es generada por la concentración de proteínas, especialmente la albúmina, en un compartimento. Las proteínas, al ser moléculas grandes, no pueden atravesar fácilmente la barrera capilar y, por lo tanto, ejercen una fuerza osmótica que tiende a "atraer" el agua hacia el compartimento donde están más concentradas. Así, la presión oncótica del plasma (en el capilar) tiende a arrastrar el fluido de vuelta al torrente sanguíneo, mientras que la presión oncótica del intersticio (debido a las proteínas que han escapado de los vasos) tiende a atraer el fluido hacia el espacio intersticial. La diferencia entre estas presiones determina la dirección neta del movimiento del fluido influenciado por las proteínas.
Además de estas presiones, otros factores cruciales que determinan el intercambio son el área de superficie (S) disponible para el intercambio y la conductividad hidráulica (Lp), que describe la "fuga" o permeabilidad de la barrera al agua. La ecuación de Starling moderna combina estos elementos, indicando que el flujo de volumen (Jv) es el resultado de la conductividad hidráulica multiplicada por el área de superficie y la presión neta de filtración (NFP), que es la suma de las fuerzas hidrostáticas y osmóticas efectivas. En condiciones de equilibrio, existe un ligero desequilibrio que favorece una filtración neta de fluido hacia los tejidos, lo cual es compensado por la eliminación de líquido intersticial a través de los linfáticos, manteniendo así el volumen de líquido intersticial constante.
El Papel Crucial de la Albúmina y el Glicocálix
Dentro de las fuerzas oncóticas, la albúmina juega un papel dominante. Es la proteína más abundante en el plasma y su tamaño relativamente pequeño, en comparación con otras proteínas plasmáticas, le permite tener una concentración comparativamente más alta en el líquido intersticial, debido a las características de "tamizado" de la barrera microvascular. Esto significa que la albúmina extravasada ejerce un mayor impacto en la presión coloidosmótica del tejido que otras proteínas plasmáticas en relación con su efecto sobre la presión oncótica del plasma.
Pero la historia de la barrera capilar no estaría completa sin mencionar una estructura fascinante: el Glicocálix. Esta capa, que recubre el endotelio luminal de todos los segmentos de la vasculatura, es una malla tridimensional de glicoproteínas y glicolípidos con carga negativa. Descubierto hace más de 40 años, el glicocálix ha ganado un interés de investigación intenso debido a su papel como barrera física para el flujo de solutos transvascular, su capacidad para influir en la adhesión y migración de leucocitos, y su función como mecanosensor para regular el tono vascular. Se ha propuesto que el glicocálix, y no toda la pared del vaso de intercambio, representa la barrera osmótica efectiva, lo que ha llevado a una reevaluación de la hipótesis original de Starling. Según esta visión más reciente, las fuerzas oncóticas de Starling se determinarían por la diferencia local de concentración de proteínas a través del glicocálix solo, y no por la diferencia global entre las presiones coloidosmóticas luminal y tisular. Esto subraya la complejidad y la regulación fina de la filtración capilar a un nivel molecular.
¿Cómo se Llama el Líquido que Sale de los Capilares?
Una de las preguntas más directas que surgen es: ¿Cómo se llama el líquido que sale de los capilares? La respuesta es sencilla: se conoce como Líquido Intersticial o líquido tisular. Este fluido, que es esencialmente una ultrafiltración del plasma sanguíneo, llena los espacios entre las células de los tejidos, proporcionando el medio acuoso necesario para que las células realicen sus funciones vitales. Contiene agua, iones, glucosa, aminoácidos y pequeñas cantidades de proteínas que han logrado atravesar la barrera capilar. Es en este líquido donde se produce el intercambio directo de nutrientes y oxígeno desde la sangre hacia las células, y de productos de desecho desde las células hacia el sistema circulatorio o linfático para su eliminación. El líquido intersticial es el "baño" constante en el que viven nuestras células, y su volumen y composición están rigurosamente controlados por la filtración capilar y el drenaje linfático.
Cuando el Equilibrio se Rompe: La Formación de Edema
El delicado equilibrio de la filtración capilar es crucial para mantener la homeostasis en nuestro cuerpo. Sin embargo, cuando este balance se altera, las consecuencias pueden ser evidentes. Una de las manifestaciones más comunes de un desequilibrio en la filtración capilar es la formación de Edema, que se define como la acumulación excesiva de líquido intersticial en los tejidos. El edema no es una enfermedad en sí misma, sino un síntoma o signo de una condición subyacente que ha perturbado los mecanismos de regulación de fluidos.
Las causas del edema son variadas y generalmente se pueden clasificar en alteraciones de las fuerzas de Starling o de la integridad de la barrera capilar:
- Aumento de la Presión Hidrostática Capilar: Si la presión dentro de los capilares aumenta significativamente (por ejemplo, en casos de hipertensión venosa, insuficiencia cardíaca congestiva o por una sobrecarga de volumen vascular), se favorece una mayor salida de líquido hacia el intersticio, superando la capacidad de drenaje linfático.
- Disminución de la Presión Oncótica Plasmática: Si la concentración de proteínas en el plasma disminuye (como en casos de desnutrición severa, enfermedades hepáticas que afectan la síntesis de albúmina o enfermedades renales que causan pérdida de proteínas en la orina), la fuerza que atrae el líquido de vuelta al capilar se debilita, lo que resulta en una mayor acumulación de líquido en el intersticio.
- Aumento de la Permeabilidad Capilar: En situaciones como la inflamación (por ejemplo, una lesión, infección o reacción alérgica), la barrera endotelial de los capilares puede volverse "más permeable" o "con fugas". Esto permite que no solo el agua, sino también una mayor cantidad de proteínas, salgan de los vasos hacia el intersticio. La presencia de más proteínas en el intersticio aumenta su presión oncótica, lo que a su vez atrae más líquido y contribuye significativamente al edema inflamatorio. Agentes inflamatorios como la histamina, bradicinina y el VEGF pueden inducir estos cambios en la permeabilidad.
- Obstrucción del Drenaje Linfático: El sistema linfático es la vía principal para el retorno del exceso de líquido y proteínas desde el intersticio a la circulación sanguínea. Si los vasos linfáticos se bloquean o dañan (por ejemplo, debido a una cirugía, infección parasitaria como la filariasis, o la extirpación de ganglios linfáticos en el tratamiento del cáncer), el líquido no puede ser drenado adecuadamente, lo que lleva a la acumulación y al edema.
El edema puede tener consecuencias tanto positivas como negativas. Por ejemplo, durante una respuesta inflamatoria, el aumento de la filtración de líquido capilar incrementa el flujo convectivo de macromoléculas como anticuerpos o proteínas del complemento activadas hacia el intersticio, lo que ayuda a combatir bacterias. Además, el aumento del volumen de líquido intersticial puede diluir sustancias químicas citotóxicas liberadas por microorganismos invasores o células dañadas. Sin embargo, un volumen expandido de líquido intersticial también aumenta la distancia de difusión para el oxígeno y otros nutrientes, lo que puede comprometer el metabolismo celular en el tejido edematoso. En órganos encapsulados, como el cerebro, el edema puede ser particularmente peligroso, ya que el cráneo óseo impide la expansión del tejido, lo que lleva a un aumento drástico de la presión intersticial, que a su vez puede comprimir los vasos cerebrales y comprometer el flujo sanguíneo, resultando en daño cerebral.
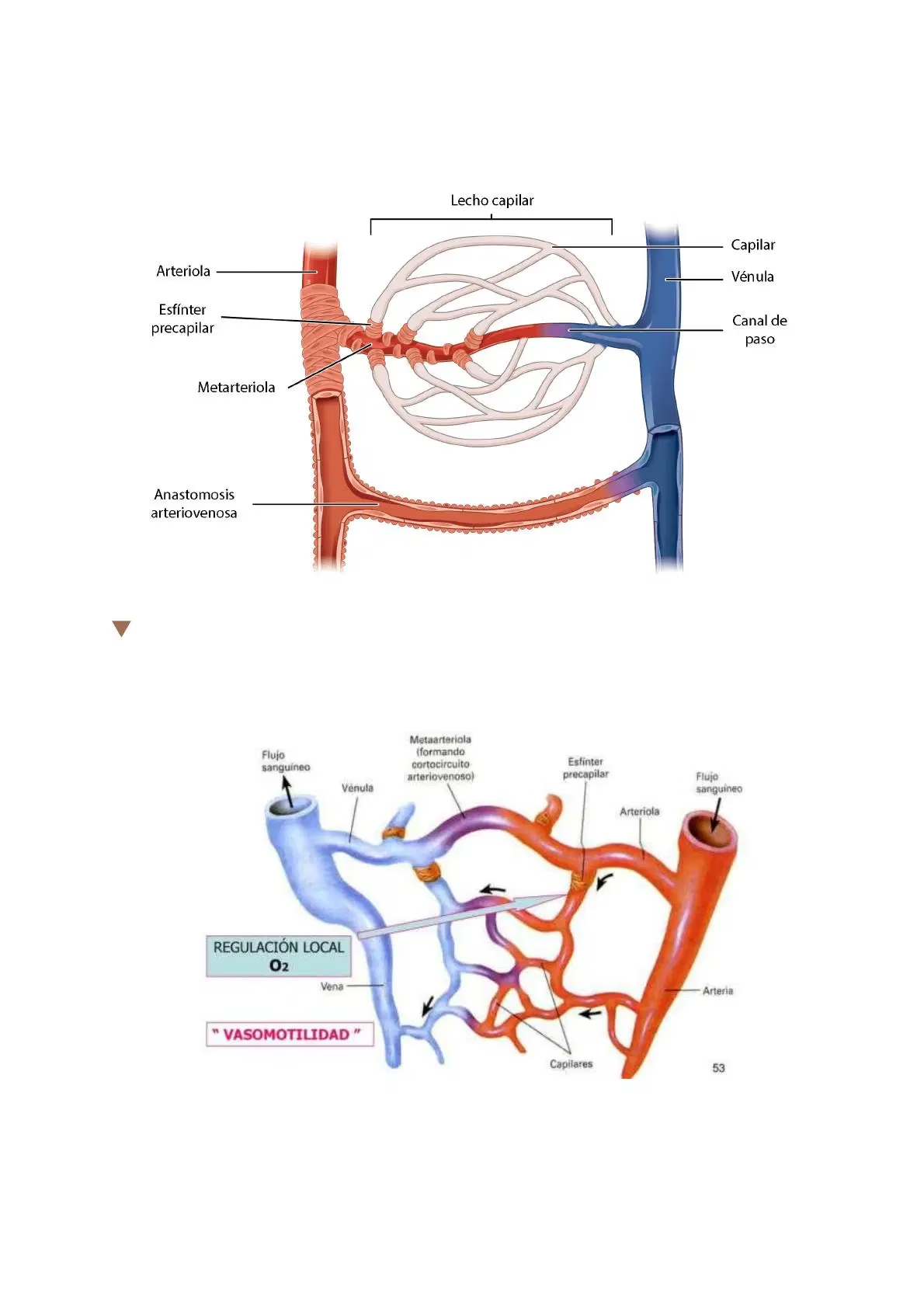
Tipos de Capilares y su Impacto en la Filtración
La morfología de los capilares no es uniforme en todo el cuerpo; varía significativamente entre órganos, lo que refleja sus funciones especializadas y el tipo de intercambio de fluidos y solutos que deben facilitar. Existen tres tipos principales de capilares:
| Tipo de Capilar | Características Morfológicas | Función y Ubicación Clave | Permeabilidad al Agua y Solutos Pequeños | Permeabilidad a Proteínas Grandes (Ej. Albúmina) |
|---|---|---|---|---|
| Capilares Continuos | Endotelio ininterrumpido con uniones intercelulares estrechas (tight junctions) y adherentes. Presencia de glicocálix y caveolas. | Los más comunes. Presentes en piel, músculo esquelético, pulmón, corazón. Forman barreras altamente restrictivas como la barrera hematoencefálica (BBB), barrera hematoacuosa (BAB) y barrera hemato-nerviosa (BNB). | Baja en barreras "estrechas" (BBB, etc.). Alta en piel/músculo. | Muy baja en barreras "estrechas". Baja en piel/músculo (σ ~ 0.8 o más). |
| Capilares Fenestrados | Endotelio con poros o "fenestraciones" (agujeros) que atraviesan las células, a veces cubiertos por un diafragma delgado. | Permiten un rápido intercambio de fluidos y solutos. Se encuentran en órganos con alta tasa de filtración o secreción, como riñones (glomérulos), glándulas endocrinas (tiroides, suprarrenales, pituitaria), páncreas exocrino, plexo coroideo y vellosidades intestinales. | Muy alta. | Moderada a alta (depende del diafragma). |
| Capilares Discontinuos (Sinusoides) | Grandes espacios o "brechas" entre las células endoteliales, y una membrana basal incompleta o ausente. | Permiten el paso de células sanguíneas y macromoléculas grandes. Ubicados en órganos donde se requiere un intercambio masivo o la migración de células, como el hígado, el bazo y la médula ósea. | Extremadamente alta. | Muy alta. |
La presencia de estas diferentes estructuras influye directamente en la permeabilidad y, por ende, en la filtración capilar. Por ejemplo, la barrera hematoencefálica, formada por capilares continuos extremadamente "herméticos", restringe drásticamente el movimiento de materiales entre la sangre y el cerebro, protegiéndolo de toxinas y fluctuaciones en la composición sanguínea. Sin embargo, en condiciones patológicas como el accidente cerebrovascular o la inflamación del SNC, esta barrera puede "abrirse", lo que lleva a un aumento de la permeabilidad y a la formación de edema cerebral, una condición particularmente peligrosa debido a la restricción del cráneo.
Regulación y Dinamismo de la Permeabilidad Capilar
Es fundamental entender que la permeabilidad de los microvasos no es una constante inmutable. Contrario a percepciones antiguas que la consideraban estática a menos que hubiera una lesión grave o inflamación, existe una considerable evidencia que demuestra que la permeabilidad vascular puede cambiar en cuestión de segundos en respuesta a hormonas reguladoras del volumen, como los péptidos natriuréticos auriculares, o a mediadores vasoactivos. Por ejemplo, la exposición a ciertos agentes inflamatorios no solo aumenta la conductividad hidráulica (Lp), haciendo la barrera más "permeable" al agua, sino que también reduce el coeficiente de reflexión osmótica (σ), lo que significa que la barrera se vuelve menos selectiva y permite que más proteínas grandes, como la albúmina, atraviesen. Estos cambios son cruciales en la respuesta inflamatoria, ya que facilitan la llegada de componentes inmunes al sitio de la lesión, pero también son la causa principal del edema asociado a la inflamación. Por otro lado, una reducción en la permeabilidad capilar, aunque pueda parecer beneficiosa, también puede ser perjudicial. Limitar el flujo de líquido hacia los espacios pericelulares puede reducir la eliminación de desechos metabólicos, como el ion hidrógeno y el lactato, lo que compromete la función celular y tisular. Por lo tanto, la filtración capilar es un proceso altamente dinámico, finamente regulado, que responde constantemente a las necesidades del cuerpo.
Preguntas Frecuentes sobre la Filtración Capilar
¿Es la filtración capilar siempre igual en todo el cuerpo?
No, la filtración capilar varía significativamente según el órgano y el tipo de capilar. Como hemos visto, los capilares continuos, fenestrados y discontinuos tienen diferentes grados de permeabilidad, lo que permite que cada tejido adapte el intercambio de fluidos y solutos a sus necesidades específicas. Por ejemplo, los capilares del riñón están diseñados para una filtración masiva, mientras que los del cerebro son extremadamente restrictivos.
¿Qué es la "reabsorción" en capilares?
Según la visión clásica de Starling, se creía que en el extremo arterial del capilar predominaba la filtración (salida de líquido) y en el extremo venoso, la reabsorción (entrada de líquido). Sin embargo, la investigación más reciente, especialmente en las últimas dos décadas, sugiere que en la mayoría de los lechos vasculares (con notables excepciones como el riñón y la mucosa intestinal), la reabsorción neta de líquido en el lado venoso de los capilares es insignificante o nula. En cambio, hay una filtración constante, aunque pequeña, a lo largo de la mayor parte del capilar, y el retorno de este líquido excedente y las proteínas al torrente sanguíneo se realiza casi exclusivamente a través del sistema linfático. La única excepción significativa a esta regla es el corazón, donde las presiones microvasculares fluctúan con cada latido, permitiendo periodos de reabsorción transitoria.
¿Cómo se mide la filtración capilar?
La medición de la filtración capilar y la permeabilidad de los vasos es un campo complejo de investigación. Métodos directos incluyen la canulación de microvasos con micropipetas para medir el flujo de volumen a diferentes presiones hidrostáticas. También se utilizan técnicas para evaluar la permeabilidad difusiva a solutos, a menudo empleando colorantes fluorescentes que permiten visualizar y cuantificar el movimiento de sustancias a través de la barrera capilar. Estos métodos avanzados han permitido desentrañar la intrincada regulación de la permeabilidad vascular.
¿Qué relación tiene con el sistema linfático?
La filtración capilar y el sistema linfático son dos caras de la misma moneda en el mantenimiento del equilibrio de fluidos. La filtración capilar produce constantemente líquido intersticial. Si no fuera por el drenaje linfático, este líquido se acumularía, provocando edema. El sistema linfático es la única vía para que el exceso de líquido intersticial, y especialmente las proteínas que han escapado de los capilares, regresen a la circulación sanguínea. Es vital para prevenir el edema y para el transporte de células inmunes.
¿La inflamación afecta la filtración capilar?
Sí, la inflamación es una de las principales condiciones que alteran drásticamente la filtración capilar. Durante una respuesta inflamatoria, se liberan mediadores químicos que aumentan la permeabilidad de los capilares y vénulas postcapilares. Esto significa que los vasos se vuelven más "permeables" o "con fugas", permitiendo que más líquido, proteínas e incluso células inmunes pasen de la sangre al tejido inflamado. Este aumento de la filtración contribuye directamente a la hinchazón (edema) y al enrojecimiento característicos de la inflamación.
Conclusión
En resumen, la filtración capilar es un pilar fundamental de la fisiología humana, un proceso incesante y finamente sintonizado que asegura el intercambio vital de sustancias entre la sangre y los tejidos. Impulsada por un delicado equilibrio de fuerzas hidrostáticas y oncóticas, y modulada por la intrincada estructura del glicocálix y los diferentes tipos de capilares, este mecanismo no solo nutre nuestras células y elimina sus desechos, sino que también juega un papel crítico en la respuesta del cuerpo a la lesión y la enfermedad. Comprender cómo funciona este sistema y qué sucede cuando se desequilibra, como en el caso del edema, nos ofrece una visión más profunda de la complejidad y resiliencia de nuestro organismo, y nos recuerda la importancia de mantener la salud vascular para el bienestar general.
Si quieres conocer otros artículos parecidos a Filtración Capilar: ¿Qué la Causa y Por Qué? puedes visitar la categoría Cabello.

