12/08/2020
El Síndrome de Dificultad Respiratoria Aguda (SDRA) es una condición devastadora que afecta a los pulmones, transformando su delicada estructura en un campo de batalla. En el corazón de esta enfermedad yace una alteración fundamental: el aumento de la permeabilidad capilar. Esta característica patológica es clave para entender por qué el SDRA es tan grave y cómo se manifiesta en los pacientes. Acompáñanos en este recorrido para desentrañar los misterios de esta compleja afección respiratoria.
- ¿Qué es el Síndrome de Dificultad Respiratoria Aguda (SDRA)?
- La Permeabilidad Capilar en el SDRA: Una Conexión Vital
- Fisiopatología Detallada: El Corazón del Problema
- Manifestaciones Clínicas del SDRA
- Factores de Riesgo y Caracterización del SDRA
- El Papel de la Genética en la Inflamación y el SDRA
- La Curva Presión-Volumen (PV) en el SDRA
- Preguntas Frecuentes (FAQ) sobre el SDRA
¿Qué es el Síndrome de Dificultad Respiratoria Aguda (SDRA)?
El SDRA se define como una lesión pulmonar aguda que puede surgir como consecuencia de un trauma severo, una infección sistémica (sepsis) o una hipoperfusión sostenida. Aunque a menudo se asocia con condiciones preexistentes, el SDRA puede desarrollarse incluso en ausencia de patología pulmonar subyacente. Es una condición de inicio rápido que lleva a una insuficiencia respiratoria aguda y se caracteriza por un daño generalizado a las células endoteliales capilares y a las células epiteliales alveolares.
A pesar de las diversas causas que pueden desencadenarlo, el SDRA comparte una patología común. Su tasa de mortalidad es alarmantemente alta, oscilando entre el 50% y el 60%, incluso con intervenciones intensivas. Históricamente, se le ha conocido por otros términos como edema pulmonar no cardiogénico, síndrome de dificultad respiratoria del adulto o pulmón de shock. Si bien en el pasado se creía que era puramente resultado de factores ambientales, hoy se reconoce que las respuestas inflamación individuales juegan un papel crucial en la extensión del problema y en la recuperación.
La Permeabilidad Capilar en el SDRA: Una Conexión Vital
La respuesta directa a la pregunta central es un rotundo sí: el SDRA aumenta significativamente la permeabilidad capilar. Este es uno de los sellos distintivos de la enfermedad y el mecanismo principal detrás de la acumulación de líquido en los pulmones.
El Síndrome de Fuga Capilar
En el SDRA, el daño a la membrana alvéolo-capilar, que normalmente es permeable solo a moléculas pequeñas, desencadena lo que se conoce como el síndrome de fuga capilar. Este proceso permite que proteínas y células, que normalmente se encuentran dentro de los vasos sanguíneos, escapen hacia los tejidos pulmonares, específicamente al intersticio y, finalmente, a los alvéolos. El intersticio del pulmón, que en condiciones normales se mantiene relativamente seco, se inunda.
Las consecuencias de esta fuga son múltiples y severas:
- Acumulación de Líquido Rico en Proteínas: El líquido que se acumula en los pulmones de los pacientes con SDRA no es solo agua, sino que contiene un alto nivel de proteínas plasmáticas. Esta presencia de proteínas aumenta la presión oncótica en el espacio intersticial y alveolar, atrayendo aún más líquido y perpetuando el edema.
- Alteraciones en la Coagulación: Algunas de las proteínas plasmáticas que se filtran incluyen tromboplastina, lo que puede aumentar la producción de coágulos y disminuir la fibrinólisis (la disolución de coágulos). Como resultado, se forman innumerables pequeños émbolos que permanecen en el pulmón, contribuyendo a la disfunción y al daño tisular. En algunos pacientes, la coagulación intravascular diseminada (CID) juega un papel importante.
- Daño Celular: La propia fuga de células y proteínas es un signo de daño. En las lesiones pulmonares directas, tanto los neumocitos tipo I como los tipo II (células productoras de surfactante) pueden resultar gravemente dañados o destruidos, junto con el daño capilar. Este daño, junto con la activación de macrófagos tisulares y leucocitos circulantes, es lo que precipita el síndrome de fuga capilar.
Fisiopatología Detallada: El Corazón del Problema
Las causas conocidas del SDRA son diversas y van más allá de trauma, sepsis y shock. Incluyen lesiones cerebrales, embolias grasas y de líquido amniótico, inhalación de gases tóxicos, oxigenoterapia excesiva, aspiración de sustancias altamente ácidas o básicas, transfusiones múltiples, bypass cardiopulmonar prolongado, ahogamiento cercano en agua dulce y pancreatitis aguda severa. Algunas de estas causas implican una lesión directa al tejido pulmonar, mientras que otras no involucran directamente el sistema respiratorio.
Un ejemplo de causa indirecta es cualquier condición que conduzca a hipoxia cerebral o un aumento repentino de la presión intracraneal. Esto puede provocar una descarga simpática masiva, llevando a una vasoconstricción sistémica con el movimiento de grandes volúmenes de sangre hacia la circulación pulmonar. El aumento de la presión hidrostática intrapulmonar conduce a cambios de líquidos y a una lesión pulmonar.
A pesar de las diferentes causas de lesión pulmonar en el SDRA, una respuesta inflamatoria sistémica es la vía común en su desarrollo. Por lo tanto, las manifestaciones del SDRA son similares independientemente de la causa. El principal sitio de lesión en el pulmón es la membrana alvéolo-capilar, que normalmente es permeable solo a moléculas pequeñas.

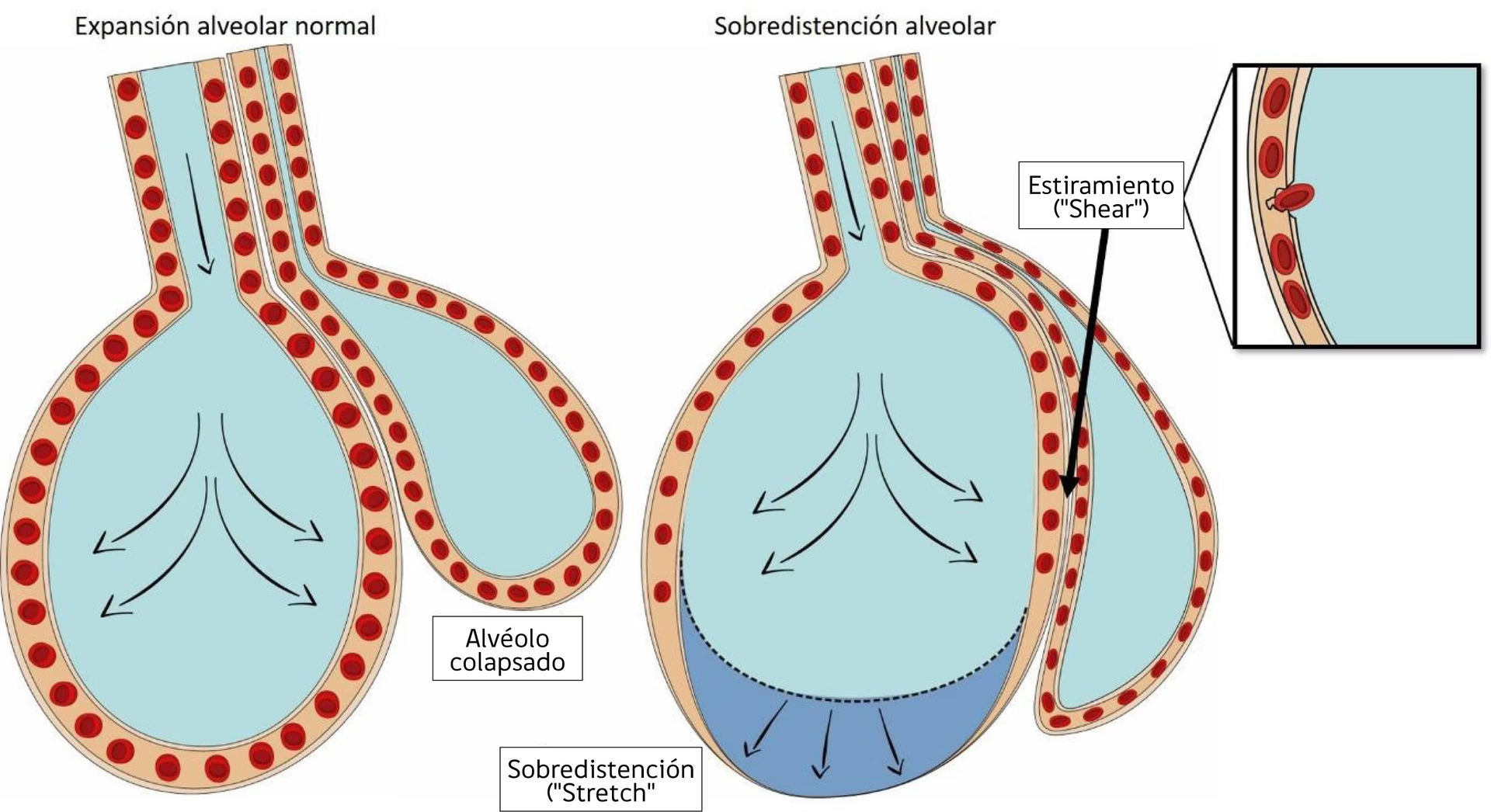
Disfunción del Surfactante y Colapso Alveolar
Además del daño capilar, ocurren otros cambios importantes en los alvéolos y los bronquiolos respiratorios. El neumocito tipo II es responsable de producir surfactante, una sustancia que mantiene la elasticidad del tejido pulmonar, reduce el retroceso excesivo y previene el colapso alveolar. La actividad del surfactante se reduce en el SDRA, ya sea porque los neumocitos tipo II están dañados o porque el surfactante se diluye por el exceso de líquidos pulmonares. Como resultado, los alvéolos se vuelven inestables y tienden a colapsar. Los alvéolos colapsados ya no pueden participar en el intercambio de gases, y se forma edema alrededor de las vías respiratorias terminales, las cuales se comprimen, cierran y son susceptibles a la destrucción o necrosis.
El volumen pulmonar se reduce aún más y la distensibilidad disminuye. A medida que el líquido continúa fugándose en más áreas pulmonares, el líquido, las proteínas y las células sanguíneas se acumulan en los alvéolos y en el espacio intersticial entre ellos. Los canales linfáticos se comprimen y se vuelven ineficaces. Los alvéolos mal ventilados reciben sangre pero no pueden oxigenarla, lo que aumenta el cortocircuito fisiológico. Esto resulta en hipoxemia y desequilibrio de la ventilación-perfusión.
Manifestaciones Clínicas del SDRA
El paciente típico con SDRA inicialmente presenta solo síntomas respiratorios leves a moderados que empeoran gradualmente, lo que resulta en un aumento del trabajo respiratorio. A medida que la respiración se vuelve más difícil, aparecen hiperpnea (respiración profunda y rápida), respiración con quejidos, cianosis (coloración azulada de la piel), palidez y retracciones intercostales o subesternales.
A medida que la hipoxia empeora, son comunes la diaforesis (sudoración excesiva), cambios en el estado mental, taquicardia y arritmias. Un punto importante es que, al principio, no se presentan sonidos pulmonares anormales en la auscultación porque el edema del SDRA ocurre primero en los espacios intersticiales y no en las vías respiratorias.
El diagnóstico de SDRA se establece por un valor de PaO2 (presión parcial de oxígeno arterial) disminuido, determinado por mediciones de gases en sangre arterial (GSA). Debido a que se desarrolla un gradiente de oxígeno alveolar ensanchado (un aumento de la fracción de oxígeno inspirado [FiO2] no conduce a un aumento de los niveles de PaO2) con un mayor cortocircuito sanguíneo, surge la necesidad de niveles más altos de oxígeno, aunque el paciente puede no responder a altas concentraciones de oxígeno y a menudo necesita intubación y ventilación mecánica.
La radiografía de tórax generalmente muestra una opacidad difusa o una apariencia blanquecina (vidrio esmerilado) del pulmón. La presión de enclavamiento capilar pulmonar suele ser baja o normal, lo que ayuda a diferenciar el SDRA del edema pulmonar de origen cardíaco. En algunos pacientes, la fibrosis pulmonar con progresión ocurre después de 10 días. Esta fase es irreversible y a menudo se denomina SDRA tardío o crónico. Las personas que desarrollan esta etapa y sobreviven tienen algún daño pulmonar permanente y pueden depender de la ventilación durante semanas o meses. Algunos pacientes pueden no ser destetados y permanecer dependientes de la ventilación mecánica por el resto de sus vidas.
Factores de Riesgo y Caracterización del SDRA
El SDRA puede ser causado por cualquier lesión directa o indirecta al pulmón. Algunas causas comunes incluyen:
- Inhalación de vómito a los pulmones (aspiración)
- Inhalación de químicos
- Trasplante de pulmón
- Neumonía, incluyendo infección a causa del COVID-19
- Shock séptico (infección en todo el cuerpo)
- Transfusiones (múltiples)
- Traumatismo
Según la cantidad de oxígeno en la sangre y al momento de respirar, la gravedad del SDRA se clasifica en:
- Leve
- Moderada
- Grave
Como se mencionó, el SDRA lleva a una acumulación de líquido en los sacos de aire (alvéolos). Este líquido impide el paso de suficiente oxígeno al torrente sanguíneo. La acumulación de líquido también hace que los pulmones se vuelvan pesados y rígidos. Esto disminuye la capacidad de los pulmones para expandirse. El nivel de oxígeno en la sangre puede permanecer peligrosamente bajo, incluso si la persona lo recibe de un respirador a través de una sonda de respiración. El SDRA a menudo se presenta junto con la insuficiencia de otros sistemas de órganos, como el corazón, el hígado o los riñones. El consumo de cigarrillo y de alcohol en exceso pueden ser factores de riesgo para su desarrollo.

El Papel de la Genética en la Inflamación y el SDRA
Si bien la sepsis y otras infecciones pulmonares parecen aumentar el riesgo de desarrollar SDRA cuando hay otras condiciones presentes, el papel de las respuestas inflamatorias está directamente relacionado con el resultado final de este problema. Cuanto más tiempo persistan las respuestas inflamatorias y más líquido se acumule en los pulmones, mayor será la probabilidad de que ocurra algún grado de fibrosis pulmonar.
Se ha observado una variación individual en las respuestas inflamatorias normalmente protectoras en todos los aspectos del proceso de inflamación. La secuencia comienza con la identificación de la presencia de lesión tisular o invasión microbiana, progresa a la estimulación inicial de citoquinas y células proinflamatorias, luego a acciones directas e indirectas de estos productos que cambian la expresión de varias vías de mejora y supresión, hasta las fases finales de curación celular y normalización de la función.
Los genes que regulan las respuestas inflamatorias son muchos y funcionan en un complicado conjunto interactivo de vías para asegurar una protección adecuada del proceso, al mismo tiempo que evitan las consecuencias de los excesos inflamatorios. Dichos productos génicos incluyen las diversas citoquinas, receptores de citoquinas, enzimas activadoras e inhibidoras, factores de crecimiento y sustancias de señalización para activar vías productoras de energía. Al igual que el sistema enzimático del citocromo P450, las vías genéticas involucradas en la evocación y regulación de las respuestas inflamatorias están sujetas a mutaciones que desequilibran la regulación, permitiendo que algunos individuos sean 'hiper-respondedores' a los desencadenantes inflamatorios. Dichos individuos son teóricamente más susceptibles genéticamente a respuestas inflamatorias prolongadas y dañinas para los tejidos, las cuales se sabe que estimulan la fibrosis excesiva y la formación de tejido cicatricial.
El procesamiento del colágeno durante la inflamación parece desempeñar un papel en si el proceso conduce o no a una fibrosis irreversible. La presencia continua de algunas formas de colágeno o metabolitos de colágeno permite una señalización más constante de factores proinflamatorios. Un estudio pudo encontrar una asociación entre el aumento de los niveles sanguíneos de biomarcadores específicos para el metabolismo del colágeno y una progresión más rápida a través de las etapas del SDRA y el desarrollo de fibrosis. El colágeno y sus metabolitos representan productos génicos. Aunque la fuente o el desencadenante del metabolismo excesivo del colágeno puede no residir dentro de los genes del colágeno, es probable que una variación genética en algún producto involucrado en la inflamación conduzca a una transcripción excesiva de los genes del colágeno.
La Curva Presión-Volumen (PV) en el SDRA
La curva presión-volumen (PV) es una herramienta fisiológica propuesta para fines de diagnóstico o monitoreo durante la ventilación mecánica del síndrome de dificultad respiratoria aguda. La reducción en la distensibilidad (compliance) medida por la curva PV y los diferentes puntos de inflexión en la curva se consideran marcadores interesantes de la gravedad y de los niveles de presión de apertura y cierre pulmonar. Trazar una curva, sin embargo, puede influir en el grado de apertura o distensión del pulmón, y la interpretación de la curva debe tener en cuenta este efecto.
La forma clásica de la curva PV en pacientes con SDRA es más o menos sigmoidea, con una pendiente general (es decir, la distensibilidad del sistema respiratorio) notablemente reducida en comparación con sujetos normales. La curva se obtiene insuflando lentamente el tórax, ya sea de forma continua o en una serie de pequeños pasos. Generalmente se considera que la curva PV consta de tres segmentos separados por dos puntos de inflexión. El primer segmento, caracterizado por baja distensibilidad, se separa de una parte más lineal de la curva por el punto de inflexión inferior. El segmento intermedio puede considerarse lineal y se utiliza para medir la distensibilidad 'lineal' entre el punto de inflexión inferior y el punto de inflexión superior. Más allá del punto de inflexión superior, la curva PV tiende a aplanarse nuevamente.
La reducción de la distensibilidad lineal medida por la curva PV se considera un sello distintivo del SDRA y generalmente se explica principalmente por la pérdida de volumen pulmonar aireado. Sin embargo, las áreas pulmonares con una apariencia normal en las radiografías simples muestran aumentos en el tejido pulmonar a pesar de la aireación preservada en las imágenes de tomografía computarizada, lo que indica que las alteraciones del tejido pulmonar son difusas en el SDRA.

Recientemente se describió una correlación débil pero significativa entre la distensibilidad y los marcadores de recambio de colágeno, con un patrón logarítmico consistente con un modelo de distensión máxima dependiente del colágeno. Este modelo sugiere que, hasta que la deposición de colágeno alcanza un nivel umbral, la distensibilidad no se ve influenciada o solo ligeramente influenciada por el recambio de colágeno. Una reducción de la distensibilidad hasta alrededor de 30 ml/cmH2O es, por lo tanto, esencialmente resultado de una reducción del volumen pulmonar. La distensibilidad más allá de este valor también puede estar limitada por la deposición de colágeno, lo que a nivel celular se denomina 'distensión máxima dependiente del colágeno'.
Preguntas Frecuentes (FAQ) sobre el SDRA
¿El SDRA es contagioso?
No, el SDRA en sí mismo no es contagioso. Sin embargo, las condiciones subyacentes que pueden causarlo, como ciertas infecciones (por ejemplo, neumonía bacteriana o viral, incluyendo COVID-19), sí pueden ser contagiosas.
¿Se puede prevenir el SDRA?
No existe una forma específica de prevenir el SDRA directamente, ya que a menudo es una complicación de otras enfermedades graves o traumas. La prevención se centra en el manejo y tratamiento oportuno de las condiciones subyacentes que pueden llevar a su desarrollo, como la sepsis, la neumonía o las lesiones traumáticas.
¿Cuál es el tratamiento principal para el SDRA?
El tratamiento principal para el SDRA es el soporte vital, que incluye la ventilación mecánica para ayudar al paciente a respirar y mantener niveles adecuados de oxígeno. Además, se busca tratar la causa subyacente del SDRA y manejar las complicaciones, como las infecciones o la disfunción de otros órganos.
¿Cuánto tiempo dura el SDRA?
La duración del SDRA varía significativamente entre los pacientes. En casos leves, la recuperación puede ocurrir en días o semanas. Sin embargo, en casos graves, especialmente si se desarrolla fibrosis pulmonar, la enfermedad puede prolongarse durante semanas o meses, y algunos pacientes pueden requerir ventilación mecánica a largo plazo o sufrir daño pulmonar permanente.
¿Qué significa el término 'pulmón de shock'?
'Pulmón de shock' es un término antiguo y menos utilizado para referirse al Síndrome de Dificultad Respiratoria Aguda (SDRA). Se utilizaba para describir la insuficiencia pulmonar que a menudo se observa en pacientes que han experimentado un shock severo, reflejando la naturaleza sistémica y el impacto en múltiples órganos que puede tener esta condición.
Si quieres conocer otros artículos parecidos a SDRA: ¿Aumenta la Permeabilidad Capilar? puedes visitar la categoría Cabello.
