29/06/2021
En nuestro día a día, estamos rodeados de fenómenos que, aunque parezcan simples, encierran principios físicos fascinantes. Uno de ellos es la acción capilar, una propiedad de los líquidos que les permite ascender o descender por tubos estrechos, desafiando a menudo la gravedad. Este fenómeno, crucial en la naturaleza y la tecnología, se manifiesta de maneras distintas y sorprendentes cuando comparamos líquidos como el agua y el mercurio. Comprender estas diferencias no solo nos abre una ventana a la física de fluidos, sino que también nos permite apreciar cómo estas interacciones microscópicas tienen un impacto gigante en el mundo que nos rodea, e incluso, en la forma en que el agua interactúa con nuestro propio cabello.

La capilaridad es el resultado de la interacción entre las fuerzas de cohesión (atracción entre moléculas del mismo tipo de líquido) y las fuerzas de adhesión (atracción entre las moléculas del líquido y las de la superficie sólida con la que está en contacto). Es este delicado equilibrio, o desequilibrio, el que dicta el comportamiento de un líquido en un capilar.
- ¿Qué es la Acción Capilar? El Baile de las Moléculas
- La Acción Capilar en el Agua: Un Ascenso Sorprendente
- La Acción Capilar en el Mercurio: Un Descenso Inesperado
- Factores que Influyen en la Acción Capilar
- Aplicaciones de la Capilaridad: Más Allá del Laboratorio
- Capilaridad y el Cabello: Una Conexión Sorprendente
- Tabla Comparativa: Agua vs. Mercurio en la Capilaridad
- Preguntas Frecuentes sobre la Capilaridad
- Conclusión: La Magia de lo Pequeño
¿Qué es la Acción Capilar? El Baile de las Moléculas
La acción capilar, o capilaridad, es la capacidad de un líquido para fluir en espacios estrechos sin la ayuda de fuerzas externas, o incluso en oposición a ellas, como la gravedad. Este efecto es particularmente evidente en tubos muy delgados, conocidos como capilares. La clave para entender este fenómeno reside en la tensión superficial y en las fuerzas intermoleculares.
Fuerzas de Cohesión y Adhesión: Los Protagonistas
Para comprender por qué el agua y el mercurio se comportan de forma tan diferente, es fundamental entender dos tipos de fuerzas moleculares:
- Fuerzas de Cohesión: Son las fuerzas de atracción entre moléculas del mismo tipo. Por ejemplo, las moléculas de agua se atraen entre sí, y las moléculas de mercurio se atraen entre sí. Una alta cohesión significa que las moléculas prefieren estar juntas.
- Fuerzas de Adhesión: Son las fuerzas de atracción entre moléculas de diferentes tipos. En el contexto de la capilaridad, se refieren a la atracción entre las moléculas del líquido y las moléculas de la superficie sólida (como el vidrio de un tubo capilar). Una alta adhesión significa que las moléculas del líquido prefieren "pegarse" a la superficie.
La tensión superficial, por su parte, es una consecuencia directa de las fuerzas de cohesión. Es la energía requerida para aumentar la superficie de un líquido, y es lo que hace que la superficie de un líquido se comporte como una membrana elástica.
La Acción Capilar en el Agua: Un Ascenso Sorprendente
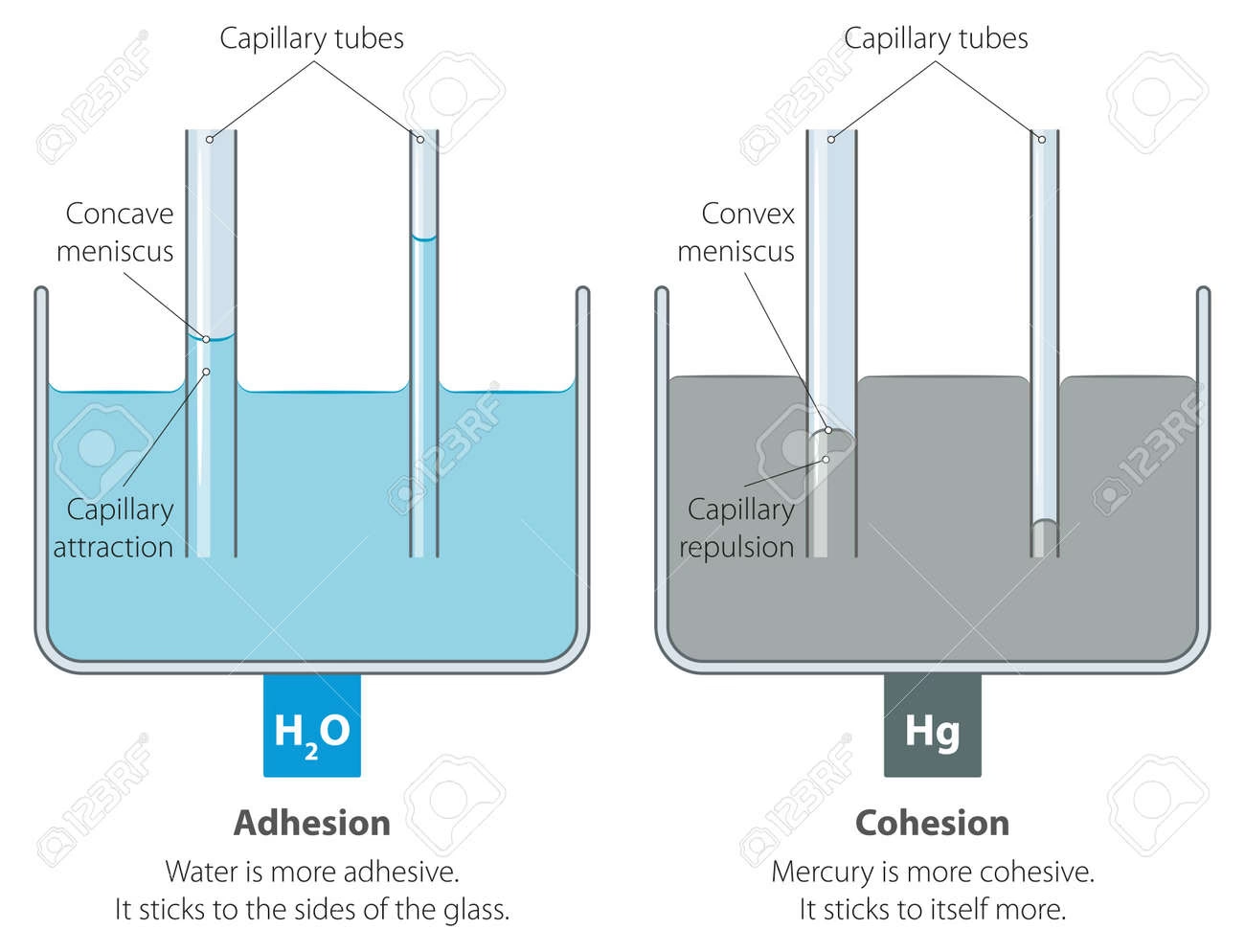
Cuando el agua entra en contacto con una superficie, como el vidrio de un tubo capilar, se observa un fenómeno muy particular: el nivel del agua dentro del tubo asciende por encima del nivel general del agua circundante. Además, la superficie del agua en contacto con el tubo forma una curva hacia abajo, conocida como menisco cóncavo.
¿Por qué el Agua Asciende y Forma un Menisco Cóncavo?
La explicación radica en la relación entre sus fuerzas de cohesión y adhesión. En el caso del agua:
- Adhesión > Cohesión: Las fuerzas de adhesión entre las moléculas de agua y las moléculas de la superficie del vidrio (que es hidrofílica, es decir, atrae el agua) son más fuertes que las fuerzas de cohesión entre las propias moléculas de agua.
- Ascenso Capilar: Debido a que el agua se siente más atraída por el vidrio que por sí misma, las moléculas de agua en la periferia son "arrastradas" hacia arriba por las paredes del tubo. A medida que estas moléculas suben, arrastran consigo a las moléculas inferiores debido a la cohesión, creando una columna ascendente de agua.
- Menisco Cóncavo: La fuerte adhesión a las paredes del tubo hace que el agua se eleve ligeramente en los bordes, mientras que la tensión superficial (resultado de la cohesión) intenta minimizar la superficie, tirando del centro hacia abajo. Esta combinación crea la característica forma de menisco cóncavo, donde el centro de la superficie está más bajo que los bordes.
Este ascenso capilar es fundamental en la naturaleza. Es el mecanismo por el cual las plantas absorben agua desde las raíces hasta las hojas, desafiando la gravedad a través de los pequeños vasos capilares de su tallo. También es lo que permite que una toalla absorba agua o que la tinta fluya por un bolígrafo.
La Acción Capilar en el Mercurio: Un Descenso Inesperado
A diferencia del agua, el mercurio (un metal líquido a temperatura ambiente) se comporta de manera opuesta cuando se encuentra en un tubo capilar. En lugar de ascender, el nivel del mercurio dentro del tubo desciende por debajo del nivel general del mercurio circundante. Y en lugar de un menisco cóncavo, forma una curva hacia arriba, conocida como menisco convexo.
¿Por qué el Mercurio Desciende y Forma un Menisco Convexo?
El comportamiento del mercurio se explica por la dominancia de sus fuerzas de cohesión sobre las de adhesión:
- Cohesión > Adhesión: Las fuerzas de cohesión entre las propias moléculas de mercurio son mucho más fuertes que las fuerzas de adhesión entre el mercurio y la superficie del vidrio. Las moléculas de mercurio tienen una fuerte atracción entre sí y una baja tendencia a adherirse a la mayoría de las superficies.
- Descenso Capilar: Dado que el mercurio prefiere estar consigo mismo que en contacto con el vidrio, las moléculas en la periferia son "repelidas" de las paredes del tubo. Esto provoca que el nivel del mercurio dentro del capilar descienda.
- Menisco Convexo: La fuerte cohesión hace que las moléculas de mercurio se agrupen y minimicen el contacto con las paredes del tubo. La tensión superficial, al intentar reducir el área de contacto con el aire, tira de los bordes hacia abajo y empuja el centro hacia arriba, formando un menisco convexo, donde el centro de la superficie está más alto que los bordes.
Este comportamiento es la razón por la que el mercurio es ideal para termómetros tradicionales: su alta tensión superficial y su tendencia a no adherirse al vidrio permiten mediciones precisas sin que el líquido se adhiera a las paredes del capilar.
Factores que Influyen en la Acción Capilar
La magnitud de la acción capilar no es constante y depende de varios factores:
- Diámetro del Tubo: Cuanto más estrecho sea el diámetro del capilar, mayor será la altura a la que ascenderá (o descenderá) el líquido. Esta relación es inversamente proporcional: a menor diámetro, mayor efecto.
- Naturaleza del Líquido: Las propiedades intrínsecas del líquido, como su tensión superficial, densidad y las fuerzas relativas de cohesión y adhesión, son determinantes. Líquidos con alta tensión superficial y fuerte adhesión (como el agua) ascienden más.
- Naturaleza de la Superficie Sólida: La composición de la superficie con la que el líquido está en contacto (si es hidrofílica o hidrofóbica) influye directamente en las fuerzas de adhesión.
- Temperatura: La tensión superficial de los líquidos generalmente disminuye con el aumento de la temperatura. Esto significa que la acción capilar tiende a ser menos pronunciada a temperaturas más altas.
Aplicaciones de la Capilaridad: Más Allá del Laboratorio
La capilaridad es un principio fundamental con innumerables aplicaciones y manifestaciones:
- En la Naturaleza: Vital para el transporte de agua y nutrientes en las plantas, la absorción de agua por el suelo, y la forma en que el rocío se adhiere a las hojas.
- En el Hogar: Las esponjas, las toallas de papel y los paños de limpieza funcionan gracias a la capilaridad, absorbiendo líquidos en sus pequeñas fibras.
- En la Industria: La impresión por inyección de tinta, la lubricación en maquinaria, y la fabricación de ciertos materiales porosos dependen de este fenómeno.
- En la Medicina: La capilaridad es clave en la absorción de medicamentos por el cuerpo y en algunos dispositivos de diagnóstico.
Capilaridad y el Cabello: Una Conexión Sorprendente
Como escritores de artículos sobre cabello, es fascinante considerar cómo la capilaridad juega un papel, aunque sutil, en la interacción de nuestro cabello con el agua y los productos. Cada hebra de cabello, aunque no es un tubo capilar en el sentido estricto, tiene una superficie porosa y una estructura que permite la absorción y retención de humedad.
Cuando el cabello está mojado, el agua puede ser atraída hacia el interior de la cutícula y la corteza a través de fenómenos que se asemejan a la capilaridad, especialmente si el cabello está dañado y sus capas externas están levantadas. Esta capacidad de absorción es crucial para la hidratación del cabello, pero también para la efectividad de los productos capilares.
- Absorción de Productos: Los tratamientos acondicionadores, mascarillas y aceites se distribuyen y absorben en cierta medida gracias a la afinidad de sus moléculas con la superficie del cabello, similar a la adhesión. La acción capilar puede influir en cómo el agua o los productos se difunden a través de las microestructuras del cabello.
- Hidratación: Un cabello bien hidratado es un cabello sano. La forma en que el agua es atraída y retenida por el cabello es una forma de capilaridad, donde las moléculas de agua se adhieren a las proteínas de la queratina.
- Secado del Cabello: El proceso de secado también implica la liberación de agua del cabello. Entender cómo el agua interactúa con la superficie del cabello puede ayudar a desarrollar técnicas y productos que optimicen la hidratación sin dejar el cabello empapado o encrespado.
Aunque el cabello no es un capilar de vidrio, la interacción de las moléculas de agua con su superficie y sus estructuras internas comparte principios fundamentales con la adhesión y la cohesión que gobiernan la capilaridad en tubos.
Tabla Comparativa: Agua vs. Mercurio en la Capilaridad
| Característica | Agua (H₂O) | Mercurio (Hg) |
|---|---|---|
| Fuerzas Dominantes | Adhesión > Cohesión | Cohesión > Adhesión |
| Comportamiento en Capilar | Asciende | Desciende |
| Forma del Menisco | Cóncavo | Convexo |
| Atracción por el Vidrio | Alta (Mojante) | Baja (No Mojante) |
| Tensión Superficial | Relativamente alta | Muy alta |
Preguntas Frecuentes sobre la Capilaridad
¿Por qué el menisco del agua es cóncavo y el del mercurio es convexo?
El menisco del agua es cóncavo porque las fuerzas de adhesión entre el agua y la superficie del recipiente (como el vidrio) son más fuertes que las fuerzas de cohesión entre las propias moléculas de agua. El agua se "pega" a las paredes y sube por los bordes. Por el contrario, el menisco del mercurio es convexo porque sus fuerzas de cohesión son mucho más fuertes que sus fuerzas de adhesión al recipiente. El mercurio prefiere estar consigo mismo y minimiza el contacto con la superficie, formando una cúpula.
¿La capilaridad solo ocurre en tubos muy delgados?
La capilaridad es más evidente y significativa en tubos de diámetro muy pequeño (capilares) porque la relación entre la superficie de contacto (donde actúan las fuerzas de adhesión) y el volumen del líquido es mayor. Sin embargo, el fenómeno de tensión superficial y las interacciones de cohesión/adhesión ocurren en cualquier superficie de contacto entre un líquido y un sólido, aunque sus efectos sean menos dramáticos en recipientes anchos.
¿Cómo afecta la temperatura a la capilaridad?
Generalmente, un aumento de la temperatura disminuye la tensión superficial de un líquido, ya que las moléculas tienen más energía cinética y las fuerzas de cohesión se debilitan. Como resultado, la altura a la que un líquido puede ascender (o descender) por acción capilar también disminuye con el aumento de la temperatura.
¿Es la capilaridad importante en el cuerpo humano?
Sí, la capilaridad es crucial en el cuerpo humano. Por ejemplo, los capilares sanguíneos, que son vasos sanguíneos extremadamente pequeños, permiten el intercambio de nutrientes, oxígeno y desechos entre la sangre y los tejidos. Aunque el flujo sanguíneo es impulsado principalmente por el corazón, las propiedades capilares de la sangre y los vasos juegan un papel en la eficiencia de este intercambio.
¿Qué significa que un líquido sea "mojante" o "no mojante"?
Un líquido es "mojante" si las fuerzas de adhesión entre el líquido y la superficie sólida son lo suficientemente fuertes como para que el líquido se extienda sobre la superficie, formando un ángulo de contacto agudo (como el agua en vidrio limpio). Un líquido es "no mojante" si las fuerzas de cohesión dentro del líquido son más fuertes que las de adhesión a la superficie, lo que hace que el líquido forme gotas y no se extienda (como el mercurio en vidrio, o el agua en una superficie encerada).
Conclusión: La Magia de lo Pequeño
La acción capilar es un testimonio de cómo las fuerzas fundamentales a nivel molecular dan forma a nuestro mundo. Desde el ascenso de la savia en el árbol más alto hasta la forma en que una gota de lluvia se adhiere a una ventana, o cómo los productos de belleza penetran en la fibra de nuestro cabello, la interacción entre la cohesión y la adhesión es una fuerza omnipresente. Entender las diferencias entre el agua y el mercurio en este contexto no solo nos ilumina sobre la física de los fluidos, sino que también nos invita a apreciar la complejidad y la belleza oculta en los fenómenos más cotidianos. La capilaridad es un recordatorio de que, a menudo, los mayores impactos provienen de las interacciones más pequeñas y sutiles.
Si quieres conocer otros artículos parecidos a La Danza Invisible: Capilaridad en Agua y Mercurio puedes visitar la categoría Cabello.