07/04/2012
En el vasto universo de la química analítica, la capacidad de separar y cuantificar componentes individuales de una mezcla es fundamental. Entre las diversas técnicas disponibles, la Electroforesis Capilar (CE, por sus siglas en inglés) se ha consolidado como una herramienta extraordinariamente potente y versátil. Esta técnica, que aprovecha las propiedades eléctricas de las moléculas, permite una resolución y sensibilidad superiores en comparación con otros métodos, abriendo puertas a descubrimientos en campos tan diversos como la medicina, la biotecnología y la ciencia de los alimentos.

Acompáñenos en este profundo recorrido para comprender qué es la electroforesis capilar, cómo funciona a nivel molecular, los pasos prácticos para su implementación en el laboratorio y sus múltiples aplicaciones que están transformando la investigación y el control de calidad en la actualidad.
- ¿Qué es la Electroforesis Capilar y Cómo Funciona?
- Análisis de Resultados: El Electroferograma
- Realizando la Electroforesis Capilar en el Laboratorio: Un Ejemplo Práctico
- Aplicaciones Avanzadas de la Electroforesis Capilar
- ¿Se puede utilizar la Electroforesis Capilar para separar Aminoácidos?
- Tabla Comparativa: CE vs. Cromatografía Líquida de Alta Resolución (HPLC)
- Preguntas Frecuentes sobre la Electroforesis Capilar
¿Qué es la Electroforesis Capilar y Cómo Funciona?
La electroforesis capilar es una técnica analítica utilizada para separar moléculas en un campo eléctrico. Su principio básico se centra en la diferencia de velocidad a la que se mueven las moléculas a través de un capilar estrecho, influenciadas por su carga, tamaño y la viscosidad del disolvente. A diferencia de otras técnicas de separación, la CE se distingue por su alta eficiencia y su capacidad para trabajar con volúmenes de muestra extremadamente pequeños.
El corazón de un sistema de CE es un tubo de diámetro submilimétrico, conocido como capilar, que contiene una solución de electrolito que fluye. Una vez que la muestra se inyecta en este capilar, se aplica un campo eléctrico a través de sus extremos. Este campo eléctrico induce una carga positiva en la entrada del capilar y una carga negativa en la salida, creando un gradiente de potencial que impulsa el movimiento de las moléculas.
El Fenómeno del Flujo Electroosmótico (EOF)
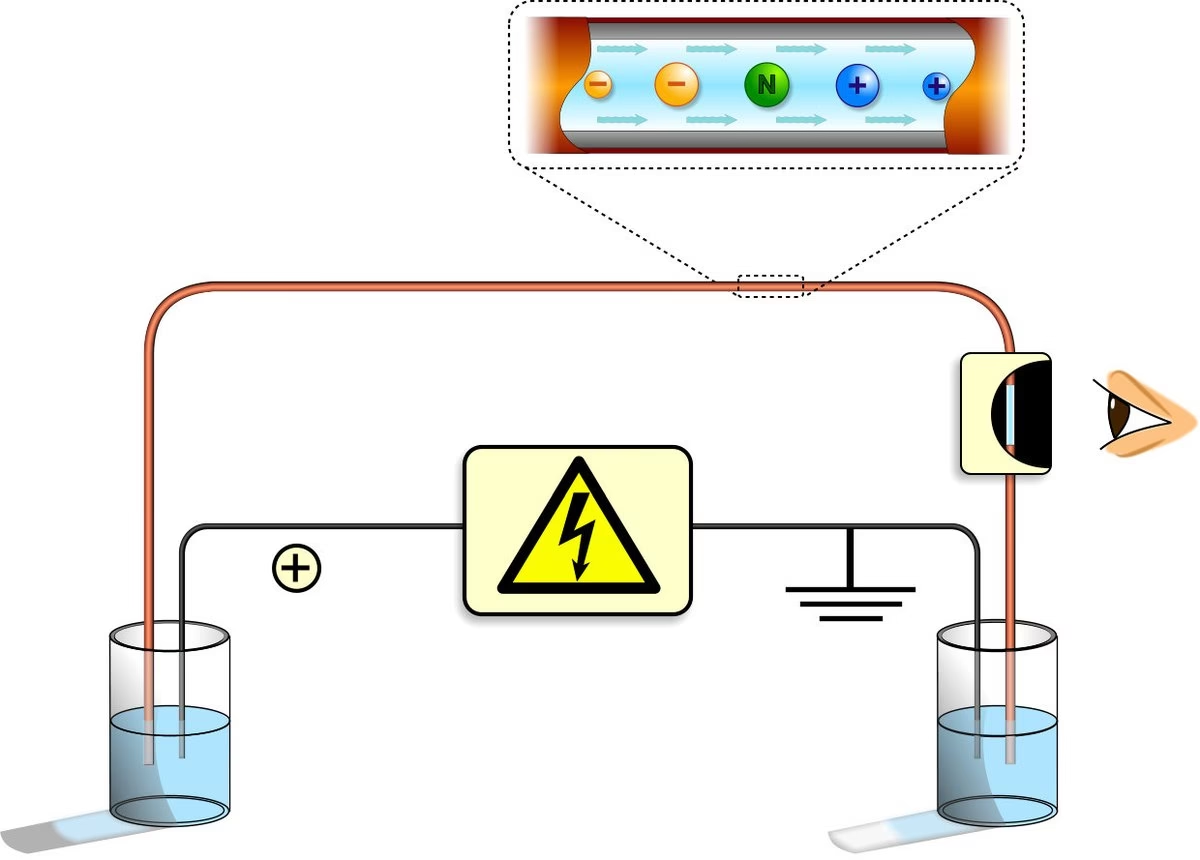
Uno de los conceptos clave para entender la CE es el flujo electroosmótico (EOF). Este flujo es el movimiento global del electrolito dentro del capilar, inducido por el campo eléctrico. Se origina debido a la interacción entre la pared interna del capilar (que generalmente tiene grupos silanol cargados negativamente en su superficie) y los iones positivos del electrolito. Los cationes se acumulan cerca de la pared del capilar formando una capa discreta. Cuando se aplica el campo eléctrico, estos cationes se mueven hacia el extremo negativo del capilar, arrastrando consigo toda la solución en el centro del tubo. Este arrastre de la solución a granel es lo que conocemos como flujo electroosmótico.
Movilidad Electroforética y Separación Molecular
Mientras el EOF transporta la solución a través del capilar, las moléculas de la muestra se separan en función de su velocidad individual, un parámetro conocido como movilidad electroforética. Esta velocidad depende directamente de la carga y el tamaño de las moléculas, así como de cuán fuertemente son atraídas o repelidas por el campo eléctrico.
- Las moléculas cargadas positivamente (cationes) se mueven más rápido a través del capilar porque son fuertemente atraídas por el potencial negativo en la salida, y su movimiento se suma al EOF.
- Las moléculas neutras son transportadas junto con el flujo a granel del EOF, ya que no son directamente atraídas ni repelidas por el campo eléctrico.
- Las moléculas cargadas negativamente (aniones) fluyen mucho más lento. Aunque son arrastradas por el EOF hacia la salida, su atracción por el potencial positivo en la entrada del capilar las frena significativamente, pudiendo incluso moverse en dirección opuesta al EOF si su carga es muy elevada.
Por lo tanto, el orden típico de las moléculas que salen del capilar es: primero las cargadas positivamente, luego las neutras y finalmente las cargadas negativamente. Además de la carga, el tamaño también juega un papel crucial: el flujo de electrolito tira de las moléculas más pequeñas más rápido que las moléculas más grandes debido a las fuerzas de fricción, lo que añade otra dimensión a la separación.
Análisis de Resultados: El Electroferograma
A medida que las moléculas separadas salen del capilar, son detectadas por un detector, comúnmente de UV-Vis, que mide la absorbancia de la luz a una longitud de onda específica. La señal del detector se registra y se visualiza en un gráfico que muestra la intensidad de la señal frente al tiempo de elución. Este gráfico se denomina electroferograma.
Los electroferogramas son una fuente rica de información. Cada pico en el electroferograma corresponde a un componente diferente en la muestra, y la posición del pico (tiempo de elución) es característica de esa molécula bajo las condiciones de análisis. La altura o el área del pico son proporcionales a la cantidad de cada sustancia presente en la muestra, lo que permite una cuantificación precisa. De esta manera, un solo electroferograma puede revelar la composición cualitativa y cuantitativa de una mezcla compleja.
Realizando la Electroforesis Capilar en el Laboratorio: Un Ejemplo Práctico
Para ilustrar cómo se lleva a cabo la electroforesis capilar, consideremos un ejemplo común: determinar la composición de un refresco. El proceso general implica varios pasos:
1. Preparación del Instrumento y Configuración de Parámetros
Primero, se enciende el instrumento de electroforesis capilar y la computadora asociada. Es crucial encender el detector UV con antelación para que se caliente y estabilice.
A continuación, se configuran los parámetros del experimento en el software del instrumento:
- Temperatura: La temperatura del compartimento del cartucho y del almacenamiento de la muestra se ajusta, por ejemplo, a 35°C para asegurar la reproducibilidad y optimizar la separación.
- Detección UV: Se selecciona la longitud de onda de detección, típicamente 214 nm, que es adecuada para muchos compuestos orgánicos.
- Pasos de Enjuague: Se programan dos pasos de enjuague del capilar antes de cada inyección. El primero, con hidróxido de sodio (NaOH), se utiliza para asegurar que los grupos silanol en la pared capilar se desprotonen, manteniendo una carga superficial constante. El segundo enjuague utiliza un tampón de funcionamiento para equilibrar el capilar y asegurar condiciones estables.
- Inyección de Muestra: Se establece la presión y el tiempo de inyección, por ejemplo, 0.5 psi durante 5 segundos, para introducir una cantidad precisa y reproducible de la muestra en el capilar.
- Paso de Electroforesis: Se selecciona el voltaje de separación (por ejemplo, 20 kV durante 5 minutos) y la polaridad (normal, que significa que el campo eléctrico es positivo en la entrada y negativo en la salida).
2. Preparación de Soluciones
La preparación de las muestras y estándares es un paso crítico para obtener resultados precisos:
- Soluciones Madre: Se preparan soluciones madre de alta concentración (por ejemplo, 500 partes por millón, ppm) de los componentes esperados en la soda, como aspartamo, cafeína y ácido benzoico, en agua.
- Solución Estándar Combinada: A partir de las soluciones madre, se prepara una solución estándar que contiene una concentración conocida de cada compuesto (por ejemplo, 150 ppm de aspartamo, 150 ppm de cafeína y 100 ppm de ácido benzoico). Esta solución se utilizará para identificar los picos en las muestras de refresco.
- Curva de Calibración: Para la cuantificación, se preparan varias soluciones estándar de concentraciones conocidas de un analito específico (por ejemplo, cafeína a 50, 100, 150 y 200 ppm). Estas se usarán para construir una curva de calibración que relacione el área del pico con la concentración.
- Muestras de Refresco: Las muestras de refresco deben desgasificarse con nitrógeno para eliminar el dióxido de carbono disuelto, que podría interferir con la inyección o la separación. Generalmente, se analizan sin dilución.
3. Ejecución de las Muestras
Con todas las soluciones preparadas, se colocan los viales que contienen las muestras estándar, las muestras de refresco, el tampón de funcionamiento y la solución de enjuague de hidróxido de sodio en el portamuestras del instrumento. Es fundamental registrar la ubicación de cada vial.
En el software del instrumento, se indica qué ranuras contienen las soluciones de enjuague y el primer vial de muestra. Luego, se procede a ejecutar la primera muestra. Posteriormente, se cambian los viales de entrada y se ejecutan el estándar de combinación, las diferentes concentraciones de cafeína y las muestras de refresco (regular y dietético).
4. Análisis de Datos
Una vez que todas las soluciones se han separado, se procede al análisis de los datos obtenidos:
- Identificación de Picos: Se utilizan los estándares para identificar los picos en las muestras de refrescos. Por ejemplo, una comparación de los tres picos observados en la muestra de refresco dietético con los estándares puede revelar la presencia de cafeína, aspartamo y ácido benzoico. En un refresco regular, es posible que solo se observe el pico de cafeína.
- Cuantificación: Se calcula el área máxima para cada solución estándar de cafeína y se construye una curva de calibración. Esta curva permite calcular la concentración de cafeína en cada muestra de refresco desconocida.
Aplicaciones Avanzadas de la Electroforesis Capilar
La electroforesis capilar no solo es una herramienta de laboratorio; se utiliza extensamente en una variedad de entornos académicos e industriales para separaciones especializadas y análisis complejos.
Control de Calidad en la Industria Farmacéutica
CE es un componente vital en las pruebas de control de calidad farmacéuticas. Tanto los medicamentos de moléculas pequeñas como los productos biológicos pueden analizarse mediante electroforesis capilar para detectar la presencia de productos secundarios, impurezas o para verificar la pureza. Además, es invaluable para determinar si las proteínas están correctamente plegadas, ya que el plegamiento puede afectar la carga proteica y, por ende, su movilidad electroforética.
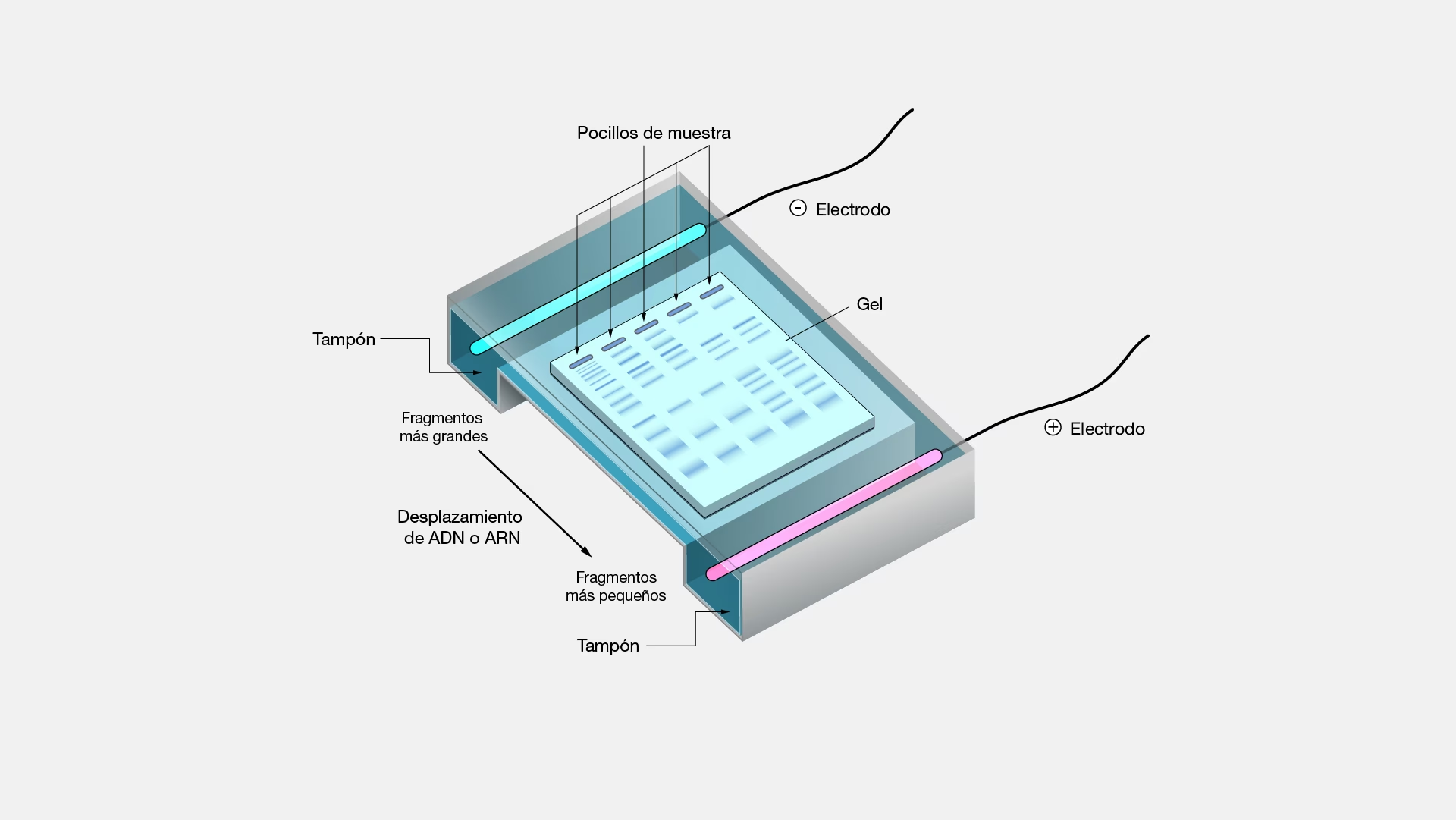
Separación y Secuenciación de ADN
Una de las aplicaciones más impactantes de la CE es la separación de ADN. Utilizando placas de micropocillos y múltiples matrices de capilares, los investigadores pueden aumentar significativamente el rendimiento de un solo experimento. Los fragmentos de ADN se separan en función de su tamaño con una resolución asombrosa, a veces de hasta un solo par de bases. Esto hace posible la secuenciación de fragmentos de ADN, así como la determinación de otros parámetros genéticos, como las variantes del número de copias, que son cruciales para diagnosticar posibles enfermedades genéticas.
Análisis de Modificaciones Proteicas
Las proteínas pueden ser modificadas por varios grupos funcionales que se unen químicamente en diferentes lugares. Diferentes copias de la misma proteína pueden variar en sus modificaciones, lo que alterará la carga y el tamaño de cada proteína. La ejecución de proteínas purificadas a través de un CE que está conectado a un espectrómetro de masas permite separar las proteínas en función de las modificaciones presentes y, además, identificar el tipo y la ubicación de la modificación. Esta capacidad es fundamental en la proteómica y el descubrimiento de fármacos.
¿Se puede utilizar la Electroforesis Capilar para separar Aminoácidos?
Sí, la electroforesis capilar ha sido ampliamente utilizada para la separación de aminoácidos y sus enantiómeros desde su introducción como técnica analítica. Se han publicado más de 150 estudios sobre este tema, lo que demuestra su eficacia y versatilidad en este campo.
Para la separación de aminoácidos, se han empleado principalmente dos variantes de la CE:
- Electroforesis de Zona Capilar (CZE): Separa los aminoácidos basándose en sus cargas y tamaños intrínsecos en un electrolito.
- Cromatografía Electrocinética Micelar (MEKC): Utiliza micelas (agregados de surfactantes) en el electrolito que actúan como una fase estacionaria pseudofija, permitiendo la separación de compuestos neutros y cargados.
Dado que muchos aminoácidos no absorben luz UV o no lo hacen de manera eficiente, a menudo se emplean esquemas de derivatización pre-columna. Estos esquemas implican la unión de un grupo cromóforo o fluoróforo a los aminoácidos antes de la separación, lo que permite una detección sensible. Se discuten criterios para la selección del agente derivatizante (pre- o post-columna), el cromóforo o fluoróforo, basándose en la sensibilidad y especificidad requeridas.
Los sistemas de detección utilizados incluyen métodos directos e indirectos, con un énfasis particular en los reactivos fluorogénicos y la detección por fluorescencia inducida por láser (LIF), que ofrecen una sensibilidad excepcional. Además, la CE es una herramienta poderosa para la separación de enantiómeros de aminoácidos, lo cual es crucial en la industria farmacéutica y en el estudio de la vida.
Tabla Comparativa: CE vs. Cromatografía Líquida de Alta Resolución (HPLC)
Aunque tanto la CE como la HPLC son técnicas de separación, tienen diferencias fundamentales que las hacen adecuadas para distintas aplicaciones.
| Característica | Electroforesis Capilar (CE) | Cromatografía Líquida de Alta Resolución (HPLC) |
|---|---|---|
| Principio de Separación | Movilidad electroforética (carga y tamaño) y flujo electroosmótico. | Interacción diferencial entre fase estacionaria y fase móvil (polaridad, tamaño, etc.). |
| Medio de Separación | Capilar estrecho lleno de electrolito. | Columna empaquetada con partículas porosas. |
| Volumen de Muestra | Nanolitros (nL). | Microlitros (µL). |
| Resolución | Muy alta (debido a la ausencia de difusión por remolino). | Alta, pero generalmente menor que CE. |
| Eficiencia | Extremadamente alta (millones de platos teóricos). | Alta (miles a cientos de miles de platos teóricos). |
| Consumo de Solvente | Muy bajo. | Moderado a alto. |
| Rango de Aplicación | Ideal para iones, proteínas, ADN, fármacos, pequeñas moléculas cargadas. | Amplio, para moléculas polares y no polares, grandes y pequeñas. |
| Sensibilidad | Alta, especialmente con detectores de fluorescencia inducida por láser. | Depende del detector, generalmente buena. |
Preguntas Frecuentes sobre la Electroforesis Capilar
- ¿Qué es el flujo electroosmótico (EOF) y por qué es importante?
- El EOF es el movimiento a granel del electrolito dentro del capilar, impulsado por el campo eléctrico. Es crucial porque transporta todas las especies (cargadas y neutras) a través del capilar y contribuye significativamente a la eficiencia de la separación al mantener un perfil de flujo plano, a diferencia del flujo parabólico en la cromatografía.
- ¿Qué información proporciona un electroferograma?
- Un electroferograma es un gráfico de la señal del detector frente al tiempo de elución. Proporciona información cualitativa (qué compuestos están presentes, identificados por su tiempo de elución característico) y cuantitativa (cuánto de cada compuesto hay, determinado por el área o altura del pico).
- ¿Para qué se utiliza la electroforesis capilar en la industria farmacéutica?
- En la industria farmacéutica, la CE se utiliza para el control de calidad de medicamentos (detección de impurezas y productos secundarios), la evaluación de la pureza de productos biológicos, el análisis de la integridad estructural de proteínas (por ejemplo, plegamiento incorrecto) y el estudio de interacciones fármaco-proteína.
- ¿Es la electroforesis capilar siempre mejor que la HPLC?
- No siempre es 'mejor', sino que es una técnica complementaria con ventajas específicas. La CE ofrece mayor resolución, menor consumo de muestra y reactivos, y es ideal para moléculas cargadas. Sin embargo, la HPLC puede ser más robusta para ciertas aplicaciones, tener mayor capacidad de carga y ser más adecuada para moléculas no cargadas o para la purificación preparativa a gran escala.
- ¿Qué tipos de moléculas puede separar la CE?
- La CE es extremadamente versátil y puede separar una amplia gama de moléculas, incluyendo iones inorgánicos y orgánicos, aminoácidos, péptidos, proteínas, nucleótidos, ácidos nucleicos (ADN y ARN), carbohidratos, fármacos, vitaminas y metabolitos, entre otros. Es particularmente eficaz para especies cargadas.
En resumen, la electroforesis capilar es una técnica analítica de gran alcance que ha revolucionado el análisis químico debido a su alta resolución, eficiencia y capacidad para trabajar con muestras mínimas. Desde la investigación fundamental hasta el control de calidad industrial, la CE continúa siendo una herramienta indispensable para desentrañar la complejidad de las mezclas moleculares y avanzar en nuestra comprensión del mundo a pequeña escala.
Si quieres conocer otros artículos parecidos a Electroforesis Capilar: Separación Molecular Eficaz puedes visitar la categoría Cabello.