31/10/2016
Los riñones son órganos vitales que desempeñan un papel fundamental en el mantenimiento de la salud general del cuerpo. Entre sus múltiples funciones, la más conocida es la de filtrar la sangre para eliminar desechos y el exceso de agua, formando la orina. En el corazón de esta intrincada maquinaria de filtración se encuentra una estructura microscópica y altamente especializada conocida como glomérulo. Entender qué es el glomérulo y cómo funciona es clave para comprender la fisiología renal y la importancia de cuidar estos órganos.
El glomérulo no es solo un simple filtro; es una obra maestra de la ingeniería biológica que garantiza que solo las sustancias no deseadas sean eliminadas, mientras que los componentes esenciales de la sangre, como las proteínas y las células sanguíneas, permanezcan en el torrente circulatorio. Su complejidad estructural y funcional lo convierte en un objetivo crucial para diversas enfermedades renales, y su estudio ha revelado detalles fascinantes sobre cómo el cuerpo mantiene su equilibrio interno. Acompáñanos en este recorrido para desentrañar los misterios de esta pequeña pero poderosa unidad funcional del riñón.
- ¿Qué es el Glomérulo? Definición y Estructura
- La Función Vital del Glomérulo: Filtración Sanguínea
- El Desarrollo Embrionario del Glomérulo
- Componentes Clave de la Barrera de Filtración Glomerular
- Mecanismos de Selectividad y Regulación
- Tabla Comparativa: Componentes de la Barrera de Filtración Glomerular
- Preguntas Frecuentes (FAQs)
- Conclusión
¿Qué es el Glomérulo? Definición y Estructura
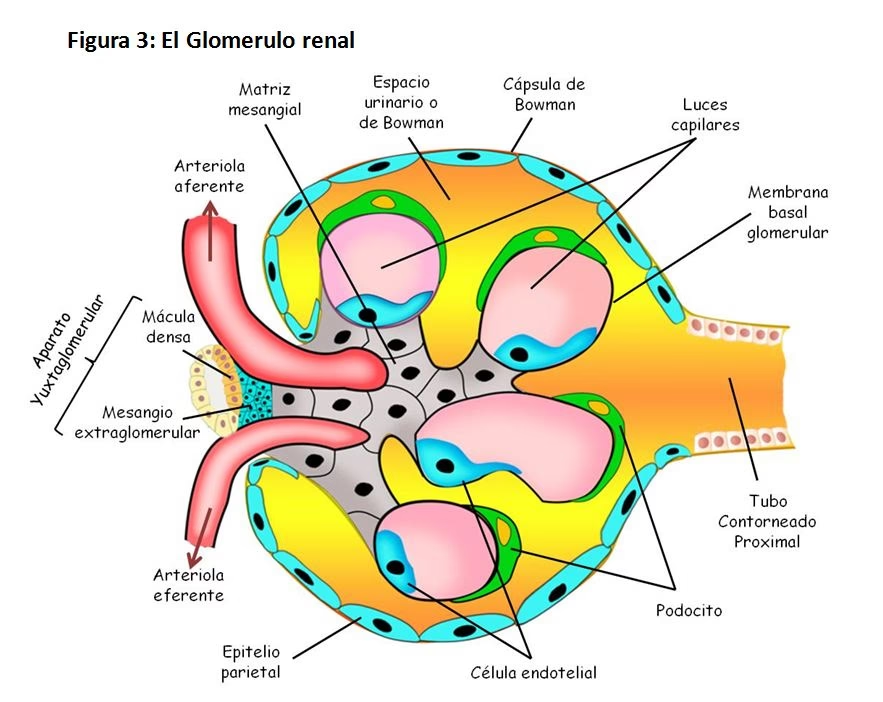
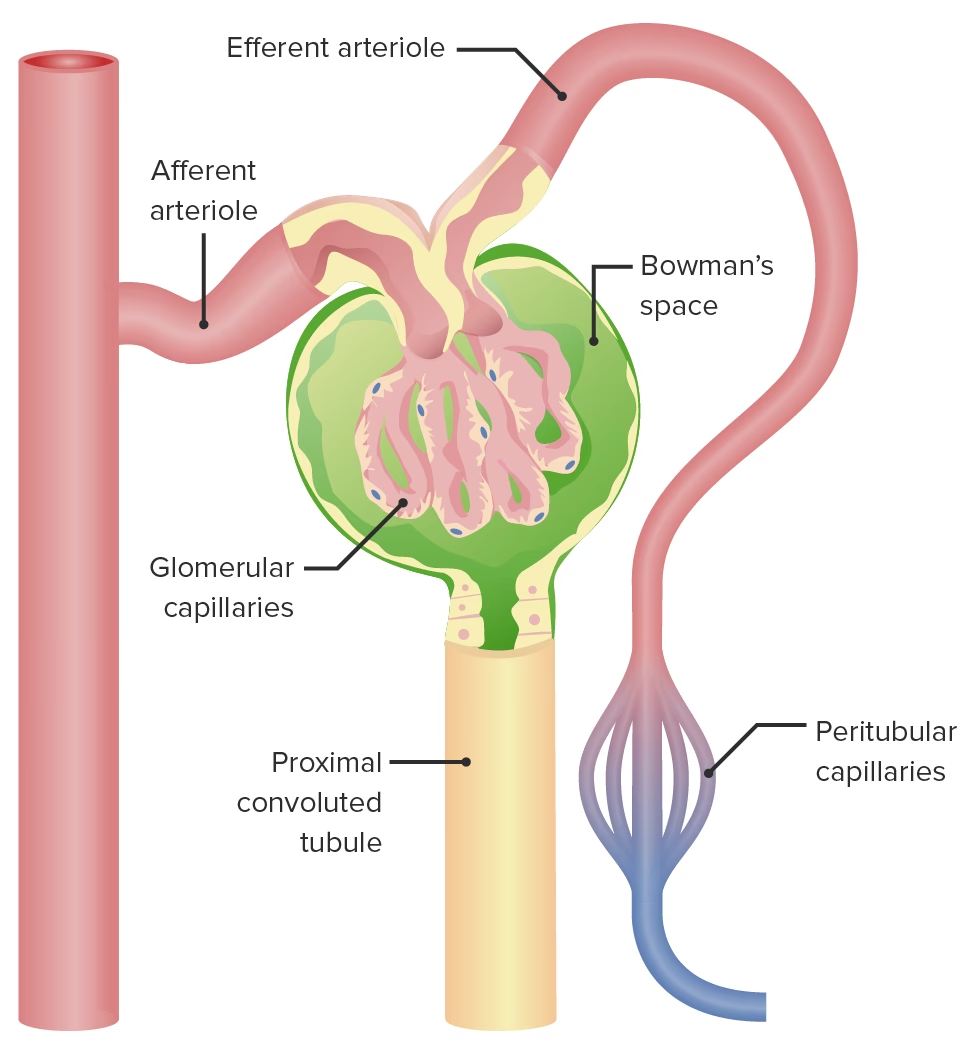
El glomérulo es una estructura compleja y altamente vascularizada que forma parte de la nefrona, la unidad funcional básica del riñón. Se define principalmente como un ovillo de capilares sanguíneos especializados, conocidos como capilares glomerulares, que están revestidos internamente por células endoteliales. Este ovillo capilar está encapsulado por una estructura en forma de copa llamada cápsula de Bowman, que a su vez está revestida por un tipo de células epiteliales altamente especializadas llamadas podocitos. Entre estas dos capas celulares (endoteliales y podocitarias) se encuentra una capa crucial: la membrana basal glomerular.
Estas tres capas —las células endoteliales fenestradas de los capilares, la membrana basal glomerular y los podocitos— funcionan de manera conjunta para formar la barrera de filtración glomerular, un sistema altamente selectivo que permite el paso de agua y pequeñas moléculas, pero restringe el de proteínas y células sanguíneas. La sangre llega al glomérulo a través de las arteriolas aferentes, una rama de la arteria renal, y es aquí donde comienza el proceso de filtración. Una vez que la sangre ha sido filtrada, regresa a la circulación sistémica a través de las arteriolas eferentes. La alta vascularización del glomérulo es notable; recibe aproximadamente 1100 mL de sangre por minuto, lo que subraya su eficiencia y su papel central en la depuración sanguínea.
La Función Vital del Glomérulo: Filtración Sanguínea
La principal y más crucial función del glomérulo es la filtración de la sangre. Este proceso es el primer paso en la formación de la orina y es esencial para eliminar los productos de desecho metabólicos y el exceso de líquidos del cuerpo, manteniendo así la homeostasis. Los podocitos, con sus intrincados procesos, son los principales responsables de permitir la filtración de toxinas, desechos metabólicos y macromoléculas pequeñas del torrente sanguíneo, al tiempo que impiden el paso de moléculas más grandes y esenciales, como las proteínas plasmáticas y las células sanguíneas. Si estas moléculas grandes pasaran al filtrado, se perderían en la orina, lo que podría llevar a graves problemas de salud.
La barrera de filtración glomerular actúa como un tamiz sofisticado, aplicando una doble selectividad: por tamaño y por carga. Las fenestraciones (pequeños poros) en las células endoteliales capilares, la composición de la membrana basal glomerular y los diafragmas de hendidura entre los procesos de los podocitos, todos contribuyen a esta selectividad. La membrana basal, por ejemplo, está cargada negativamente, lo que repele a las proteínas que también tienen una carga negativa, impidiendo su paso. Este mecanismo asegura que solo el ultrafiltrado glomerular, una solución libre de proteínas y células, pase a la cápsula de Bowman para su posterior procesamiento en los túbulos renales. La eficacia de esta función es vital para prevenir la acumulación de sustancias tóxicas en el cuerpo y para mantener el equilibrio de líquidos y electrolitos.
El Desarrollo Embrionario del Glomérulo
La formación del riñón mamífero en la embriología es un proceso fascinante que se desarrolla en varias etapas, comenzando con el mesodermo intermedio. Este tejido primitivo experimenta un patrón antero-posterior (AP) guiado por un delicado equilibrio entre el ácido retinoico y sus inhibidores (como Fgf8 y Cyp26). Esta variabilidad en los factores divide el mesodermo intermedio en tres zonas distintas: mesodermo intermedio anterior (alta actividad de ácido retinoico), mesodermo intermedio medio (actividad moderada de Fgf8) y mesodermo intermedio posterior (alta actividad de Fgf8 y Cyp26).
Estos morfógenos proporcionan una guía quimiotáctica a las células y dirigen la transición mesenquimal-epitelial del mesodermo intermedio anterior. Simultáneamente, el conducto pronefrítico se extiende posteriormente, y cuando alcanza el extremo caudal del embrión, la yema ureteral invade el mesénquima metanéfrico circundante, marcando el inicio de la nefrogénesis. La yema ureteral luego brota células epiteliales, un proceso mediado por el factor neurotrófico derivado de células gliales (GDNF) y el ácido retinoico, secretados desde el conducto néfrico hacia el mesénquima metanéfrico. En este momento, Wnt9b, emanando del metanefros con la ayuda de BMP7, impulsa la condensación del mesénquima metanéfrico para formar el mesénquima capuchón.
El mesénquima capuchón está compuesto por una población de progenitores de nefronas en la punta, y la formación de nefronas ocurre en el tallo del epitelio ureteral. Estos progenitores de nefronas se agrupan en la unión punta-tallo para formar los agregados pretubulares. Una secreción autócrina adicional de Wnt4 de estos agregados impulsa la transición mesénquima-epitelial, dando lugar a vesículas renales quísticas. La secuencia de reclutamiento de estas células progenitoras de nefronas en la vesícula renal ofrece trayectorias geométricas y funcionales únicas. Las células reclutadas en las primeras etapas contribuyen a la formación de los precursores tubulares distales, las reclutadas más tarde forman los precursores tubulares proximales, y las últimas reclutadas forman los precursores glomeruloides.
En esta etapa, se observan cambios estructurales en la vesícula renal quística, ya que se pliega hacia adentro para formar cuerpos en forma de coma y en forma de S. Estos cambios estructurales van acompañados de una expresión diferencial de Cadherina 1 y Jagged canonical notch ligand-1. Simultáneamente, se genera un gradiente de Wilms Tumor 1 (WT1) en el extremo distal de los cuerpos en forma de S, lo que marca el comienzo de la glomerulogénesis cuando un único capilar invade la hendidura glomerular. Este capilar luego se divide en seis o siete asas capilares, delineando así la etapa de asa capilar de la nefrogénesis. Durante el desarrollo, los podocitos inmaduros y las células endoteliales secretan sus propias láminas basales, que con el tiempo se fusionan para formar la membrana basal glomerular naciente. Esta maduración implica cambios en la expresión de laminina y la extensión de las redes arborizadas y procesos podocitarios, características estructurales clave que permiten su función de filtración.
Componentes Clave de la Barrera de Filtración Glomerular
La barrera de filtración glomerular (BFG) es una estructura altamente especializada que asegura la selectividad en el paso de sustancias desde la sangre hacia el espacio urinario. Está compuesta por tres elementos principales que trabajan en conjunto para cumplir esta función vital: las células endoteliales fenestradas de los capilares glomerulares, la membrana basal glomerular (MBG) y los podocitos.
La Membrana Basal Glomerular (MBG)
La membrana basal glomerular (MBG) es una matriz fibrosa, densa y porosa que se sitúa entre las células endoteliales vasculares y los podocitos. En humanos, tiene un grosor aproximado de 350 nm y está compuesta principalmente por proteínas de la matriz extracelular (MEC). Entre sus componentes más importantes se encuentran las cadenas heterotriméricas de colágeno tipo IV (α3, α4 y α5), nidogen-1 y 2, la proteína similar al antígeno de nefritis tubulointersticial (TINAGL1), glicoproteínas de heparán sulfato (agrina, perlecano, colágeno XVIII) y laminina 11 (α5β2γ1). Estas proteínas son sintetizadas tanto por los podocitos como por las células endoteliales.
La organización de la MBG implica una integración concertada de receptores y proteínas de la MEC que forman una red polimérica. Las dos moléculas más abundantes dentro de la MBG, la laminina y el colágeno tipo IV, se estabilizan mediante numerosas moléculas de puente. Esta red confiere selectividad por tamaño y carga, minimizando el paso de macromoléculas aniónicas (cargadas negativamente) hacia el filtrado. La orientación de las redes de colágeno y laminina dentro de la MBG es específica: las redes de colágeno α3α4α5 y α1α1α2 (IV) se centralizan, alejadas de la superficie de los podocitos, mientras que la laminina α5, la agrina y las integrinas β1 se alinean bimodalmente, hacia los podocitos.
La agrina es el proteoglicano de heparán sulfato más prominente de la MBG. Su extremo N-terminal se une a la laminina α5β2γ1, mientras que su extremo C-terminal interactúa con receptores como las integrinas en los podocitos, lo que en conjunto contribuye a la selectividad de carga de la MBG. Además, la agrupación de integrinas ayuda a la adhesión de alta afinidad de los podocitos con la MBG. La principal integrina que facilita esta adhesión es la integrina α3β1, apoyada por la tetraspanina CD151. Las deficiencias en la integrina α3 y CD151 pueden llevar a una MBG desorganizada y laminada y a procesos podocitarios menos especializados, lo que resulta en proteinuria severa, glomeruloesclerosis focal y segmentaria (GEFS) y enfermedad renal terminal (ERT).
Además de las integrinas, los distroglicanos confieren señales adhesivas a los podocitos al unir los filamentos de actina con la laminina en la interfaz de los procesos podocitarios y la MBG. Proteoglicanos aniónicos como el sindecano-1 también pueden modular la fuerza adhesiva de los podocitos regulando la expresión de la integrina β3 a través de la señalización autócrina. La MBG se caracteriza aún más por las quinasas de adhesión focal que están estrechamente ligadas a las integrinas (a través de paxilina y talina), formando adhesomas estabilizados para contrarrestar la distensión de la MBG durante la filtración. Estos complejos de proteínas, como el complejo ILK/PINCH/Parvin, actúan como centros de señalización para las integrinas y la red citoesquelética de actina de los podocitos, manteniendo la barrera de filtración glomerular y controlando la dinámica citoesquelética, previniendo así el borramiento de los procesos podocitarios y la proteinuria.
Los Podocitos: Guardianes de la Filtración
Los podocitos son células epiteliales muy especializadas que constituyen la última capa de la barrera de filtración glomerular. Poseen procesos primarios y secundarios que se envuelven alrededor de los capilares glomerulares, formando una compleja red arborizada. Estas células exhiben una red citoesquelética dinámica que les permite mantener la permselectividad glomerular intrínseca, evitando la obstrucción del filtro durante la filtración molecular. Los procesos podocitarios arborizados se unen físicamente con los podocitos vecinos mediante interdigitaciones, lo que resulta en la formación de poros de aproximadamente 12.1 nm, conocidos como diafragmas de hendidura.

Los podocitos también promueven la proliferación y el mantenimiento de las células endoteliales fenestradas mediante la secreción de moléculas pro-angiogénicas, incluyendo el factor de crecimiento endotelial vascular (VEGFA), la Angiopoyetina 1 (ANGPT1) y el factor derivado de células estromales 1 (SDF1). De esta manera, estas redes de podocitos arborizadas con células endoteliales fenestradas son los actores clave de la BFG. La MBG madura en su etapa final consiste en varias proteínas, incluyendo Laminina 11 y colágeno tipo IV α3, α4 y α5 heterotrímeros.
El Diafragma de Hendidura: Un Filtro Preciso
Los principales guardianes de la barrera de filtración glomerular son los podocitos y sus diafragmas de hendidura. El diafragma de hendidura es una estructura de unión altamente especializada que se extiende entre los procesos podocitarios adyacentes. Los principales componentes de este diafragma incluyen proteínas como la nefrina (NPHS1) y proteínas similares a la nefrina (NEPH1 y NEPH3). La nefrina es la proteína principal del diafragma de hendidura y es fundamental para su función. NEPH1, N-WASP y Arp2/3 son proteínas críticas para el desarrollo de los procesos podocitarios arborizados.
La nefrina (NPHS1) se encuentra en la porción apical del diafragma de hendidura y contribuye a la dinámica citoesquelética, induciendo la polimerización de actina. También puede interactuar con dianas citoplasmáticas como PI3K para activar Akt y cofilina, ayudando así en el remodelado de la actina durante el estrés mecánico. Los podocitos están envueltos por agrina, perlecano y otros proteoglicanos cargados negativamente, junto con podocalixina, glicano-1 y sindecano-4, que contribuyen a la selectividad de carga del diafragma de hendidura.
El diafragma de hendidura también es rico en proteínas de unión estrecha, como ZO-1, CASK, espectrinas, JAMA-A, cingulinas e IQGAP1, que preservan las arborizaciones del podocito y previenen la fusión de los procesos podocitarios y la proteinuria con una barrera de carga selectiva a las proteínas. Además, se ha sugerido un vínculo directo entre el adhesoma del podocito y la señalización del diafragma de hendidura a través del ensamblaje de quinasas ligadas a integrinas con α-actinina 4. Otra proteína importante es la Podocina (NPHS2), miembro de la familia de proteínas estomatinas, que se localiza en el sitio apical del diafragma de hendidura. La expresión de NPHS2 está regulada por la activación y translocación del factor de transcripción LIM homeobox 1-ß (LMX1ß) al núcleo. Las mutaciones en LMX1B están asociadas con el síndrome uña-rótula, que afecta el fenotipo de los podocitos terminalmente diferenciados.
Mecanismos de Selectividad y Regulación
La filtración glomerular es un proceso altamente regulado que va más allá de un simple tamizaje físico. Involucra complejos mecanismos de selectividad que operan a nivel molecular y biofísico, asegurando que el cuerpo retenga lo que necesita y elimine solo los desechos.
El Modelo Electrocinético de Filtración
Según el modelo electrocinético propuesto por Moeller y sus colegas, se genera un campo eléctrico a lo largo de la pared capilar glomerular durante la filtración que ayuda a la migración de moléculas aniónicas (cargadas negativamente). La migración de estas moléculas se guía por la repulsión de los residuos sialilados, mediante electroforesis. En este proceso, la nefrina (NPHS1) regula la permeabilidad de la membrana basal glomerular a través de la compresión en un gradiente creciente desde la luz hasta la capa de podocitos de la barrera de filtración. De este modo, la nefrina rige la selectividad por tamaño y carga de la barrera de filtración glomerular. La anisotropía electroforética establece un equilibrio entre la compresión radial y la tensión circunferencial a lo largo de la barrera de filtración, favoreciendo una amplia dispersión espacial de las macromoléculas y restringiendo la transmisión de proteínas al compartimento urinario.
Modulación del Microambiente y Respuesta a la Lesión
El microambiente local modula los ciclos de organización y desorganización de los procesos podocitarios para adaptarse a una alta permeabilidad hidráulica. Por ejemplo, el canal de calcio TRPC6 ayuda a los podocitos a sentir su microambiente y apoya el remodelado citoesquelético en respuesta a la presión glomerular, el flujo de líquido y la tasa de filtración. Además, la fosfolipasa C puede activar el TRPC6, permitiendo un rápido influjo de iones de calcio en los podocitos. Como resultado, una alta concentración intracelular de Ca(II) reduce la expresión de nefrina (NPHS1) y sinaptopodina en el diafragma de hendidura, lo que aumenta la actividad de RhoA y la desorganización de la actina.
Otra proteína multifuncional, la proteína asociada a CD2 (CD2AP), se une a NPHS1, NPHS2, sinaptopodina y el sustrato de Src cortactina, y regula la nucleación de actina a través del complejo Arp2/3. Durante una lesión, los podocitos experimentan un borramiento y retracción de sus procesos, lo que les impide contrarrestar la alta presión hidrostática de filtración, lo que lleva a la proteinuria. Aunque la mayoría de los estudios hasta la fecha se han centrado en líneas celulares inmortalizadas y modelos animales, las tecnologías emergentes en sistemas microfluídicos pueden desarrollarse utilizando tejidos derivados de células iPS humanas para imitar funciones biológicas humanizadas miniaturizadas.
Tabla Comparativa: Componentes de la Barrera de Filtración Glomerular
| Componente | Descripción | Función Principal | Moléculas Clave |
|---|---|---|---|
| Células Endoteliales Fenestradas | Capa interna que recubre los capilares glomerulares. Presentan poros (fenestraciones) que permiten el paso de líquidos. | Primer filtro, impiden el paso de células sanguíneas, secretan moléculas pro-angiogénicas. | VEGFA, ANGPT1, SDF1 |
| Membrana Basal Glomerular (MBG) | Matriz extracelular densa y cargada negativamente, situada entre las células endoteliales y los podocitos. | Principal filtro de tamaño y carga; retiene macromoléculas y proteínas cargadas negativamente. | Colágeno tipo IV (α3, α4, α5), Laminina 11 (α5β2γ1), Agrina, Perlecano, Integrinas. |
| Podocitos y Diafragma de Hendidura | Células epiteliales especializadas con procesos complejos que se interdigitan, formando poros de filtración (diafragmas de hendidura). | Filtración fina de tamaño y carga; evitan el paso de proteínas pequeñas y medianas; mantienen la integridad de la MBG. | Nefrina (NPHS1), Podocina (NPHS2), NEPH1/3, CD2AP, TRPC6. |
Preguntas Frecuentes (FAQs)
¿Por qué es tan importante el glomérulo para la salud?
El glomérulo es crucial porque realiza la etapa inicial y más crítica de la filtración de la sangre en los riñones. Sin un glomérulo que funcione correctamente, el cuerpo no podría eliminar eficazmente las toxinas, los productos de desecho metabólicos y el exceso de líquidos. Esto llevaría a una acumulación de sustancias nocivas en la sangre, lo que se conoce como uremia, y a un desequilibrio severo de líquidos y electrolitos, lo cual es incompatible con la vida a largo plazo. Es, en esencia, el purificador principal de la sangre.
¿Qué sucede si el glomérulo no funciona correctamente?
Cuando el glomérulo no funciona adecuadamente, su capacidad de filtración se ve comprometida. Esto puede manifestarse de varias maneras, dependiendo de la naturaleza del daño. Si el filtro se daña y se vuelve demasiado permeable, puede permitir que las proteínas (como la albúmina) o incluso las células sanguíneas pasen a la orina, una condición conocida como proteinuria o hematuria, respectivamente. Si la capacidad de filtración disminuye drásticamente, los desechos se acumulan en la sangre, lo que lleva a la insuficiencia renal. Enfermedades como la glomerulonefritis, la nefropatía diabética o la glomeruloesclerosis focal y segmentaria (GEFS) son ejemplos de afecciones que afectan directamente al glomérulo.
¿Qué es la proteinuria y cómo se relaciona con el glomérulo?
La proteinuria es la presencia de cantidades anormales de proteínas en la orina. Normalmente, el glomérulo, con su selectividad de tamaño y carga, impide que las proteínas grandes, como la albúmina, pasen de la sangre al filtrado glomerular. Si el glomérulo está dañado, especialmente la membrana basal glomerular o los podocitos y sus diafragmas de hendidura, esta barrera se vuelve defectuosa, permitiendo que las proteínas se “escapen” a la orina. La proteinuria es un signo clave de daño glomerular y, si no se trata, puede progresar a una enfermedad renal crónica.
¿Se puede regenerar un glomérulo dañado?
La capacidad de regeneración del glomérulo en humanos adultos es limitada. Una vez que los podocitos se pierden o se dañan significativamente, o cuando la estructura glomerular se esclerosiza (se cicatriza), la recuperación de la función glomerular es difícil. Las investigaciones actuales se centran en comprender mejor los mecanismos de reparación y en desarrollar terapias que puedan prevenir el daño, ralentizar su progresión o, en el futuro, quizás inducir la regeneración de las estructuras glomerulares. Sin embargo, en la actualidad, el daño glomerular severo a menudo conduce a la insuficiencia renal terminal, que requiere diálisis o trasplante de riñón.
¿Cómo se diagnostican las enfermedades que afectan al glomérulo?
El diagnóstico de las enfermedades glomerulares generalmente implica una combinación de pruebas. Los análisis de orina son fundamentales para detectar la presencia de proteinuria y hematuria. Los análisis de sangre miden la función renal (creatinina, BUN) y pueden buscar marcadores de inflamación o autoanticuerpos. Las pruebas de imagen, como la ecografía renal, evalúan el tamaño y la estructura de los riñones. Sin embargo, el método diagnóstico más definitivo para muchas glomerulopatías es la biopsia renal, donde se toma una pequeña muestra de tejido renal para su examen microscópico detallado.
Conclusión
El glomérulo es, sin lugar a dudas, una de las estructuras más sofisticadas y vitales del cuerpo humano. Su capacidad para filtrar selectivamente la sangre, eliminando desechos y manteniendo sustancias esenciales, es fundamental para la vida y la salud. Desde su intrincado desarrollo embrionario hasta su compleja función en la edad adulta, cada componente del glomérulo, desde las células endoteliales y la membrana basal glomerular hasta los especializados podocitos y sus diafragmas de hendidura, trabaja en una sinfonía perfecta para asegurar la homeostasis.
Comprender la importancia de esta diminuta unidad funcional nos permite apreciar la magnitud de su papel en la prevención de enfermedades y en la preservación de nuestra calidad de vida. El estudio continuo del glomérulo no solo profundiza nuestro conocimiento sobre la fisiología renal, sino que también allana el camino para nuevas estrategias terapéuticas que algún día podrían restaurar la función de este invaluable filtro natural.
Si quieres conocer otros artículos parecidos a El Glomérulo Renal: Pilar de la Filtración Sanguínea puedes visitar la categoría Cabello.