08/02/2023
Imagina por un momento que el agua, ese líquido vital que conocemos tan bien, pudiera desafiar las leyes más básicas de la física. ¿Podría ascender por sí misma, incluso ir cuesta arriba, en contra de la fuerza implacable de la gravedad? La respuesta instintiva es un rotundo no. Sin embargo, la naturaleza y la ciencia nos demuestran una y otra vez que lo imposible puede volverse posible bajo ciertas condiciones. Prepárate para descubrir un fenómeno asombroso, presente en cada rincón de nuestro mundo, desde las raíces de un árbol hasta la forma en que tu café se absorbe en una servilleta: la capilaridad, también conocida como acción capilar.
Este artículo te guiará a través de un experimento sencillo pero revelador que puedes hacer en casa, desvelando el misterio de cómo el agua puede ascender contra todo pronóstico. Exploraremos los principios fundamentales que rigen este comportamiento inusual del agua y cómo estas propiedades microscópicas tienen un impacto gigante en nuestra vida cotidiana y en la naturaleza.
- ¿Qué es la Capilaridad? El Secreto del Agua Ascendente
- El Experimento Clásico del Papel de Cocina: Observando la Magia
- Decodificando la Capilaridad: Cohesión, Adhesión y Tensión Superficial
- La Capilaridad en Nuestro Día a Día: Más Allá del Laboratorio
- Factores que Influyen en la Acción Capilar
- Preguntas Frecuentes (FAQ) sobre la Capilaridad
¿Qué es la Capilaridad? El Secreto del Agua Ascendente
La capilaridad es una propiedad física del agua (y de otros líquidos) que le permite ascender o descender por un tubo capilar (un tubo de diámetro muy pequeño) o a través de materiales porosos, incluso en contra de la fuerza de la gravedad. Es como si el agua tuviera su propio sistema de elevación incorporado. Este fenómeno es crucial para la vida en la Tierra y para innumerables procesos que damos por sentado. Pero, ¿cómo es esto posible? La respuesta reside en las interacciones moleculares del agua, un ballet invisible de atracción y unión que la convierte en un líquido verdaderamente único.
El Experimento Clásico del Papel de Cocina: Observando la Magia
Para entender la capilaridad de primera mano, no necesitas un laboratorio sofisticado. Con unos pocos materiales comunes, puedes ser testigo de cómo el agua desafía la gravedad ante tus ojos. Este experimento es ideal para niños y adultos curiosos, ya que demuestra de forma visual y clara el principio de la acción capilar.
Materiales Necesarios
- Dos vasos (preferiblemente transparentes para una mejor observación).
- Agua.
- Colorante alimentario (opcional, pero altamente recomendado para hacer el fenómeno más visible y atractivo). También puedes usar acuarelas o témperas.
- Un trozo de papel de cocina (servilleta de papel o toalla de papel).
Procedimiento Detallado: Pasos para el Descubrimiento
- Prepara el Vaso con Agua: Llena uno de los vasos con agua hasta la mitad o un poco más. Asegúrate de que haya suficiente líquido para que el experimento sea efectivo.
- Añade Color: Este paso es clave para la visibilidad. Vierte unas gotas de colorante alimentario (o disuelve un poco de acuarela/témpera) en el agua. Remueve suavemente para que el color se disperse por completo. ¡Cuanto más vibrante sea el color, más fácil será seguir el viaje del agua!
- Prepara el Papel de Cocina: Toma un trozo de papel de cocina y dóblalo o retuércelo longitudinalmente para formar una tira. La idea es crear una especie de puente o mecha.
- Conecta los Vasos: Coloca el vaso vacío junto al vaso lleno de agua coloreada. Introduce un extremo del papel de cocina en el agua coloreada, asegurándote de que toque el fondo del vaso. Luego, introduce el otro extremo del papel de cocina en el vaso vacío, también hasta el fondo. El papel debe conectar ambos vasos de forma estable.
- Espera y Observa: La paciencia es una virtud en la ciencia. Al principio, puede que no veas mucho, pero si observas con atención, notarás cómo el agua comienza a ascender por el papel. Este proceso puede tardar varias horas en completarse, pero verás el progreso de forma gradual. Revisa de vez en cuando para ver cómo el color se extiende.
¿Qué Ocurrió? La Evidencia Visual
Después de un tiempo, te darás cuenta de que el agua coloreada ha escalado poco a poco por el papel de cocina y ha empezado a acumularse en el vaso que inicialmente estaba vacío. El proceso continuará hasta que el nivel de agua en ambos vasos se iguale. ¡Has sido testigo de la acción capilar en su máxima expresión!
Decodificando la Capilaridad: Cohesión, Adhesión y Tensión Superficial
Para entender realmente por qué el agua se comporta de esta manera, debemos adentrarnos en el mundo microscópico de sus moléculas. La capilaridad es el resultado de una compleja interacción entre tres fuerzas fundamentales: la cohesión, la adhesión y la tensión superficial.
Cohesión: El Amor Propio del Agua
Las moléculas de agua son como pequeños imanes que se atraen fuertemente entre sí. Esta atracción mutua se conoce como cohesión. Las moléculas de agua están unidas por enlaces de hidrógeno, lo que las hace querer permanecer muy juntas. Es esta fuerza de cohesión la que le da al agua su propiedad de "gota", haciendo que las gotas se mantengan unidas en lugar de dispersarse. Es el lazo de unión que mantiene al agua como un líquido cohesionado.
Adhesión: El Agua se Enamora de Todo
Además de quererse a sí mismas, las moléculas de agua también sienten una fuerte atracción por otras superficies. Esta tendencia del agua a pegarse a otras sustancias se llama adhesión. En nuestro experimento, el agua se adhiere a las fibras microscópicas del papel de cocina. Piensa en cómo el agua se adhiere al cristal de un vaso, formando pequeñas gotas que se pegan a la superficie en lugar de resbalar completamente.
Tensión Superficial: La Piel Invisible del Agua
La tensión superficial es una consecuencia directa de la cohesión. En la superficie del agua, las moléculas no tienen otras moléculas de agua por encima o por los lados con las que unirse. Esto hace que las fuerzas de cohesión las tiren hacia abajo y hacia los lados, creando una especie de 'piel' elástica o 'película' en la superficie del líquido. Esta 'piel' es lo suficientemente fuerte como para soportar pequeños objetos, como insectos caminando sobre el agua, o para formar gotas esféricas. Es esta tensión superficial la que permite que el agua sea 'arrastrada' hacia arriba en la capilaridad.
| Característica | Cohesión | Adhesión |
|---|---|---|
| Definición | Atracción entre moléculas iguales (ej. agua-agua). | Atracción entre moléculas diferentes (ej. agua-papel). |
| Fuerza | Responsable de la unión interna del líquido. | Responsable de que el líquido se pegue a superficies. |
| Ejemplo Clave | Las gotas de agua se mantienen unidas. | El agua 'moja' una superficie o escala por ella. |
| Papel en Capilaridad | Mantiene las moléculas unidas mientras suben. | Permite que el agua se 'agarre' a las paredes del capilar. |
En nuestro experimento, el agua se pega a los diminutos poros o 'capilares' del papel de cocina por adhesión. A medida que las moléculas de agua se adhieren y suben por las fibras del papel, las moléculas de agua que están debajo y a su lado son arrastradas hacia arriba debido a la fuerte cohesión entre ellas y la tensión superficial en la superficie del agua. Es como una cadena humana donde cada molécula tira de la siguiente, superando la gravedad hasta que el equilibrio de fuerzas se alcanza en ambos vasos.
La Capilaridad en Nuestro Día a Día: Más Allá del Laboratorio
La acción capilar no es solo un truco de laboratorio; es un fenómeno omnipresente que juega un papel vital en la naturaleza y en la tecnología. Una vez que entiendes sus principios, empezarás a verla por todas partes.
Las Plantas: Ingenieros Hidráulicos Naturales
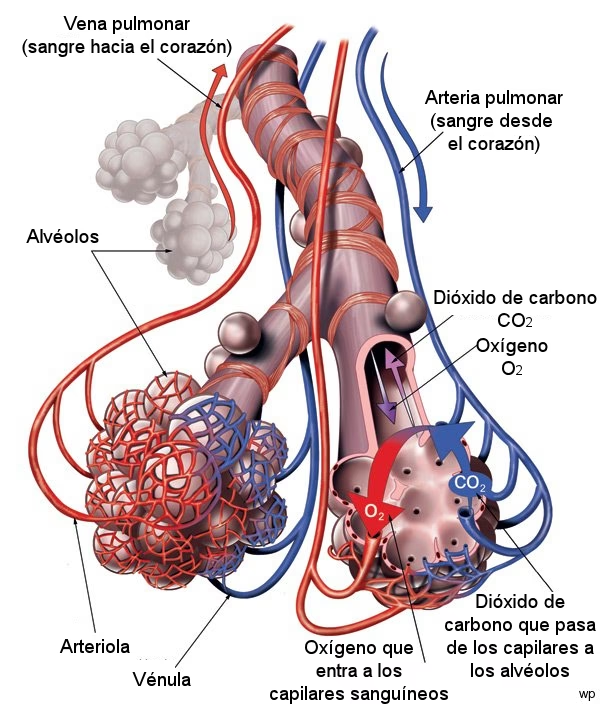
Uno de los ejemplos más impresionantes y esenciales de capilaridad se encuentra en el mundo vegetal. ¿Alguna vez te has preguntado cómo un árbol gigante, como una secuoya, puede transportar agua desde sus raíces en el suelo hasta sus hojas más altas, a decenas de metros de altura? La respuesta es la capilaridad. Las plantas poseen diminutos tubos llamados xilema que actúan como capilares. El agua es absorbida por las raíces y asciende por estos tubos gracias a la adhesión del agua a las paredes del xilema y la cohesión entre las moléculas de agua, creando una columna continua que se eleva contra la gravedad. Es un sistema de bombeo natural increíblemente eficiente.
Las Toallas: Héroes de la Absorción
Cuando te secas después de una ducha, la toalla absorbe el agua de tu piel. Esto es pura capilaridad en acción. Las fibras de la toalla (algodón, microfibra, etc.) están llenas de espacios microscópicos que actúan como capilares. El agua es atraída hacia estos espacios y se distribuye por todo el tejido, dejando tu piel seca. Lo mismo ocurre con las esponjas, el papel secante o el papel de cocina que usamos para limpiar derrames.
Lágrimas y Galletas: Sorpresas Cotidianas
- Las Lágrimas: Incluso en nuestros propios cuerpos, la capilaridad tiene su papel. Los conductos lagrimales que drenan las lágrimas de nuestros ojos son pequeños capilares que utilizan este principio para mantener nuestros ojos húmedos y eliminar el exceso de líquido.
- Galletas en la Leche: ¿Quién no ha mojado una galleta en la leche o el café y ha visto cómo el líquido asciende rápidamente por ella? Las galletas, al ser porosas, actúan como un material capilar. Los pequeños espacios entre las partículas de harina absorben el líquido por acción capilar, haciendo que la galleta se ablande y, a veces, se rompa si la dejas demasiado tiempo.
Otros Ejemplos Sorprendentes
- Mechas de Lámparas de Aceite: Las mechas de las velas o lámparas de aceite funcionan por capilaridad, extrayendo el combustible líquido hacia la llama.
- Tintas y Plumas: La forma en que la tinta fluye a través de los pequeños canales de una pluma estilográfica o se absorbe en el papel también es un ejemplo de acción capilar.
- Ascenso del Agua Subterránea: En el suelo, el agua puede ascender desde capas más profundas hacia la superficie a través de los poros del terreno, un proceso vital para la humedad del suelo en épocas de sequía.
Factores que Influyen en la Acción Capilar
La magnitud de la elevación capilar no es siempre la misma; depende de varios factores clave:
El Diámetro del Capilar
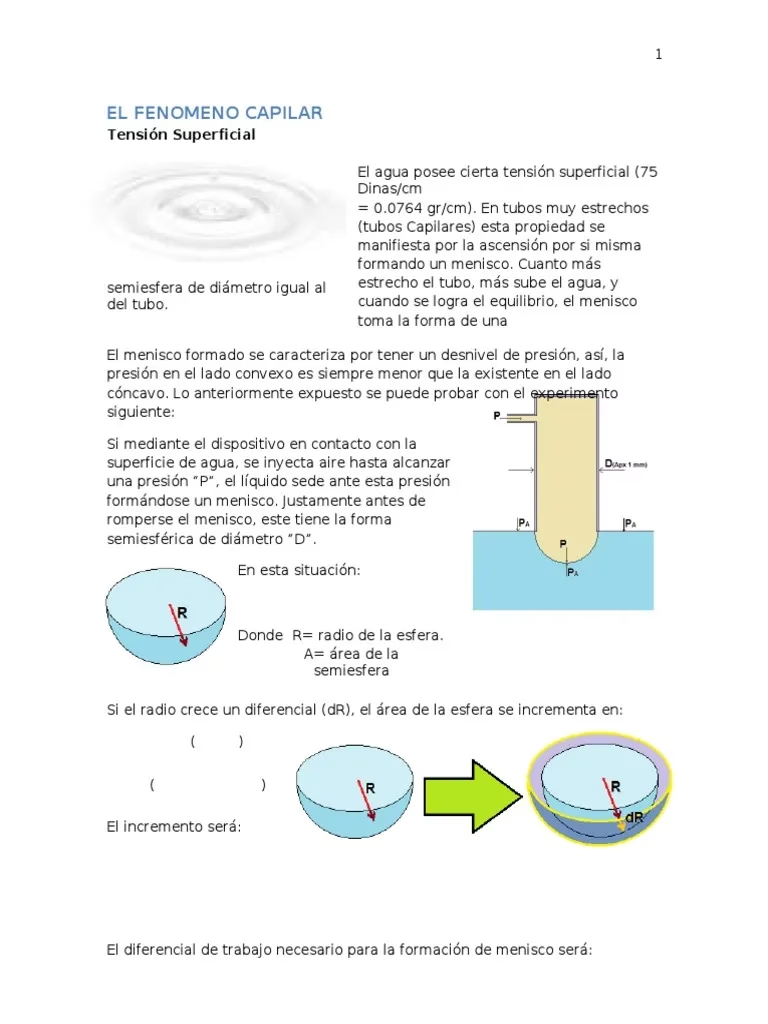
Una regla fundamental de la capilaridad es que cuanto más estrecho sea el tubo o el espacio poroso, mayor será la altura a la que ascenderá el líquido. Esto se debe a que la relación entre la superficie de contacto (donde ocurre la adhesión) y el volumen del líquido es mayor en capilares más finos, permitiendo que las fuerzas de adhesión y cohesión sean más efectivas contra la gravedad.
La Naturaleza del Líquido
No todos los líquidos exhiben la misma capilaridad. Depende de las fuerzas de cohesión y adhesión específicas de cada líquido. El agua, con sus fuertes enlaces de hidrógeno, tiene una capilaridad muy pronunciada. Otros líquidos, como el mercurio, tienen fuerzas de cohesión tan fuertes que la adhesión a las superficies es menor, lo que hace que su nivel en un capilar sea menor que en el recipiente principal, incluso formando un menisco convexo.
La Temperatura
La temperatura puede afectar la capilaridad. Generalmente, a medida que la temperatura aumenta, la tensión superficial y las fuerzas de cohesión del agua disminuyen. Esto puede resultar en una menor altura de ascenso capilar, ya que las moléculas están más energizadas y menos unidas.
Preguntas Frecuentes (FAQ) sobre la Capilaridad
¿Es la capilaridad lo mismo que la absorción?
La capilaridad es un mecanismo clave de la absorción. La absorción es el proceso general por el cual una sustancia toma o retiene otra. La capilaridad describe específicamente cómo un líquido es atraído y se mueve a través de pequeños espacios o materiales porosos debido a las fuerzas de cohesión y adhesión. Así, toda capilaridad es absorción, pero no toda absorción es capilaridad (por ejemplo, una esponja absorbe agua por compresión, no solo por capilaridad).
¿Por qué el agua sube más en tubos más delgados?
En tubos más delgados, la superficie de contacto del agua con las paredes del tubo es mayor en proporción al volumen de agua en el tubo. Esto significa que las fuerzas de adhesión a las paredes tienen un efecto proporcionalmente mayor sobre el agua, permitiéndole 'tirar' de más agua hacia arriba contra la gravedad. Cuanto más estrecho es el tubo, más fuerte es la influencia de la adhesión sobre el volumen de agua contenido.
¿La capilaridad solo ocurre con el agua?
No, la capilaridad puede ocurrir con cualquier líquido, aunque el grado de ascenso o descenso variará según las propiedades específicas de ese líquido (sus fuerzas de cohesión y adhesión con la superficie). Sin embargo, el agua es un ejemplo muy notable debido a sus fuertes fuerzas de cohesión y adhesión.
¿Cómo afecta la temperatura a la capilaridad?
A medida que la temperatura de un líquido aumenta, sus moléculas se mueven más rápidamente y las fuerzas intermoleculares (como la cohesión y la tensión superficial) tienden a debilitarse. Esto generalmente resulta en una disminución de la altura a la que el líquido puede ascender por acción capilar, ya que las fuerzas que impulsan el ascenso son menos potentes.
La capilaridad es un testimonio fascinante de cómo las propiedades a nivel molecular pueden tener efectos macroscópicos profundos. Desde el simple experimento con papel de cocina hasta el transporte de agua en los árboles más altos del planeta, este fenómeno nos recuerda la complejidad y la belleza inherente a los procesos naturales. La próxima vez que veas una gota de agua adherirse a una superficie o un papel secante absorber un derrame, recordarás la increíble danza de la cohesión, la adhesión y la tensión superficial que hace posible la magia del agua.
Si quieres conocer otros artículos parecidos a La Magia del Agua: Capilaridad Al Descubierto puedes visitar la categoría Cabello.